编者按:胰腺癌作为全球范围内的重大健康挑战,非转移性胰腺癌的治疗一直是医学领域的研究焦点。在2024中国整合肿瘤学大会(CCHIO)上,复旦大学附属肿瘤医院徐近教授在做了题为“非转移性胰腺癌的新辅助和转化治疗”的专题报告,展示这些创新治疗策略如何为非转移性胰腺癌患者的治疗带来变革。现将内容整理如下,以飨读者。
徐近 教授
复旦大学附属肿瘤医院
主任医师,博士生导师
现任复旦大学附属肿瘤医院胰腺外科主任,胰腺肿瘤综合治疗部主任。
擅长胰腺各种良恶性肿瘤的微创、开放手术,胰腺周围包括十二指肠、壶腹部、胆囊胆管、脾脏、后腹膜肿瘤的外科切除,胰腺癌和神经内分泌肿瘤的综合治疗。
兼任中国抗癌协会胰腺肿瘤整合康复专业委员会主任委员、中国抗癌协会胰腺癌专业委员会常委、中国抗癌协会神经内分泌肿瘤专业委员会常委、上海市抗癌协会神经内分泌肿瘤专业委员会主任委员等。荣获上海市卫健委杰出青年医学人才,上海市职工优秀创新成果一等奖,上海市优秀发明金奖,获评2023年第八届医学家年会。
一、预后评分与治疗目标:精准决策的基石
(一)预后评分系统:多维度评估风险
在非转移性胰腺癌的治疗中,精准的预后评估对于制定个性化治疗方案至关重要。一项大规模研究针对1835例患者展开,这些患者初始均接受至少 1个周期的(m)FOLFIRINOX治疗,并依据ABC三个维度进行评分。其中,肿瘤范围(PR:0;BR,1;LA:2)、CA19-9水平(≤500:0,>500:1)和WHO体力状态(WHO 0:0;WHO≥1:1)是评分的关键因素。研究结果显示,预后评分与患者的切除率和R0切除率密切相关(图1)。例如,评分为0分的患者中位OS可达21.1个月,切除率高达 88.8%;而评分为4分的患者中位OS仅为14.9个月,切除率为55.3%。

图1. ABC评分与生存结局
(二)治疗目标:全方位提升治疗效果
1.削减微转移病灶:降低复发风险
新辅助治疗的首要目标之一是减少术后微转移病灶,从而降低复发率。通过检测循环肿瘤DNA(ctDNA),研究人员发现了一些关键信息。在一项研究中,对42例患者的血浆样本进行检测,术前有62%的患者检测到 KRAS突变的ctDNA,术后仍有37%的患者存在。令人担忧的是,术后 ctDNA持续阳性的患者100%出现复发,即便接受了基于吉西他滨的辅助化疗,这表明单纯辅助化疗在清除微转移病灶方面存在局限性。而在另一项研究中,患者接受新辅助和辅助mFOLFIRINOX治疗后,术后4周 ctDNA阴性的患者OS明显优于ctDNA阳性患者,12个月无进展生存期(PFS)达67%(图2)。
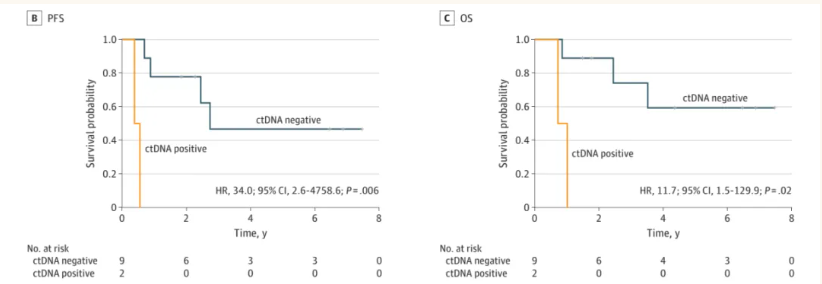
图2. ctDNA与预后关系
2.患者筛选:优化手术决策
新辅助治疗还具有筛选患者的重要作用。多项随机对照试验表明,可切除胰腺癌(RPC)患者在接受新辅助治疗后,切除率虽有所降低,但总体生存(OS)期却显著延长。这看似矛盾的结果实则揭示了新辅助治疗的筛选价值,它能够帮助医生识别出那些真正能从手术中获益的患者,避免不必要的手术干预,使手术治疗更加精准有效。
3.提高R0切除率:改善患者生存
R0切除(切缘大于1mm无肿瘤残留)是影响胰腺癌患者预后的关键因素之一。一项涵盖357例患者的研究显示,新辅助治疗后,R0切除患者的 OS明显长于R1切除患者(41.0个月 vs. 20.7个月),在接受辅助化疗的患者中,这种差异更为显著(44.8个月 vs. 20.1个月)(图3)。
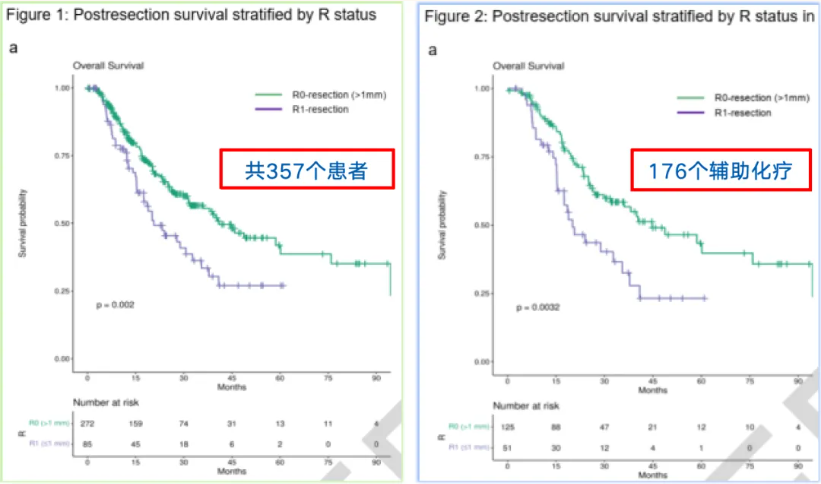
图3. R0切除与R1切除在生存概率上的显著差异
二、适用人群与治疗方案:个性化治疗的探索
(一)聚焦高危人群:精准定位治疗对象
1.“三阳性”患者:手术获益的再评估
对于CEA+/CA125+/CA19-9≥1000 U/ml的“三阳性” 患者,以往研究发现其术后半年肿瘤复发率高达90%以上,被视为“手术不获益”人群。然而,新辅助治疗为这部分患者带来了新的希望,通过新辅助治疗可能改善其预后,提高手术治疗的效果,为他们提供了更多的治疗选择。
2.量化高危特征:多因素综合判断
为了更精准地评估患者的高危程度,目前有多种方法被用于量化高危特征。例如,通过肿瘤直径、胰外器官浸润情况、CT报告的淋巴结状态、增强模式及术前血清CA19-9水平等多因素综合评估患者的风险。意大利的一项研究提出了一种简洁的量化方法,即通过肿瘤大小与CA19-9联合量化。研究发现,当肿瘤大小与CA19-9满足特定条件时(如T<2 cm 且 CA19-9<1000;T<3 cm且CA19-9<500;T<4 cm且CA19- 9<150;T<5 cm且CA19-9<50),患者的无病生存期(DFS)和OS 更长,手术无效可能性低于20%(图4)。
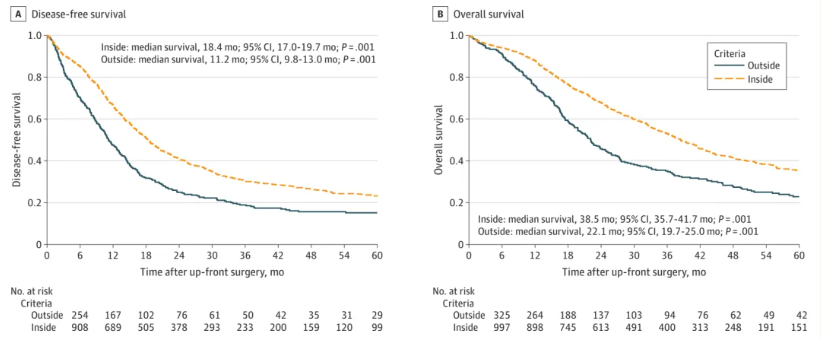
图4. 肿瘤大小与CA19-9联合量化与生存关系
(二)多样化治疗方案:寻求最佳治疗策略
1.化疗主导:多药联合显优势
化疗在非转移性胰腺癌的新辅助/转化治疗中占据重要地位,不同国家和地区的研究提出了多种化疗方案。日本的治疗方案以化疗和化放疗为主,针对不同分期的胰腺癌制定了相应的治疗策略。而在可切除胰腺癌的治疗中,多药新辅助化疗(如mFOLFIRINOX)相较于单药新辅助化疗展现出明显优势。一项研究对比了多药新辅助化疗与单药新辅助化疗及直接手术的效果,结果显示多药新辅助化疗后切除的患者中位OS显著长于直接手术患者(35.8个月 vs. 27.1个月)(图5)。
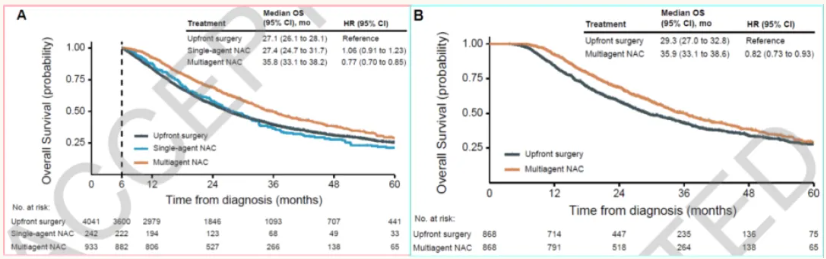
图5. 多药与单药新辅助化疗生存对比
2.化放疗联合:局部控制与生存改善
化放疗在非转移性胰腺癌的治疗中也发挥着重要作用。PREOPANC研究表明,新辅助化放疗用于RPC和交界可切除胰腺癌(BRPC),平均随访59 个月后发现,新辅助化放疗比直接手术显著延长了OS。进一步分层分析显示,新辅助化放疗在交界可切除患者中的地位可能更为重要。此外,对于BRPC患者,全程新辅助治疗(Total neoadjuvant therapy,TNT),即全身化疗后进行化放疗,也显示出一定优势。一项研究比较了TNT、单纯新辅助化放疗(NACRT)和直接手术(UFS)的效果,结果显示TNT治疗后的患者OS和无进展生存率高于NACRT和UFS(图6)。
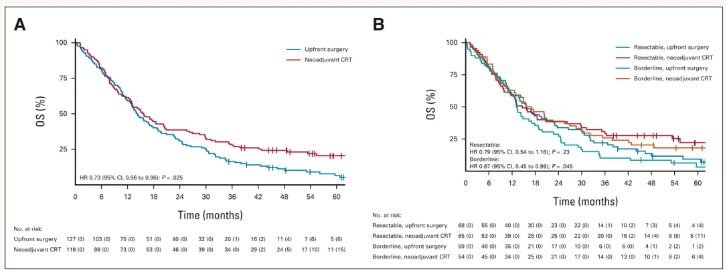
图6. 化放疗与直接手术生存对比
3.疫苗辅助:创新免疫治疗策略
疫苗辅助治疗作为一种新兴的治疗策略,为可切除胰腺癌的治疗带来了新的曙光。个性化RNA疫苗(如autogene cevumeran)与阿替利珠单抗、化疗联合使用,在化疗前为患者定制个性化疫苗。初步研究结果令人鼓舞,在3年随访中,接受疫苗治疗的患者复发率低于未接受疫苗治疗的患者(2/8 vs. 7/8)。目前,后续Ⅱ期临床研究正在积极开展,有望为患者带来更好的治疗效果。此外,DC疫苗在标准治疗(SOC)后使用也显示出一定的疗效。一项研究对38例患者进行了DC疫苗治疗,其中28例患者完成5次治疗,随访25.5个月后,2年无复发生存率(RFS)达64%。可切除胰腺癌的辅助和新辅助治疗处于一种平衡当中。
(三)靶向与免疫治疗:挑战与机遇并存
目前,单纯针对免疫检查点的治疗或联合化、放疗在胰腺癌治疗中的效果并不理想。这可能与胰腺癌中微卫星高度不稳定(MSI-H)、错配修复缺陷(dMMR)、肿瘤突变负荷高(TMB-H)的患者比例较低(不到 2%),属于“冷肿瘤”有关。尽管如此,研究人员仍在不断探索新的联合治疗方案,希望能够克服这些挑战,为胰腺癌患者带来更有效的治疗。
(四)联合治疗探索:综合治疗的潜力
未来,潜在的新辅助/转化治疗联合方案具有很大的探索空间。例如,不同化疗药物组合、化疗与靶向治疗联合、化疗与免疫治疗联合等,这些联合治疗方案有望发挥协同作用,提高治疗效果,为患者提供更多个性化的治疗选择,从而改善非转移性胰腺癌患者的预后。
三、评估与预后因素:优化治疗效果的关键
(一)预后因素研究:明确关键影响因素
1.BRPC和LAPC患者的独立预后因素
针对BRPC和局部进展期胰腺癌(LAPC)患者的研究发现,化疗超过6个周期、手术前CA19-9明显降低、手术后病理学反应达主要缓解(MPR)是独立预后因素。若患者能够满足这三个因素,其生存时间将显著延长;反之,任何一个因素未达到,生存时间均会受到影响。这一研究结果为临床医生在制定治疗方案和评估患者预后时提供了重要的参考依据,有助于更精准地治疗BRPC和LAPC患者。
2.功能影像学与病理学缓解的关联
功能影像学在预测病理学缓解方面具有重要价值。新辅助/转化治疗后,通过FDG-PET检查发现,获得完全代谢缓解(CMR)与MPR密切相关。在一项研究中,对67例患者进行了基线和化疗后代谢(PET)成像检查,结果显示化疗后CMR与MPR高度相关,其阳性和阴性预测值分别为80%和100%。表明FDG-PET检查可作为预测主要病理学缓解的有效手段,为及时调整治疗方案提供了依据。

图7. 胰腺癌病理评估
(二)手术评估方法:多维度评估手术可行性
1.LAPC转化治疗后的手术评估
复发时间界定与预后差异:LAPC转化治疗后,以6个月为界区分早期复发和晚期复发具有重要意义。一项国际多中心研究对168例患者进行了随访,结果显示早期复发患者(52例)的OS明显短于晚期复发和未复发患者(8.4个月 vs. 31.1个月)。这一结果表明,早期复发是影响 LAPC患者预后的重要因素,需要进一步研究其危险因素,以制定更有效的治疗策略。
危险因素分析与评分模型构建:年龄、性别、ypN分期、肿瘤分化程度、术后CA19-9水平及辅助治疗情况等均被确定为早期复发的危险因素(图8)。此外,肿瘤密度、化疗后CA19-9改善情况及肿瘤缩小程度等因素也可构建评分模型预测手术效果和预后。韩国和日本的单中心回顾性研究分别通过肿瘤大小与CA19-9联合、转化手术的严格筛选等方法评估患者预后,为LAPC转化治疗后的手术评估提供了更多的参考依据。
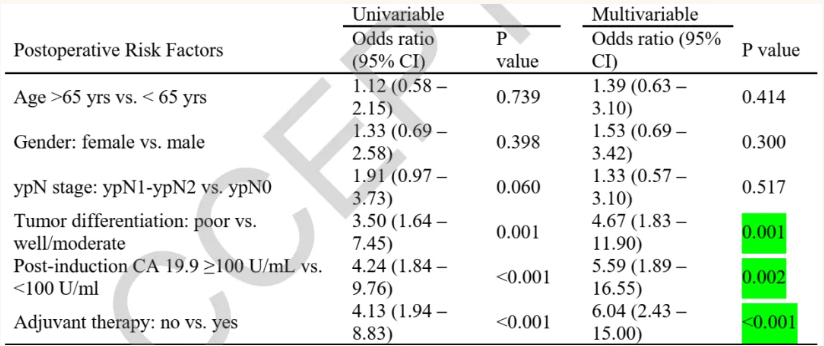
图8. 早期复发的危险因素(肿瘤标志物的生物学评估)
2.不同研究中的手术预后情况
UCSF的数据显示,长程新辅助/转化治疗(如FOLFIRINOX 中位周期达 10)后,可切除、交界可切除和局部进展期胰腺癌患者的预后差别不大,R0切除率为76%,可切除胰腺癌患者的OS可达37个月(图9)。这一结果表明,长程新辅助/转化治疗在不同可切除性状态的胰腺癌患者中均能取得较好的治疗效果,为临床治疗提供了新的思路。
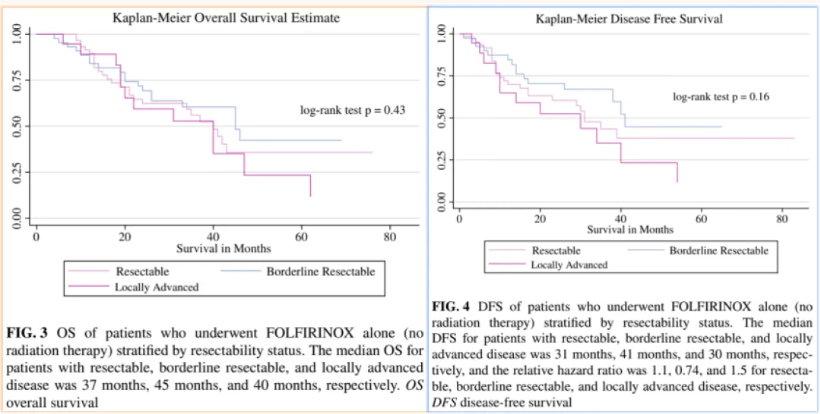
图9. 不同可切除性状态患者生存曲线对比
(三)未来展望:持续创新改善预后
非转移性胰腺癌的新辅助和转化治疗在近年来取得了显著进展。预后评分系统的建立为精准治疗提供了重要依据,多样化的治疗方案为患者带来了更多选择,而评估方法的不断完善有助于优化治疗效果。然而,我们仍面临诸多挑战,如提高化疗有效率、克服靶向和免疫治疗的耐药性等。未来,随着研究的深入和技术的不断进步,有望进一步提高非转移性胰腺癌患者的治疗效果和生存质量,为患者带来更多的生存希望。









