- 首页 > 正文
岂有此“例”丨从三药化疗到钇90放疗:一例乙状结肠癌肝转移患者的MDT全程诊疗启示录
发表时间:2025-03-25 10:34:55
编者按:在晚期结直肠癌肝转移(CRLM)的诊疗中,多学科协作(MDT)模式已成为延长生存、改善生活质量的核心策略。本期《岂有此“例”》所报道的病例来自重庆医科大学附属第一医院结直肠癌MDT团队,由朱婧教授在2025 POST-ASCO GI大会上进行了报告。该病例患者为45岁乙状结肠癌伴肝转移男性,历经三药化疗联合靶向、钇90选择性内放射治疗(SIRT)、外科手术干预等多重治疗波折,在肿瘤进展与并发症中博弈。该案例不仅展现了基因检测指导下的精准治疗决策,更揭示了局部治疗与全身治疗协同的潜在价值,为晚期CRLM的临床实践提供了极具参考意义的范本。

患者基线特征
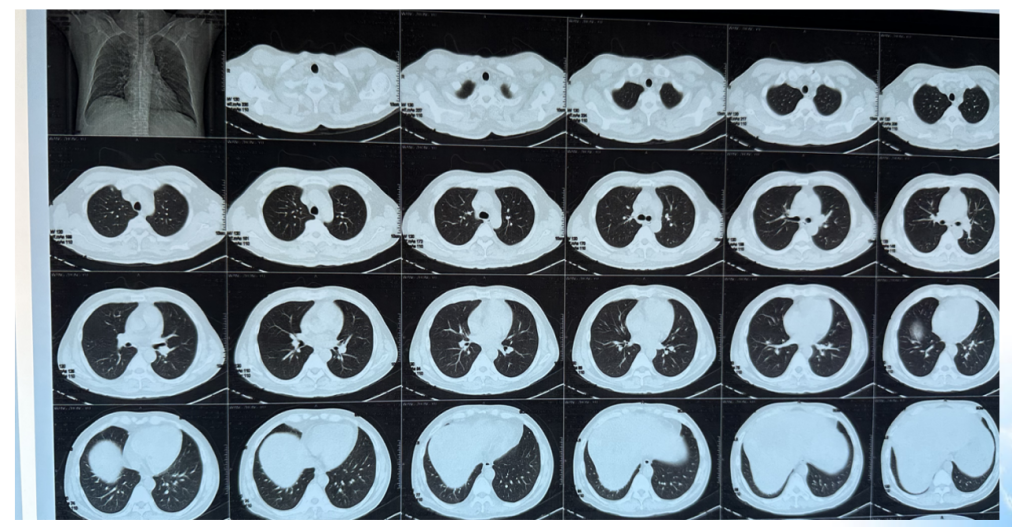
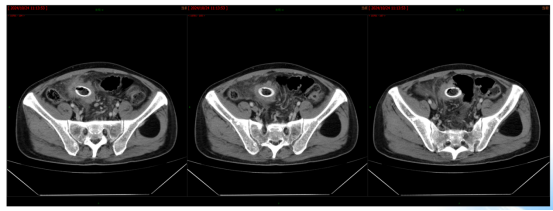
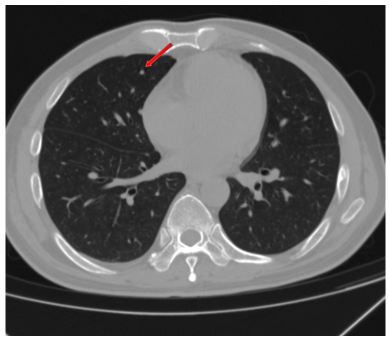
影像学检查:2024年7月30日,院外腹部CT显示乙状结肠管壁增厚,考虑肿瘤性病变(cT3N2,图1),2024年8月5日,肝脏MRI显示肝脏多发转移灶(侵犯门静脉右支、肝右静脉,图2)。2024年8月2日胸部CT显示双肺结节待排(图3)。
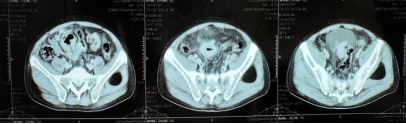
图1. 腹部CT
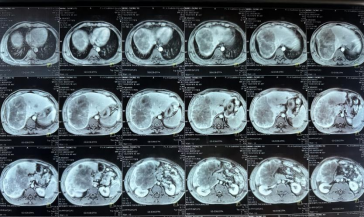
图2. 肝脏MRI
2024年7月31日肠镜检查:距肛门15 cm见环周型粘膜肿块,活检示乙状结肠腺癌。
二、治疗历程:MDT驱动下的动态决策
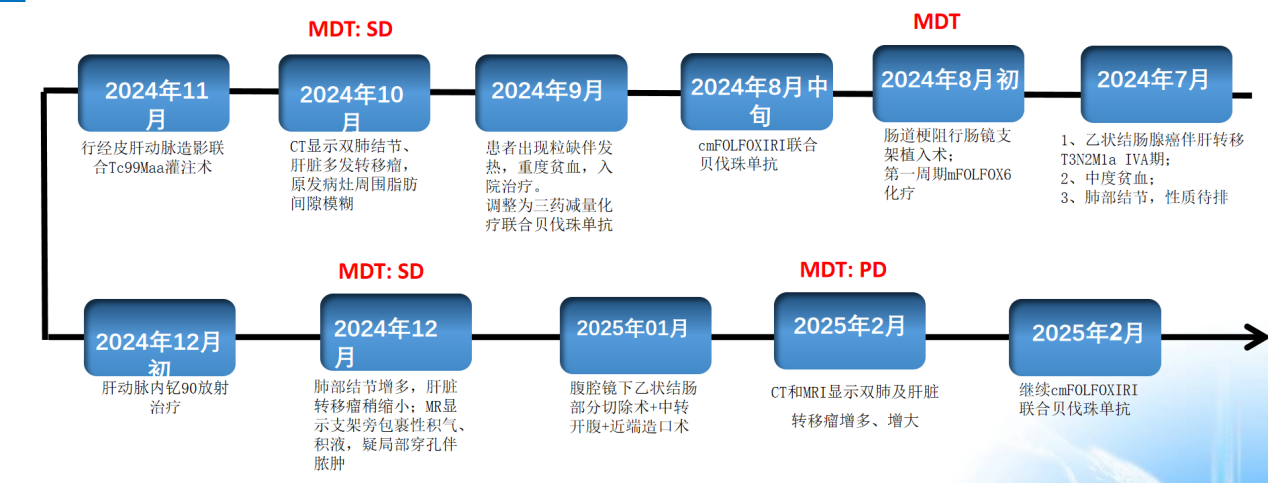
2024年8月5日:第一次MDT
初步诊断:乙状结肠腺癌伴肝转移(cT3N2M1a IVA期);中度贫血;肺部结节,性质待排。
病情评估:基线评估肿瘤负荷大,肝脏多发转移(S2、S4肝脏弥漫性肿块),双肺结节待排。
治疗方案:患者肿瘤负荷大、年轻、体力状况好、期望值高。完善基因检测,选择全身治疗作为一线治疗方案,后续根据疗效评估考虑局部治疗。
治疗目标:姑息治疗为主,目标为延长生存期、控制肿瘤进展、缓解症状、提高生活质量。
治疗实施
2024年8月8日,患者因有肠道梗阻症状进行了肠镜支架植入术(图4)。病检显示结肠中分化腺癌,MLH1(+),MSH2(+),MSH6(+),PMS2(+),Syn(-),CD56(-), her2(0)。
鉴于基因检测结果和患者姑息治疗目标,转至肿瘤科接受FOLFOXIRI联合贝伐珠单抗化疗方案。
2024年8月24日,患者接受了第一周期cmFOLFOXIRI(奥沙利铂+ 伊立替康+5FU/亚叶酸钙)联合贝伐珠单抗的三药治疗。
2024年9月3日血常规显示异常:白细胞总数:0.71×109/L(↓,严重减少);中性粒细胞:0.13×109/L(↓,严重减少);红细胞计数:3.18×1012/L(↓);血红蛋白:55.0 g/L(↓,重度贫血);血小板:127×109/L(正常范围)。患者伴有发热。诊断为粒细胞缺乏伴发热以及重度贫血。予以头孢曲松静脉注射,使用粒细胞集落刺激因子促进白细胞生成;输注红细胞悬液,迅速提升血红蛋白水平,使用重组人促红细胞生成素刺激红细胞生成;密切监测生命体征,维持水电解质平衡。经过上述治疗,患者血常规较前好转,感染得到控制,贫血症状缓解。
考虑患者重度贫血,既往三药化疗患者出现粒缺伴发热,化疗耐受性差,遂于2024年9月10日予以患者三药减量化疗,考虑患者获益比,继续使用贝伐珠单抗。同时,采用长效升白针来预防和治疗粒缺。2024年9月10日至10月24日,予以患者cmFOLFOXIRI+贝伐治疗4周期。
疗效评估
治疗4周期后,肝脏转移灶较基线缩小约20%(图5/6),CEA从532.4 ng/ml降至217.3 ng/ml,CA199从344.2 U/ml降至172.9 U/ml,评估为SD。
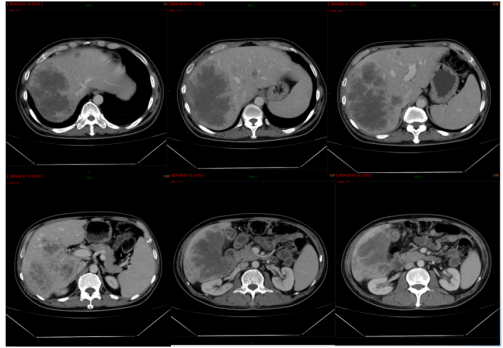
图5. 2024年10月24日CT:肝脏多发转移瘤,较大者位于右半肝,致肝右静脉、门静脉右支受侵
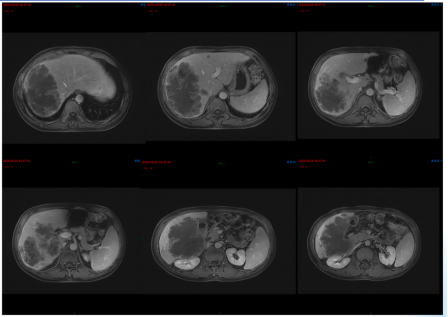
图6. 2024年10月29日MRI:肝脏多发转移瘤,伴有肝右静脉及门静脉右支受侵
2024年11月4日,第二次MDT
目前诊断:乙状结肠腺癌伴肝转移(cT3N2M1a IVA期) NRAS p.Q61L突变,TMB 6.2,MSS;中度贫血;双肺多发结节,转移待排(图7)。
下一步治疗方案:鉴于肝脏转移灶仍显著,MDT团队考虑联合钇90放射治疗(SIRT)以增强局部控制
治疗目标:姑息治疗为主,目标为控制肝脏转移灶、延长无进展生存期、缓解症状。治疗实施
2024年11月8日~22日行cmFOLFOXIRI治疗2周期,停用贝伐珠单抗,为后续治疗准备。
2024年12月3日行肝动脉内钇90放射治疗,术后继续三药化疗联合贝伐珠单抗维持。
在局部治疗后,患者继续接受三药化疗联合贝伐治疗1周期以保持治疗效果。疗效评估
肝脏病灶稍缩小(图8/9),评价为SD。但出现支架旁包裹性积气、积液,提示局部穿孔伴脓肿(图10)。

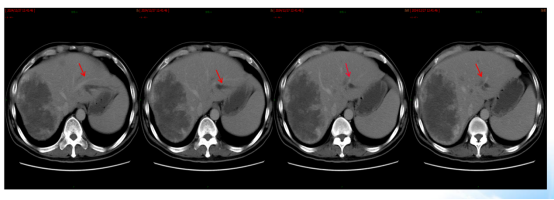
图8. 2024年12月27日CT:肝脏多发转移瘤,伴有肝右静脉及门静脉右支受侵,较2024年10月24日稍缩小
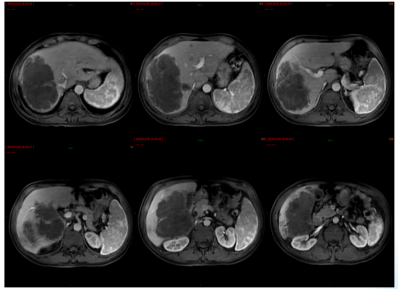
图9. 2024年12月29日MRI:肝脏多发转移瘤,伴有肝右静脉及门静脉右支受侵,较2024年10月24日稍缩小
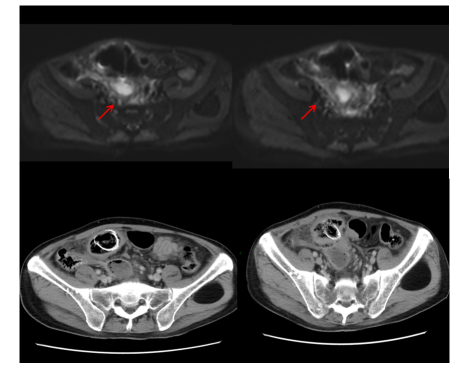
图10. 2024年12月29日MRI:支架旁包裹性积气、积液,考虑局部穿孔伴脓肿形成可能
2024年12月31日,第3次MDT
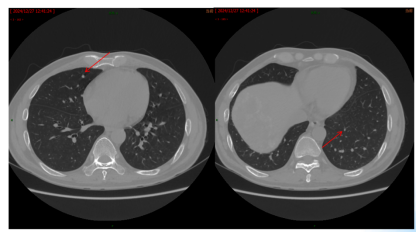
目前诊断:乙状结肠腺癌伴肝转移;肝动脉内钇90放射治疗后;中度贫血;双肺多发结节,转移待排(图12)。
治疗目标:姑息治疗为主,通过控制局部感染,缓解症状,延长生存期。
治疗实施
患者术中探查提示肿瘤周围存在炎性浸润及粘连,解剖层次紊乱(可能与感染/脓肿相关),增加腹腔镜操作难度,故于2025年1月26日气管插管全麻下行腹腔镜下乙状结肠部分切除术+中转开腹+远端封闭+近端造口术。
术中见肿瘤周围组织(右侧腹壁及膀胱壁)呈僵硬、水肿改变,证实为肿瘤侵犯合并慢性炎症;因炎症粘连导致输尿管区域解剖不清,联合泌尿外科评估后标记可疑区域,拟术后必要时放疗覆盖。
术后病理显示(图13),乙状结肠中-低分化腺癌,侵及肠壁全层及肠外脂肪层,见大片坏死伴广泛纤维增生及急慢性炎症细胞浸润,化疗后TRG 2级(AJCC评分标准),未见明确神经及脉管侵犯,肿瘤出芽分级:Bd1级。近、远及放射状切缘未见癌累及。肠周淋巴结未见癌转移(0/21),网膜未见癌组织。Ki67 60%(+),MLH1(+),MSH2(+),MSH6( +),PMS2(+),her2(0)。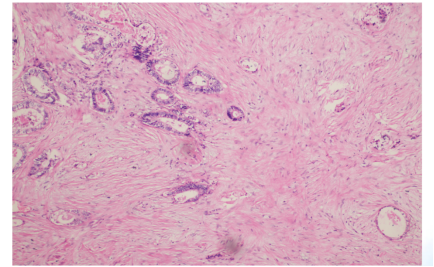
疗效评估
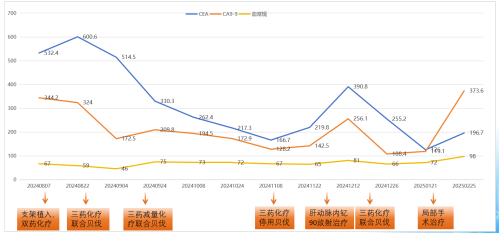
CEA、CA19-9略微升高(图17),肝脏多发转移瘤较前增多、增大(图15/16),双肺结节较前增多、增大(图14),评估为PD。
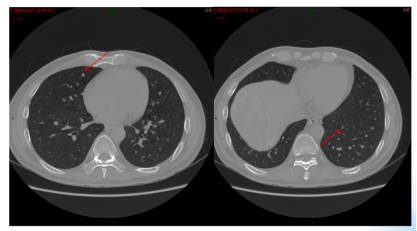
图14. 2025年2月25日CT:双肺结节,较2024年12月27日CT增多、增大
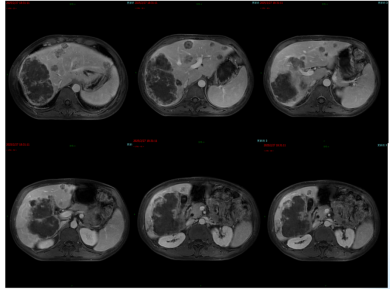
图15. 2025年2月25日MRI:肝脏多发转移瘤,较2024年12月29日MRI增多、增大

图16. 2025年2月25日MRI:术区未见异常强化影
2024年12月31日,第4次MDT
目前诊断:乙状结肠腺癌术后(中-低分化腺癌,TRG 2级,ypT4bN0M1b ⅣB期)伴肝、肺转移;中度贫血。
下一步治疗方案:鉴于既往三药治疗有效,手术间歇期停用全身治疗后肿标升高,则继续FOLFOXIRI联合贝伐珠单抗化疗。治疗目标为姑息性治疗1.针对该患者的后续治疗计划:是否继续FOLFOXIRI联合贝伐珠单抗化疗?是否考虑二线治疗方案(如免疫治疗、靶向治疗)?
2.局部区域治疗的地位与价值:钇90放射治疗(SIRT)等局部治疗手段在不可切除肝转移患者中的疗效如何?如何优化局部治疗与全身治疗的联合应用?
3.MDT优化:如何进一步提高MDT在晚期结直肠癌治疗中的决策效率?如何平衡治疗效果与患者生活质量?
总之,该患者体现了晚期结直肠癌伴肝转移治疗的复杂性和挑战性,通过三药化疗、靶向治疗、局部治疗(钇90放射治疗)及手术的多模式联合治疗,探索了个体化治疗的可能性。尽管患者的肿瘤控制效果有限,但治疗过程中的多学科协作、动态调整治疗方案以及对局部治疗的积极探索,为类似病例提供了临床经验。未来,随着精准治疗和免疫治疗的发展,晚期结直肠癌的治疗将迎来更多突破,为患者带来更多希望。
团队简介

- 推荐文章
