- 首页 > 正文
刘静教授:结直肠癌靶向治疗进展——精准医学时代的突破丨中国医师协会结直肠肿瘤专业委员会年会
发表时间:2025-03-19 09:39:30
编者按随着精准医学的发展,CRC的治疗逐步走向个体化和精准化,尤其是在转移性结直肠癌(mCRC)的治疗中,靶向药物的应用为患者带来了新的希望。近日,中国医科大学附属盛京医院消化肿瘤内科的刘静教授在第九届中国医师协会结直肠肿瘤专业委员会年会上分享了结直肠癌(CRC)靶向治疗的最新进展。

刘静 教授
中国医科大学附属盛京医院
医学博士,主任医师、教授
中国医科大学附属盛京医院消化肿瘤内科 副主任
美国国立癌症研究所(NCI) 、 华盛顿大学医学院Fred Hutchinson Cancer Center访问学者
CSCO青年专家委员会副主任委员、胃癌专家委员会委员、肝癌专家委员会委员、抗肿瘤药物安全管理专家委员会委员
中国抗癌协会肿瘤支持治疗专委会青委会副主任委员、恶性间皮瘤专委会常委、肿瘤靶向治疗专委会委员
中国医疗保健国际交流促进会消化肿瘤综合诊疗学分会常务委员
国家癌症中心结直肠癌质控专家委员会委员
辽宁省预防医学会肿瘤防治专委会副主任委员
辽宁省细胞生物学学会肿瘤多学科协作诊疗和细胞学研究专委会副主任委员
辽宁省免疫学会肿瘤免疫分会常委
CSCO基金会评审专家、《中国医学前沿杂志(电子版)》、《肿瘤综合治疗电子杂志》编委
对于RAS/RAF野生型的mCRC患者,新型EGFR-MET双特异性抗体Amivantamab的应用显示出初步的疗效。2024年ESMO会议上公布的研究(513MO)表明,针对左半和右半结肠癌的不同患者群体,Amivantamab在未暴露过或既往使用过EGFR单抗的患者中均表现出良好的治疗效果,特别是对于KRAS/NRAS/BRAF/EGFR野生型且无HER2扩增的患者,Amivantamab联合化疗在一线或二线治疗中显示出显著的临床获益:ORR 49%;DCR 88%;mDoR 7.4个月;mPFS 7.5个月(图1)。
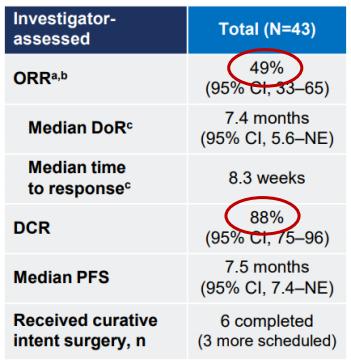
BRAF V600E突变型mCRC的治疗策略从单靶向治疗逐步发展为双靶向和三靶向联合治疗。BEACON研究结果证实,BRAF抑制剂Encorafenib联合EGFR抑制剂西妥昔单抗已成为二线治疗的标准方案,在ORR(客观缓解率)、mPFS(中位无进展生存期)和mOS(中位总生存期)方面均显著优于化疗。在晚期一线治疗中,2025年ASCO GI会议上公布了BREAKWATER研究(16O)的初步疗效数据,Encorafenib +西妥昔单抗+FOLFOX化疗对比标准治疗可显著提高ORR (60.9% vs. 40.0%),OS的期中分析也显示了生存获益趋势。此外,靶向治疗联合免疫治疗(如PD-1抑制剂)在BRAF V600E突变型mCRC中也显示出潜在的生存获益。2022 ASCO GI会议上的研究显示,Encorafenib +西妥昔单抗+纳武利尤单抗(抗PD-1)治疗MSS、BRAF v600e突变型mCRC (NCT04017650,N = 26),ORR 为50%,DCR为 96%, DOR为7.7个月(BACON研究中,ORR为20%);mPFS为7.4个月,mOS为15.1个月,而BACON研究中,mPFS为4个月(图2)。
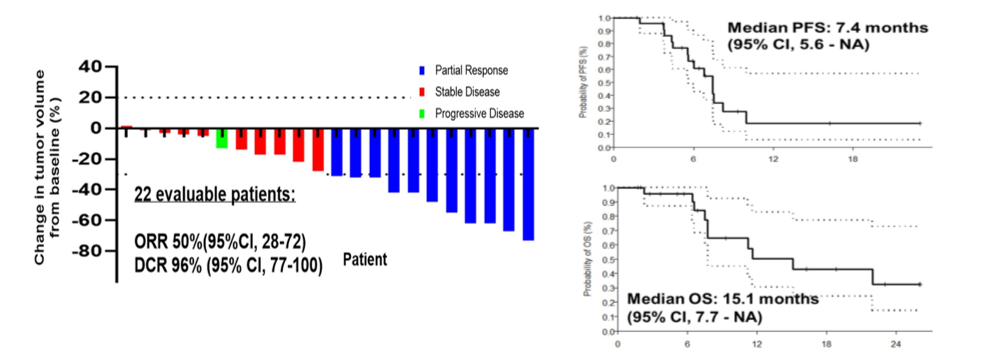
HER2阳性mCRC的治疗也取得了显著进展。DESTINY-CRC02研究是一项多中心、随机、Ⅱ期研究,旨在评估T-DXd(5.4mg/kg和6.4mg/kg)在HER2阳性mCRC患者中的疗效和安全性。研究对象均为中心实验室确认的HER2阳性(IHC3+或IHC2+/ISH+)、RAS野生型或突变型、BRAF野生型且既往接受过标准治疗mCRC患者,允许既往接受过抗HER2治疗。研究结果表明,5.4 mg/kg组和6.4 mg/kg组的中位随访时间分别为8.9个月和10.3个月,5.4 mg/kg组的cORR在数值上高于6.4 mg/kg组,分别为37.8%和27.5%。两组DCR分别为86.6%和85.0%,DoR均为5.5个月。BICR评估的中位PFS分别为5.8个月和5.5个月。中位OS分别为13.4个月和NE(图3)。
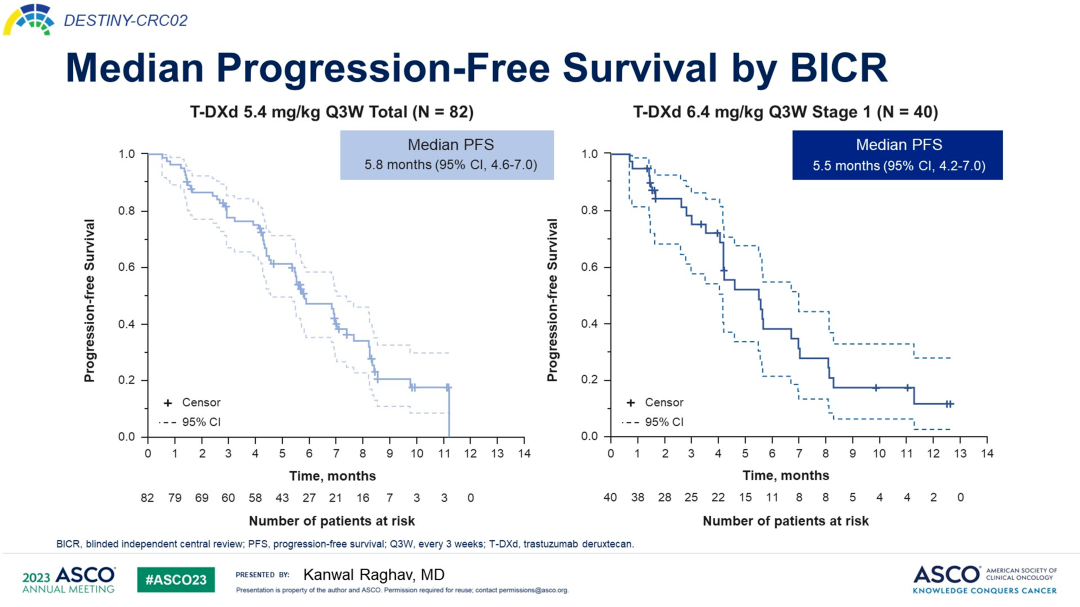
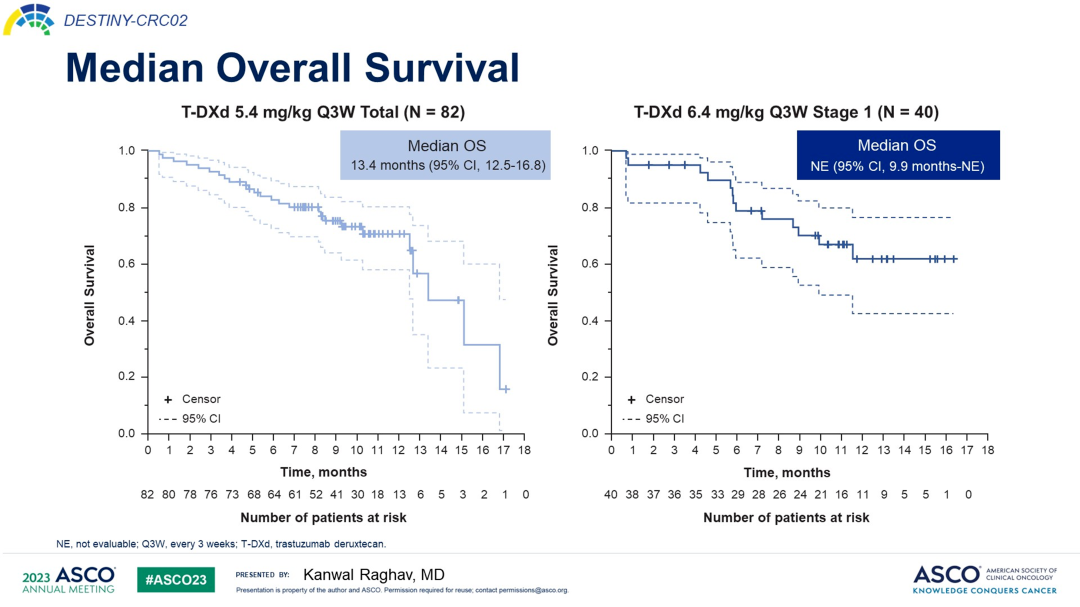
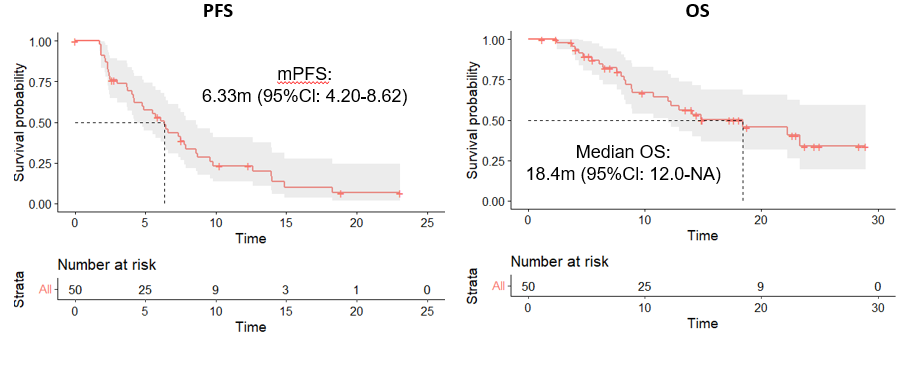
对于无驱动基因突变的mCRC患者,抗血管生成药物联合化疗仍然是标准治疗。2024年ASCO会议上公布的研究(199P)显示,呋喹替尼联合TAS-102在三线治疗中表现出良好的耐受性和临床活性。这是一项开放标签、单臂、多中心、2期研究(NCT05004831),招募了至少两种既往标准治疗方案失败的mCRC患者。研究结果显示,50例患者中46例患者至少有一次肿评:ORR 为10.9%;DCR为73.9%;中位无进展生存期(mPFS)为6.33个月;中位总生存期(mOS)为18.4个月(图4)。
- 推荐文章
