- 首页 > 正文
岂有此“例”丨颠覆认知!C期左肝全累及+门静脉侵犯HCC,手术切除实现6年无复发生存
发表时间:2025-06-25 17:57:00
编者按
肝细胞癌(HCC)仍是全球癌症相关死亡的主要原因之一,尤其在慢性肝炎病毒感染和肝硬化患者中。通常,影像学显示晚期HCC且预后不良特征的患者被认为适合系统治疗而非手术切除。然而,在特定病例中,即使处于疾病晚期阶段,手术切除仍可能为延长生存期提供独特机会。
本期《岂有此“例”》聚焦一例45岁慢性乙型肝炎男性患者,确诊为累及整个左肝并侵犯门静脉左支的晚期HCC,巴塞罗那临床肝癌分期(BCLC)为C期。该患者存在多个不良预后影像学特征,但仍坚持接受左半肝切除,且术后未行辅助治疗,当前已随访6年,患者仍保持无复发状态。本病例凸显了个体化治疗决策的重要性,并揭示了即使对于高风险HCC,外科手术干预仍具有潜在治疗价值。

患者主诉
45岁,男性,慢性乙型肝炎病毒(HBV)感染者,因近几个月出现上腹不适和体重下降前来就诊。
生化检查
肝功能指标处于正常范围(AST 61 U/L,ALT 39 U/L,血清白蛋白39.3 g/L,总胆红素15.06 μmol/L,INR 1.04),肝功能Child-Pugh分级为A级。甲胎蛋白(AFP)水平为6.4 ng/mL,亦在正常范围内。
影像学检查
初始腹部超声检查发现左肝占位性病变,高度怀疑恶性肿瘤。后续多期增强CT显示:左肝被HCC广泛占据,合并左门静脉侵犯,提示肿瘤处于进展期且伴有不良预后指标,以下为具体的影像学表现:
肿瘤大小与部位:影像学显示肝左叶巨大占位,累及Ⅱ、Ⅲ、Ⅳ段。肿瘤最大径约12×10×9 cm,呈膨胀性生长,完全占据肝左叶整个解剖空间(图1)。血管侵犯:肿块可见浸润左门静脉,提示直接血管受累。门静脉的侵犯表现为肿瘤组织在血管腔内延伸并扩张管腔,呈现为充盈缺损伴部分强化。然而,肿瘤未侵犯右门静脉及主门静脉(图1)。瘤内坏死:肿瘤中心区域可见坏死区,表现为团块内的非强化区域。在增强成像中,坏死组织呈低密度影,提示该处肿瘤组织发生变性(图1)。
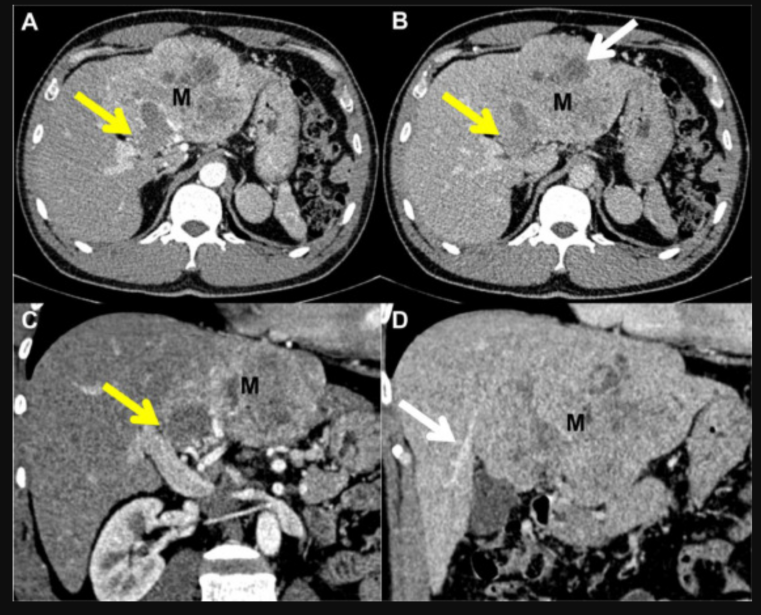
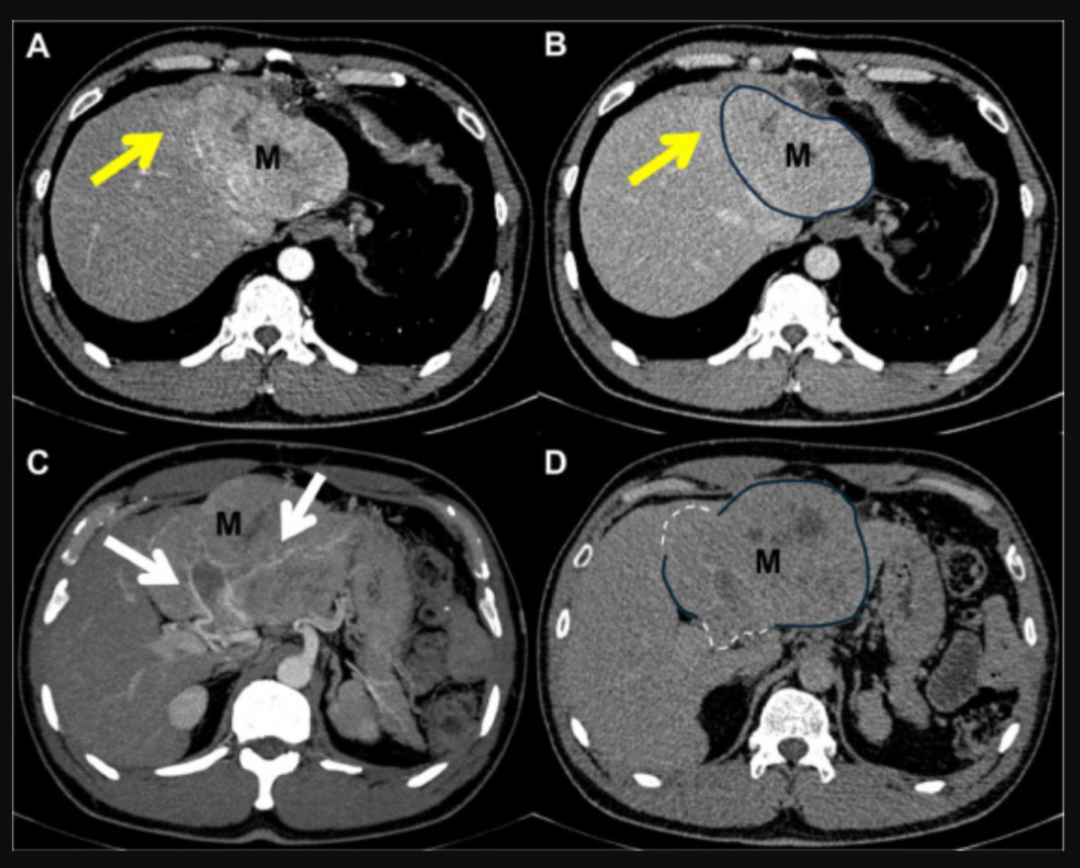
图2. 轴向增强CT扫描显示了额外的预后影像特征
治疗方案
尽管影像学提示预后不良,患者仍强烈倾向于接受外科手术治疗。经过多学科讨论,决定行左肝切除术,未进行术后辅助治疗。患者手术耐受良好,术后无并发症。切除肝脏的组织病理学检查证实为中分化肝细胞癌,伴血管侵犯,切缘阴性(图3)。
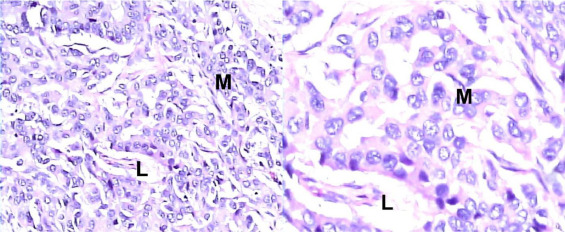
图3. 术后病理检查显示符合中分化HCC特征
随访
术后患者接受密切监测并随访6年,期间影像学检查均未见肿瘤残留或复发迹象。术后1.5年进行的增强CT扫描证实左半肝切除术后无残留病灶(图4)。通过定期腹部超声及AFP监测随访,结果始终稳定且正常。
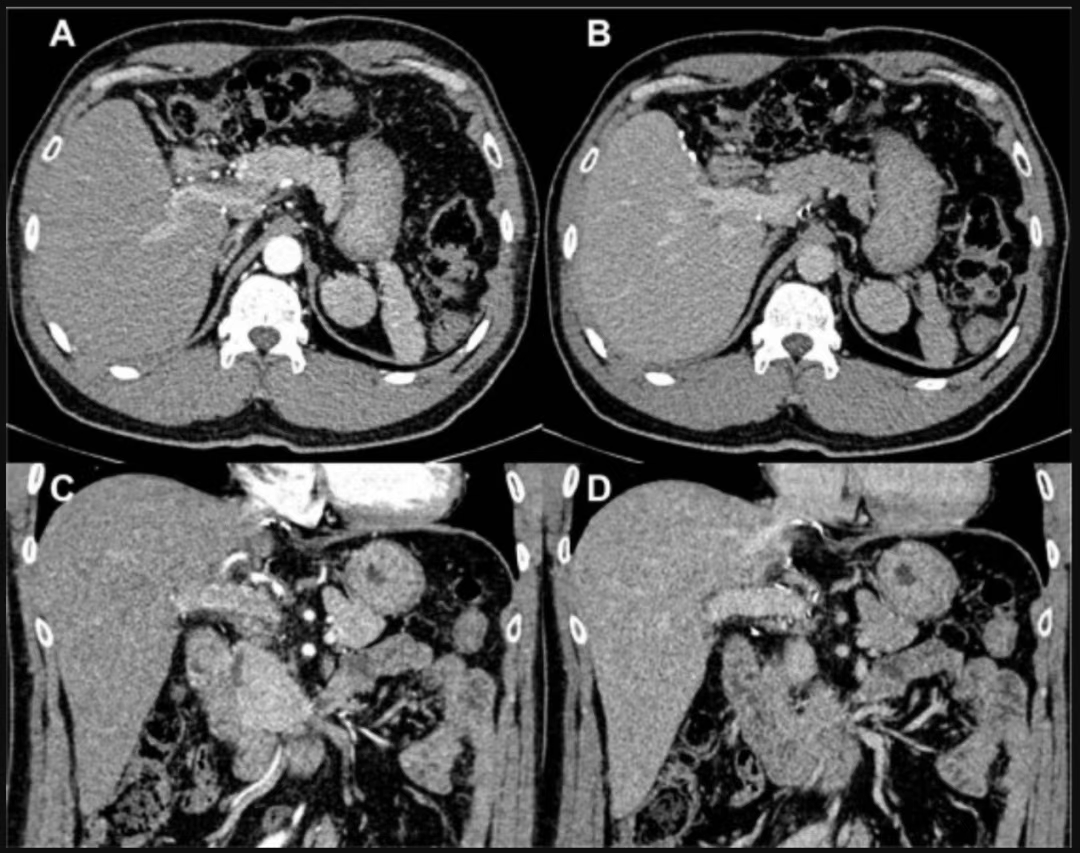
图4. 术后1.5年行增强CT扫描证实左肝切除术后无残留病灶病例
总结与思考
晚期HCC的标准治疗,尤其是存在门静脉侵犯和不良影像学预后特征的病例,通常倾向于非手术方案。手术切除一般仅适用于病灶局限、肝功能保留且侵袭程度较低的患者。然而,本病例尽管存在多个影像学不良预后指标(这些指标提示高复发率和较差的总生存期),仍按照患者意愿进行了手术治疗,而未按常规指南治疗。
1.影像学特征的预后意义
近期多项研究表明,特定影像学标志物可作为HCC术后早期复发的预测指标,其中许多特征在本病例中均有体现。这些发现提示该病例为具有高度侵袭性生物学行为和不良预后的晚期HCC。
(1)肿瘤体积较大。肿瘤大小是HCC预后的关键因素。由于较大肿瘤更易发生血管侵犯、肝内播散且难以完全切除,通常与较差的预后相关。体积较大的HCC往往提示肿瘤负荷较高,并与术后早期复发风险增加相关。本病例中,肿瘤占据了整个左肝叶,显著增加了肝内和肝外转移的风险。(2)肿瘤侵犯门静脉。门静脉侵犯通常被视为手术切除的主要禁忌证,因其与全身播散和不良预后密切相关。门静脉受累提示血管结构受损,可能促进肝内播散和复发。研究表明,门静脉侵犯患者的生存率显著降低,因其提示肿瘤处于进展期且存在较高的微血管转移风险。(3)晕征增强。晕征增强常见于高血管性HCC,与肿瘤早期静脉引流相关。这一现象可作为微观肿瘤向周围肝实质浸润扩散的替代标志物。该特征的存在通常意味着术后早期复发风险增加,因为术前影像学检查可能无法检测到微转移病灶。(4)包膜不完整。完整纤维包膜的缺失提示结构完整性丧失,使得肿瘤呈现浸润性生长模式。在HCC中,包膜不完整与较差的预后相关。这种结构缺陷削弱了可能限制恶性细胞扩散的"屏障"作用,从而增加了复发的可能性。(5)肿瘤内部坏死。肿瘤内部坏死区域通常由肿瘤快速生长超过其血液供应所致,导致肿瘤内部细胞死亡。坏死提示高级别恶性肿瘤,常伴随侵袭性行为及较差预后,因其多见于增殖指数较高的肿瘤。(6)肿瘤内动脉。肿瘤内存在多条动脉是高血供的标志,反映肿瘤动脉供血丰富。此特征常见于体积更大、侵袭性更强的肿瘤,并增加肿瘤内出血风险。此外,高血供通常与血管生成增加相关,后者是促进更侵袭性扩散和复发潜能的因素。(7)边界不规则。不规则的浸润性肿瘤边界是HCC复发率更高的特征。此类不规则轮廓提示侵袭性生长模式,常与微血管侵犯风险升高及肿瘤超出肉眼可见范围扩散相关,进一步增加手术切除难度及术后残留病灶风险。
此外,其他通常与HCC不良预后相关但在本病例中未出现的影像学特征包括边缘强化(LI-RADS M类)和卫星结节。边缘强化的特征是动脉期病灶周围出现环形强化带,通常与HCC低分化及预后更差的亚型相关。然而本病例术后病理显示为常规亚型的中分化HCC,术前影像呈现典型的HCC强化模式(LI-RADS 5类)。卫星结节表现为邻近主灶的微小瘤灶,提示存在微血管侵犯,因多灶性病变特征而具有更高的早期复发风险。尽管本例肿瘤呈单发大肿块表现,但可能存在CT无法检出的微小结节,因为CT对卫星结节的检测敏感度有限。
2.手术决策与结果
尽管存在高风险特征(如血管侵犯和多项不良预后指标),但患者相对年轻且具有根治性手术意愿,同时基线肝功能良好且肿瘤标志物水平正常。本病例凸显了个体化治疗的重要性——患者的偏好、年龄及身体状况在决策过程中起关键作用。无早期复发的优异结果显示,在特定病例中,即使对于伴有血管侵犯和不良预后指标的进展期HCC,积极手术切除仍可能带来获益。
3.文献与临床启示
目前针对BCLC分期C期HCC的手术切除仍存争议,但近期文献表明,部分肝功能良好且肝外转移极少的患者可能通过手术获得生存获益。本病例为此提供了新证据:即使影像学特征提示疾病进展,经谨慎评估后仍可考虑手术切Ⅱ除。报告强调,仍需进一步研究以更精确界定晚期HCC患者的手术适应证标准。
总之,本病例报告展示了一例罕见病例——一例年轻男性晚期HCC患者,影像学特征显示多项不良预后指标,但在接受左肝切除术后实现了无病生存。尽管存在不利的影像学特征,但该患者已保持无复发状态长达6年,突显了手术干预在特定晚期HCC病例中的潜在价值。这一病例为晚期HCC手术治疗作用的持续讨论提供了新的依据,并强调了在特定的病例中可能获得良好预后的可能性。
参考文献:[1] Le HDM, Vo DT, Do HT, Le HNG, Phan CC, Nguyen DT, Le QND. Hepatectomy in a young patient with advanced hepatocellular carcinoma and poor prognostic imaging features: A case of recurrence-free survival. Radiol Case Rep. 2025 Mar 15;20(6):2704-2709.?
- 推荐文章
