- 首页 > 正文
JCO:RESET-C结果公布,单周期帕博利珠单抗新辅助治疗dMMR结肠癌pCR率达44%
发表时间:2026-05-12 19:32:46
编者按
免疫检查点抑制剂(ICIs)新辅助治疗是错配修复缺陷型(dMMR)结直肠癌(CRC)治疗领域的一项重大进展。尽管dMMR直肠癌凭借新辅助免疫治疗的高临床完全缓解(cCR)率,成功推动了“观察等待”策略的实施,但在结肠癌中,器官保留策略的推广仍举步维艰。其核心瓶颈之一在于缺乏精准的cCR评估手段。此外,延长疗程或多药联合免疫方案可获得高缓解率,但短程单周期方案有望在疗效、安全性及卫生经济学之间实现更优平衡。
如何在保障疗效的前提下实现“降级治疗”?RESET-C试验对此给出了创新性解答,该研究系统评估了单周期帕博利珠单抗新辅助治疗局限性dMMR结肠癌的疗效与安全性。近期,该研究结果正式发表于Journal of Clinical Oncology。本文将深入解读这一关键研究,探讨其对于优化dMMR结肠癌治疗范式的启示。

研究设计
RESET-C是一项丹麦全国性、研究者发起的Ⅱ期多中心临床试验,共纳入85例局限性dMMR结肠癌患者。入组患者接受单周期帕博利珠单抗治疗(4 mg/kg,最大剂量400 mg,采用每6周给药方案),并于术前接受内镜检查及活检,随后在3~5周后按计划行根治性手术。其中1例患者拒绝手术。
入组标准:患者年龄≥18岁,经组织学确诊为局限性dMMR结肠癌,临床分期为cT1N0M0~cT4N2M0(Ⅰ~Ⅲ期),具有择期根治性手术指征且未接受新辅助化疗,同时无免疫治疗禁忌证。
研究终点:主要终点为病理完全缓解(pCR)率。次要终点包括:(1)安全性;(2)术后并发症;(3)主要病理缓解(MPR)率;(4)总生存期(OS);以及(5)无病生存期(DFS)。此外,研究还探讨了内镜图像、治疗后活检、循环肿瘤DNA(ctDNA)与病理缓解之间的关联。
研究结果
患者基线特征:入组患者以女性为主(72%),60%为国际抗癌联盟(UICC)临床Ⅲ期,中位年龄74岁(IQR,68~79)。手术方式方面,绝大多数患者(74/84)接受了右半结肠切除术,其中23例为扩大右半结肠切除术;5例行左半结肠切除术(含2例扩大手术);其余病例中,3例行乙状结肠切除术,1例行横结肠切除术,1例同时接受了结肠切除及回肠切除术。术后重建方面,共有80例患者实施了消化道吻合术。
疗效结局
在符合方案集(PP)分析中,84例患者中有37例达到pCR,pCR率为44%(95%CI:33%~55%,图1);MPR率为57%(48/84,95%CI:46%~68%)。5例患者表现为免疫治疗无缓解。
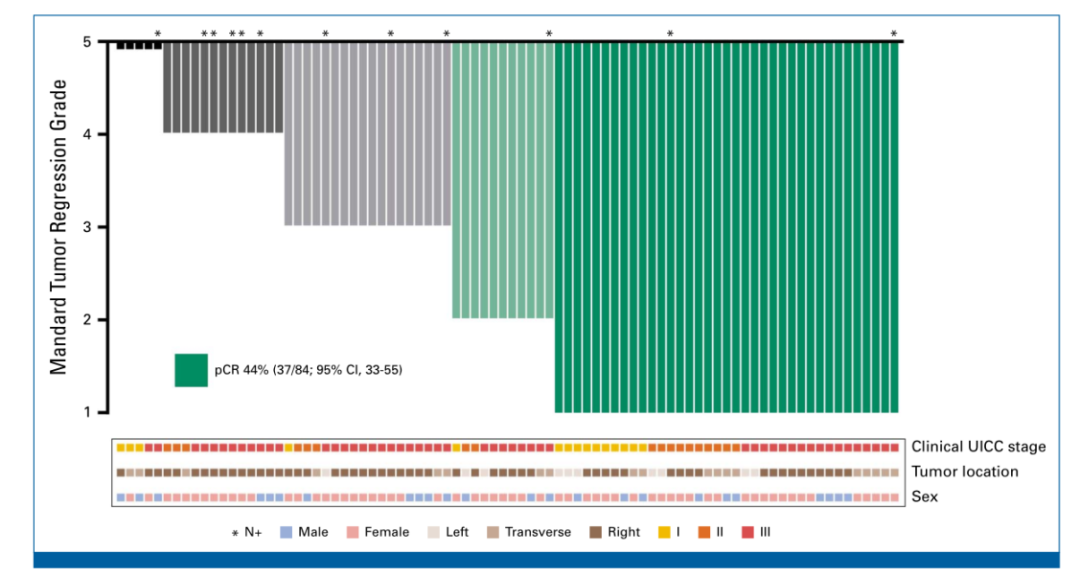
图1. 肿瘤缓解与患者特征的瀑布图
意向性治疗(ITT)人群的pCR:85例患者中有37例达到pCR,pCR率为44%(95%CI:33%~55%)。按临床分期分层的pCR率显示:Ⅰ期、Ⅱ期、Ⅲ期患者的pCR率分别为67%(10/15,95%CI:38%~88%)、56%(10/18,95%CI:31%~78%)和33%(17/51,95%CI:21%~48%)。Ⅰ期与Ⅱ期患者的pCR率无统计学差异(P=0.72);但早期(Ⅰ~Ⅱ期)与晚期(Ⅲ期)患者的pCR率存在显著分期相关性:早期患者pCR率为61%(20/33),显著高于Ⅲ期的33%(17/51)(P=0.02)。校正年龄、性别、体能状态及治疗间隔后,Ⅰ~Ⅱ期患者的pCR率仍高于Ⅲ期患者(比值比[OR]=3.1,95%CI:1.2~8.1,P=0.02)。各亚组的pCR率分布详见图2。
按临床分期分层的MPR率显示:Ⅰ期、Ⅱ期、Ⅲ期患者的MPR率分别为73%(11/15,95%CI:45%~92%)、67%(12/18,95%CI:41%~87%)和49%(25/51,95%CI:35%~63%)。Ⅰ~Ⅱ期(23/33)与Ⅲ期(25/51)患者的MPR率未达到统计学显著差异(70% vs. 49%,P=0.07)。
手术结局:82例患者实现R0切除(98%,95%CI:92%~100%),2例为R1切除。12例患者的切除标本证实淋巴结阳性,中位阳性淋巴结数为1.5枚(IQR:1~2)。其中,2例淋巴结阳性患者(均为单枚淋巴结转移)同时达到pCR。总体而言,42%的参与者(35/84,95%CI:31%~53%)实现了“pCR且淋巴结阴性”的双重病理缓解。
辅助治疗:3例淋巴结阳性患者接受了辅助化疗(卡培他滨联合奥沙利铂),9例淋巴结阳性患者未接受辅助化疗。
随访结果:至数据截止日期(2025年4月1日),85例患者的中位随访时间为18.4个月(IQR:16.3~21.1)。随访期间,76例(89%)患者完成了术后1年标准胸腹部CT复查。意向性治疗(ITT)分析显示:OS为98%(83/85,95%CI:92%~100%);2例患者(80岁、81岁,临床分期ⅢB/ⅢC期)术后30天内死于手术相关并发症。DFS为96%(80/85,95%CI:90%~99%),即绝大多数患者无复发存活。1例cT3N0M0期、TRG2缓解的患者,在入组后13个月(乙状结肠切除术后11个月)出现降结肠异时性肿瘤,经全结肠切除术处理后病情控制。
安全性结局
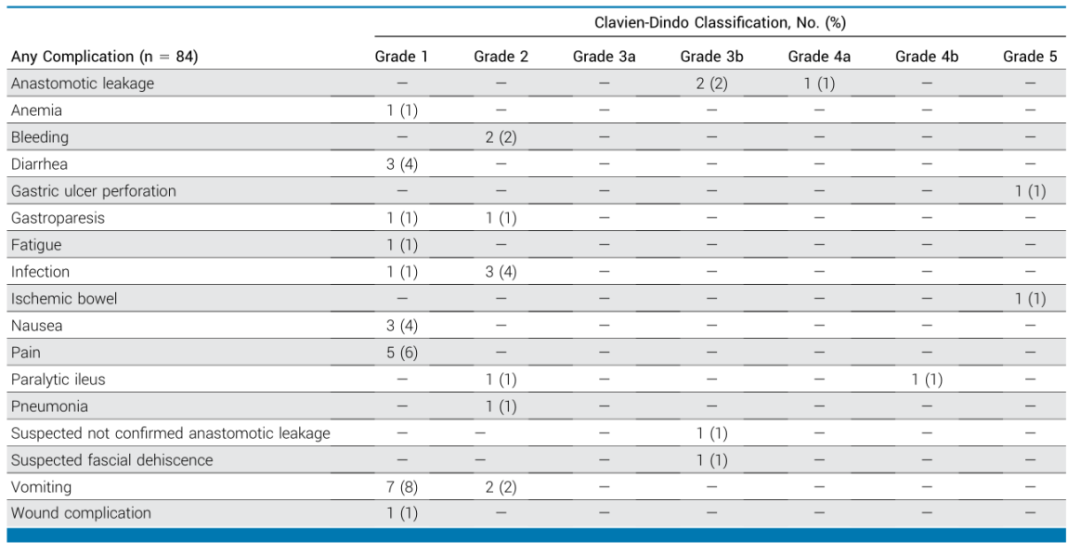
治疗间隔的中位数为32天(IQR:30~34天)。在84例患者中,31例(37%,95%CI:27%~48%)共发生了41起手术并发症(表1)。其中,8例患者(10%,95%CI:4%~18%)出现了8起Clavien-Dindo分级≥3b级的严重并发症。术后住院时间(LOS)的中位数为4天(IQR:3~6天),共有4例患者(4.8%)在出院后发生再入院。
表1. 手术并发症
85例患者中,70例(82%[95%CI,73%~90%])发生了至少1种任何级别的不良事件(AE),其中9例(11%[95%CI,5%~19%])报告了17起3级AE,未观察到4级或5级AE;共报告5起与治疗相关的严重不良事件(SAE),具体为3级肝炎、3级结肠炎、3级无症状丙氨酸氨基转移酶升高、2级肾上腺功能不全及1级无症状肌炎/心肌炎各1例,上述5起SAE中有4例接受了糖皮质激素治疗。
研究结论
RESET-C研究证实了单周期4 mg/kg(每6周给药一次)新辅助帕博利珠单抗在局限性dMMR结肠癌患者中的疗效与安全性。该方案诱导了显著的肿瘤退缩,且病理缓解呈现出明显的分期依赖性梯度,同时验证了内镜反应评估作为制定适应性治疗策略工具的可行性。
讨论
RESET-C研究结果显著推进了局限性dMMR结肠癌新辅助免疫治疗范式的发展,并为该领域提供了超越既往里程碑研究的新见解。尽管本研究的pCR率低于双药联合方案,但其提供了一种更为实用且潜在毒性更低的替代策略。在比较不同研究的疗效与安全性时,需充分考虑研究人群的差异及真实世界代表性;例如,本研究患者中位年龄为74岁,显著高于其他大型研究(分别为57岁和60岁)。NICHE-2研究显示,双药免疫检查点抑制剂(纳武利尤单抗联合伊匹木单抗)方案的pCR率达68%且安全性良好;IMHOTEP试验则证实帕博利珠单抗单药在dMMR人群中亦可获得较高的临床及病理缓解率。然而,这两项研究主要侧重于验证治疗的可行性与早期疗效,而RESET-C研究则旨在将免疫治疗精简为单周期方案,以优化临床转化路径。通过将治疗限制为单周期(根据体重调整),本研究降低了双药或延长治疗方案带来的医疗后勤负担及经济成本,这对因合并症无法耐受强化治疗的患者尤为重要,同时也强调了在Ⅰ~Ⅱ期疾病中,需在获取成熟的DFS和OS数据后,方可确立适应性治疗策略的应用价值——毕竟对于大多数Ⅰ~Ⅱ期患者而言,单纯手术即可实现治愈。
RESET-C研究的安全性数据为进一步探索特定患者的非手术治疗策略提供了支撑。尽管11%的患者发生了3级AE,但仅3例(占发生AE患者的三分之一)被判定为治疗相关,其安全性特征显著优于手术相关的发病与死亡风险。在本研究队列中,手术并发症发生率较高,且包含2例术后30天内死亡病例,这与该年龄段人群的全国手术数据趋势一致。上述结果凸显了开展dMMR结肠癌“观察等待”策略临床试验的迫切性。未来研究应优先纳入手术或复发风险较高的患者群体,并构建整合临床风险模型与复发生物标志物的个体化治疗路径。
参考文献:
Gögenur I, et al. J Clin Oncol. 2026 May 5:JCO2502274.
免疫检查点抑制剂(ICIs)新辅助治疗是错配修复缺陷型(dMMR)结直肠癌(CRC)治疗领域的一项重大进展。尽管dMMR直肠癌凭借新辅助免疫治疗的高临床完全缓解(cCR)率,成功推动了“观察等待”策略的实施,但在结肠癌中,器官保留策略的推广仍举步维艰。其核心瓶颈之一在于缺乏精准的cCR评估手段。此外,延长疗程或多药联合免疫方案可获得高缓解率,但短程单周期方案有望在疗效、安全性及卫生经济学之间实现更优平衡。
如何在保障疗效的前提下实现“降级治疗”?RESET-C试验对此给出了创新性解答,该研究系统评估了单周期帕博利珠单抗新辅助治疗局限性dMMR结肠癌的疗效与安全性。近期,该研究结果正式发表于Journal of Clinical Oncology。本文将深入解读这一关键研究,探讨其对于优化dMMR结肠癌治疗范式的启示。

研究设计
RESET-C是一项丹麦全国性、研究者发起的Ⅱ期多中心临床试验,共纳入85例局限性dMMR结肠癌患者。入组患者接受单周期帕博利珠单抗治疗(4 mg/kg,最大剂量400 mg,采用每6周给药方案),并于术前接受内镜检查及活检,随后在3~5周后按计划行根治性手术。其中1例患者拒绝手术。
入组标准:患者年龄≥18岁,经组织学确诊为局限性dMMR结肠癌,临床分期为cT1N0M0~cT4N2M0(Ⅰ~Ⅲ期),具有择期根治性手术指征且未接受新辅助化疗,同时无免疫治疗禁忌证。
研究终点:主要终点为病理完全缓解(pCR)率。次要终点包括:(1)安全性;(2)术后并发症;(3)主要病理缓解(MPR)率;(4)总生存期(OS);以及(5)无病生存期(DFS)。此外,研究还探讨了内镜图像、治疗后活检、循环肿瘤DNA(ctDNA)与病理缓解之间的关联。
研究结果
患者基线特征:入组患者以女性为主(72%),60%为国际抗癌联盟(UICC)临床Ⅲ期,中位年龄74岁(IQR,68~79)。手术方式方面,绝大多数患者(74/84)接受了右半结肠切除术,其中23例为扩大右半结肠切除术;5例行左半结肠切除术(含2例扩大手术);其余病例中,3例行乙状结肠切除术,1例行横结肠切除术,1例同时接受了结肠切除及回肠切除术。术后重建方面,共有80例患者实施了消化道吻合术。
疗效结局
在符合方案集(PP)分析中,84例患者中有37例达到pCR,pCR率为44%(95%CI:33%~55%,图1);MPR率为57%(48/84,95%CI:46%~68%)。5例患者表现为免疫治疗无缓解。

图1. 肿瘤缓解与患者特征的瀑布图
意向性治疗(ITT)人群的pCR:85例患者中有37例达到pCR,pCR率为44%(95%CI:33%~55%)。按临床分期分层的pCR率显示:Ⅰ期、Ⅱ期、Ⅲ期患者的pCR率分别为67%(10/15,95%CI:38%~88%)、56%(10/18,95%CI:31%~78%)和33%(17/51,95%CI:21%~48%)。Ⅰ期与Ⅱ期患者的pCR率无统计学差异(P=0.72);但早期(Ⅰ~Ⅱ期)与晚期(Ⅲ期)患者的pCR率存在显著分期相关性:早期患者pCR率为61%(20/33),显著高于Ⅲ期的33%(17/51)(P=0.02)。校正年龄、性别、体能状态及治疗间隔后,Ⅰ~Ⅱ期患者的pCR率仍高于Ⅲ期患者(比值比[OR]=3.1,95%CI:1.2~8.1,P=0.02)。各亚组的pCR率分布详见图2。
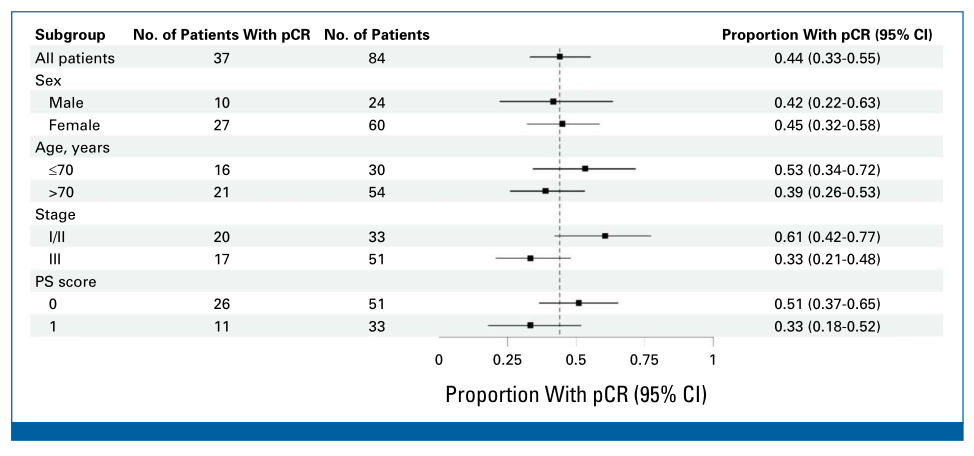
按临床分期分层的MPR率显示:Ⅰ期、Ⅱ期、Ⅲ期患者的MPR率分别为73%(11/15,95%CI:45%~92%)、67%(12/18,95%CI:41%~87%)和49%(25/51,95%CI:35%~63%)。Ⅰ~Ⅱ期(23/33)与Ⅲ期(25/51)患者的MPR率未达到统计学显著差异(70% vs. 49%,P=0.07)。
手术结局:82例患者实现R0切除(98%,95%CI:92%~100%),2例为R1切除。12例患者的切除标本证实淋巴结阳性,中位阳性淋巴结数为1.5枚(IQR:1~2)。其中,2例淋巴结阳性患者(均为单枚淋巴结转移)同时达到pCR。总体而言,42%的参与者(35/84,95%CI:31%~53%)实现了“pCR且淋巴结阴性”的双重病理缓解。
辅助治疗:3例淋巴结阳性患者接受了辅助化疗(卡培他滨联合奥沙利铂),9例淋巴结阳性患者未接受辅助化疗。
随访结果:至数据截止日期(2025年4月1日),85例患者的中位随访时间为18.4个月(IQR:16.3~21.1)。随访期间,76例(89%)患者完成了术后1年标准胸腹部CT复查。意向性治疗(ITT)分析显示:OS为98%(83/85,95%CI:92%~100%);2例患者(80岁、81岁,临床分期ⅢB/ⅢC期)术后30天内死于手术相关并发症。DFS为96%(80/85,95%CI:90%~99%),即绝大多数患者无复发存活。1例cT3N0M0期、TRG2缓解的患者,在入组后13个月(乙状结肠切除术后11个月)出现降结肠异时性肿瘤,经全结肠切除术处理后病情控制。
安全性结局
治疗间隔的中位数为32天(IQR:30~34天)。在84例患者中,31例(37%,95%CI:27%~48%)共发生了41起手术并发症(表1)。其中,8例患者(10%,95%CI:4%~18%)出现了8起Clavien-Dindo分级≥3b级的严重并发症。术后住院时间(LOS)的中位数为4天(IQR:3~6天),共有4例患者(4.8%)在出院后发生再入院。
表1. 手术并发症

85例患者中,70例(82%[95%CI,73%~90%])发生了至少1种任何级别的不良事件(AE),其中9例(11%[95%CI,5%~19%])报告了17起3级AE,未观察到4级或5级AE;共报告5起与治疗相关的严重不良事件(SAE),具体为3级肝炎、3级结肠炎、3级无症状丙氨酸氨基转移酶升高、2级肾上腺功能不全及1级无症状肌炎/心肌炎各1例,上述5起SAE中有4例接受了糖皮质激素治疗。
研究结论
RESET-C研究证实了单周期4 mg/kg(每6周给药一次)新辅助帕博利珠单抗在局限性dMMR结肠癌患者中的疗效与安全性。该方案诱导了显著的肿瘤退缩,且病理缓解呈现出明显的分期依赖性梯度,同时验证了内镜反应评估作为制定适应性治疗策略工具的可行性。
讨论
RESET-C研究结果显著推进了局限性dMMR结肠癌新辅助免疫治疗范式的发展,并为该领域提供了超越既往里程碑研究的新见解。尽管本研究的pCR率低于双药联合方案,但其提供了一种更为实用且潜在毒性更低的替代策略。在比较不同研究的疗效与安全性时,需充分考虑研究人群的差异及真实世界代表性;例如,本研究患者中位年龄为74岁,显著高于其他大型研究(分别为57岁和60岁)。NICHE-2研究显示,双药免疫检查点抑制剂(纳武利尤单抗联合伊匹木单抗)方案的pCR率达68%且安全性良好;IMHOTEP试验则证实帕博利珠单抗单药在dMMR人群中亦可获得较高的临床及病理缓解率。然而,这两项研究主要侧重于验证治疗的可行性与早期疗效,而RESET-C研究则旨在将免疫治疗精简为单周期方案,以优化临床转化路径。通过将治疗限制为单周期(根据体重调整),本研究降低了双药或延长治疗方案带来的医疗后勤负担及经济成本,这对因合并症无法耐受强化治疗的患者尤为重要,同时也强调了在Ⅰ~Ⅱ期疾病中,需在获取成熟的DFS和OS数据后,方可确立适应性治疗策略的应用价值——毕竟对于大多数Ⅰ~Ⅱ期患者而言,单纯手术即可实现治愈。
RESET-C研究的安全性数据为进一步探索特定患者的非手术治疗策略提供了支撑。尽管11%的患者发生了3级AE,但仅3例(占发生AE患者的三分之一)被判定为治疗相关,其安全性特征显著优于手术相关的发病与死亡风险。在本研究队列中,手术并发症发生率较高,且包含2例术后30天内死亡病例,这与该年龄段人群的全国手术数据趋势一致。上述结果凸显了开展dMMR结肠癌“观察等待”策略临床试验的迫切性。未来研究应优先纳入手术或复发风险较高的患者群体,并构建整合临床风险模型与复发生物标志物的个体化治疗路径。
参考文献:
Gögenur I, et al. J Clin Oncol. 2026 May 5:JCO2502274.
- 推荐文章
JCO:RESET-C结果公布,单周期帕博利珠单抗新辅助治疗dMMR结肠癌pCR率达44%
NordICC研究13年随访结局登顶《柳叶刀》:结肠镜检查可降低CRC发病率,死亡率获益仍未体现
全程新辅助化疗联合信迪利单抗与IL-2治疗MSS/pMMR型局部晚期直肠癌,无放疗方案pCR率高达42.4%!
国际视角丨知名肿瘤专家解析:靶向DLL4/VEGF-A双特异性抗体CTX-009为胆道恶性肿瘤患者二线治疗带来新希望
呋喹替尼联合TAS-102±SBRT治疗转移性结直肠癌,中位PFS达8.58个月,三联方案ORR高达36.4%!
心灵驿站丨当手术刀指向自己:一位医学生从旁观者到亲历者的心灵蜕变
奥美拉唑肠溶胶囊
枯草杆菌二联活菌颗粒
整蛋白型肠内营养剂
硫糖铝口服混悬液
JCO丨徐瑞华、周志伟、袁庶强团队为胃癌围手术期免疫治疗长期生存获益再添新证据!
“瘤瘤”新知丨警惕!心理痛苦是结直肠癌幸存者生活质量的“头号杀手”,自我效能感成最强“护心盾”
埃万妥单抗单药治疗化疗难治性RAS/BRAF野生型mCRC展现持久抗肿瘤活性,疗效不受原发肿瘤部位及既往抗EGFR治疗史影响!
杨春康教授专访:结直肠外科视角下的腹膜后肿瘤解剖逻辑与入路选择
帕博利珠单抗新辅助治疗MSI/dMMR型结直肠癌患者pCR率高达53%!增加治疗周期可进一步显著提高pCR率
腹膜后肿瘤大会秘书长肖萌萌副主任医师专访:解读会议创新亮点,展望学科发展方向
放疗在腹膜后肿瘤治疗中扮演何种角色?从临床定位到技术突破
第九届全国腹膜后肿瘤大会丨杨盈赤教授专访:多学科协同,开启腹膜后肿瘤诊疗新时代
岂有此“例”|GIST的长期潜伏:一例辅助治疗不足却获超长无病生存期的罕见病例分析
2026 CSCO指南会丨李印教授:新版CSCO食管癌诊疗指南更新要点与落地思考
转移性胃癌精准治疗:从化疗基石到新型疗法的演进与挑战
第九届全国腹膜后肿瘤大会|罗成华教授专访:深耕腹膜后肿瘤专科化建设,共启学科新征程
2026 CSCO指南会丨胰腺癌诊疗指南更新要点,一文速览!
2026 CSCO指南会丨黄镜教授:聚焦分层与突破,新版CSCO食管癌诊疗指南引领治疗迈向精准个体化新征程
2026 CSCO指南会丨胃癌诊疗更新要点,一文梳理
2026 CSCO指南会丨结直肠癌诊疗更新要点,一文梳理
2026 CSCO指南会丨原发性肝癌诊疗指南更新要点,一文速览!
精准融合,创新共赢:王桂华教授剖析胃癌免疫治疗前沿,共绘胃癌治疗新蓝图丨2026北京胃肠肿瘤学术会议
“瘤瘤”新知丨阿司匹林真的能预防结直肠癌吗?超12万人数据显示,普通人群风险明确而获益遥远
立足精准,突破耐药:杨合利教授畅谈胃癌抗HER2治疗进展与临床实践丨2026北京胃肠肿瘤学术会议
2026 ASCO摘要标题公布!消化系统肿瘤领域中国入选重磅研究抢先一览
武爱文教授深度解析:结直肠癌新辅助治疗后器官保留的筛选策略、实施挑战与未来方向丨2026北京胃肠肿瘤学术会议
中位OS高达19.4个月!CD73抑制剂Quemliclustat联合化疗为转移性胰腺癌 一线治疗带来新希望
春满京华,群贤毕至——2026北京胃肠肿瘤学术会议圆满召开!
第九届腹膜后肿瘤大会在京成功召开——开启腹膜后肿瘤专科发展新时代
JCO丨习勉教授团队探索局部晚期食管鳞癌免疫“前置”新策略:诱导化免联合同步放化免显著改善患者生存,免疫维持未添额外获益
中国Ⅱ期研究:TAS-102联合伊立替康与贝伐珠单抗为mCRC后线治疗提供可行性新选择
岂有此“例”丨肝细胞癌血清标志物新证据:AKR1B10联合检测提升AFP阴性患者诊疗效能
大型队列研究证实:基于f-Hb的CRC精准监测策略可减少近10%结肠镜检查需求
nature medicine丨POLAR研究显示,HRD突变胰腺癌患者可从PARPi+免疫联合维持治疗中获益
赢在整合,向生命而行——一场关于生命守护的行动在星城拉开序幕
一项基于18万例数据的倾向评分匹配分析揭秘:早发性 vs. 晚发性结肠癌的预后真相
会议通知丨2026北京胃肠肿瘤学术会议即将召开
会议通知丨第九届腹膜后肿瘤大会即将召开
“瘤瘤”新知丨一夜好眠有多重要?研究发现存在中重度睡眠障碍的结直肠癌患者死亡风险增加46%,这些人群尤其要当心!
系统综述与荟萃分析揭示,PD-L1阳性胃癌中MSI与EBV阳性的预后意义
突破!恩沃利单抗联合卡培他滨和仑伐替尼为术后具有高危复发因素的胆道恶性肿瘤患者辅助治疗带来新希望
NEJM丨KRAS G12D蛋白降解剂Setidegrasib首次人体研究公布,晚期胰腺癌患者ORR达24%
中国智慧,世界回响:沈琳教授团队领衔实现关键突破,为晚期胃癌一线治疗注入“中国力量”
T1期结直肠癌ESD术后:低危者预后较好,高危者补充手术价值存疑
nature medicine丨ILUSTRO研究为CLDN18.2阳性胃癌一线“靶向+免疫+化疗”策略提供新依据
岂有此“例”丨一例胰腺来源的罕见GIST揭示腹腔镜在肿瘤定位中的决定性价值
JAMA丨ORCHESTRA研究解读:肿瘤减瘤术联合化疗未改善多器官转移性结直肠癌生存期
NEJM重磅丨ATOMIC研究结果公布:免疫联合化疗有望成为dMMR Ⅲ期结肠癌辅助治疗新策略
研究显示:诊断延迟>5个月、治疗延迟>2个月与局部晚期直肠癌不良预后显著相关
