- 首页 > 正文
Lancet Oncol | 晚期食管癌一线治疗新突破:双免联合化疗ORR近70%!
发表时间:2026-03-04 15:43:12
T细胞免疫球蛋白和免疫受体酪氨酸抑制基序结构域(TIGIT)是一种抑制性免疫检查点受体,在多种免疫细胞上高度表达,与PD-1共表达并协同抑制T细胞功能。Tiragolumab是一种全人源抗TIGIT单克隆抗体。早期研究提示,其联合PD-L1抑制剂阿替利珠单抗在晚期实体瘤中显示出可控的安全性和初步疗效。MORPHEUS-EC研究旨在初治的局部晚期不可切除或转移性食管癌患者中,评估Tiragolumab联合阿替利珠单抗及化疗对比标准治疗(化疗联合或不联合阿替利珠单抗)的疗效与安全性。该研究结果近期发表于The Lancet Oncology杂志。本文旨在对该研究的关键数据进行梳理和评述,从而为临床实践提供信息参考。

研究介绍
MORPHEUS-EC是一项开放标签、多中心、随机的Ⅰb/Ⅱ期伞式研究,在中国台湾、韩国、澳大利亚、以色列、英国和美国的20个中心进行。符合条件的患者年龄≥18岁,患有既往未接受过治疗的局部晚期不可切除或转移性食管癌,且美国东部肿瘤协作组体能状态评分(ECOG PS)为0~1分。符合条件的患者最初被分配至某个联合治疗组或对照组(第1阶段);临床获益有限或发生不可耐受毒性的患者可在符合方案条件的情况下改用不同方案继续治疗(第2阶段)。本次报告MORPHEUS-EC第1阶段的数据,第2阶段数据将另行报告。
符合条件的患者被随机分配至以下三个预设治疗组之一:接受Tiragolumab(600 mg,每21天静脉注射一次)联合阿替利珠单抗(1200 mg,每21天静脉注射一次)和化疗(顺铂80 mg/m²,每21天静脉注射一次,并在每个21天周期的第1~5天静脉注射氟尿嘧啶800 mg/m²,每24小时一次);接受阿替利珠单抗联合化疗;仅接受化疗。
研究的主要终点是经确认的客观缓解率(ORR),关键次要终点包括研究者评估的疾病控制率(DCR)、研究者评估的经确认的缓解持续时间(DoR)、研究者评估的无进展生存期(PFS)和总生存期(OS)。
研究结果
2020年6月5日至2022年11月8日期间,共有152例患者被随机分配至Tiragolumab联合阿替利珠单抗和化疗组(n=63)、阿替利珠单抗联合化疗组(n=65)或单纯化疗组(n=24)。Tiragolumab+阿替利珠单抗+化疗组的中位随访时间为10.9个月(IQR=7.1~17.3),阿替利珠单抗+化疗组为11.4个月(IQR=7.9~14.7),单独化疗组为8.7个月(IQR=3.9~12.0)。
主要终点结果
在疗效可评估人群(150名患者)中,Tiragolumab+阿替利珠单抗+化疗组研究者评估的确认ORR为67.7%(42/62,95%CI:54.7~79.1),阿替利珠单抗+化疗组ORR为53.8%(35/65,95%CI:41.0~66.3),单纯化疗组ORR为47.8%(11/23,95%CI:26.8~69.4)(表1)。
表1. 在疗效可评估人群中,研究者评估的抗肿瘤活性
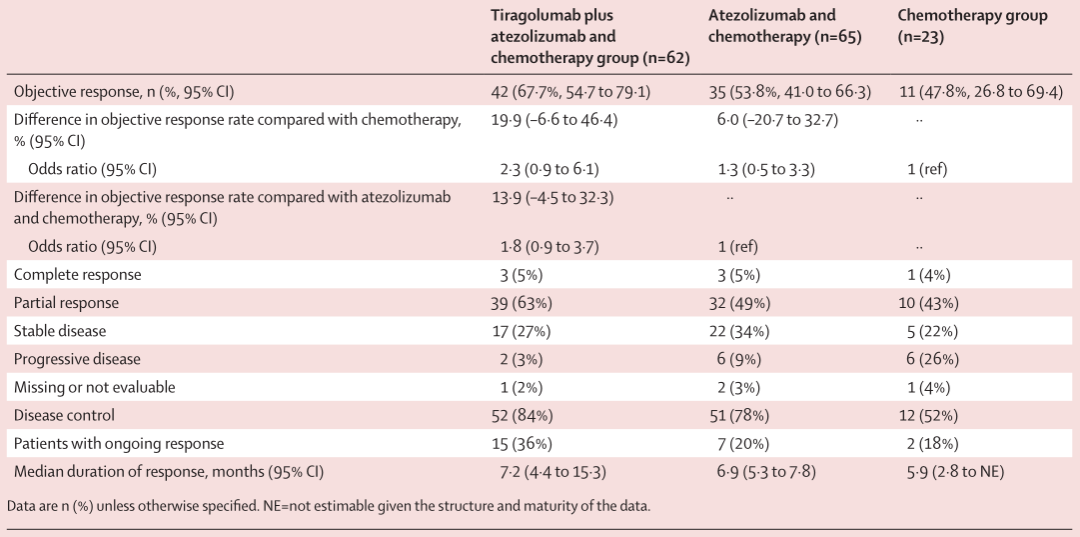
Tiragolumab+阿替利珠单抗+化疗组中位DoR为7.2个月(95%CI:4.4~15.3),阿替利珠单抗+化疗组为6.9个月(95%CI:5.3~7.8),单纯化疗组为5.9个月(95%CI:2.8~不可估计)(图1)。
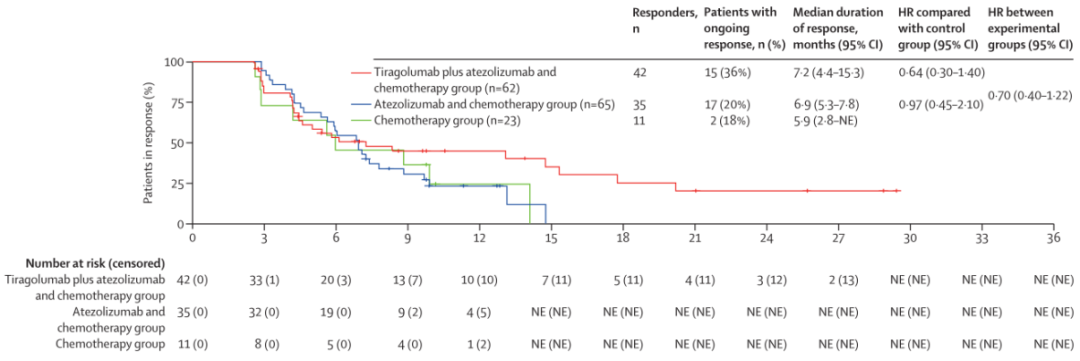
图1. 在疗效可评估人群中,研究者根据实体瘤疗效评价标准1.1版评估的DoR
至数据截止日期,Tiragolumab+阿替利珠单抗+化疗组的62名患者中有43名(69%)、阿替利珠单抗+化疗组的65名患者中有56名(86%)以及单独化疗组的23名患者中有19名(83%)发生了无进展生存事件。Tiragolumab+阿替利珠单抗+化疗组的中位PFS为6.9个月(95%CI:6.0~9.9),阿替利珠单抗+化疗组为6.8个月(95%CI:5.6~8.3),单独化疗组为4.1个月(95%CI:2.7~7.6)(图2)。
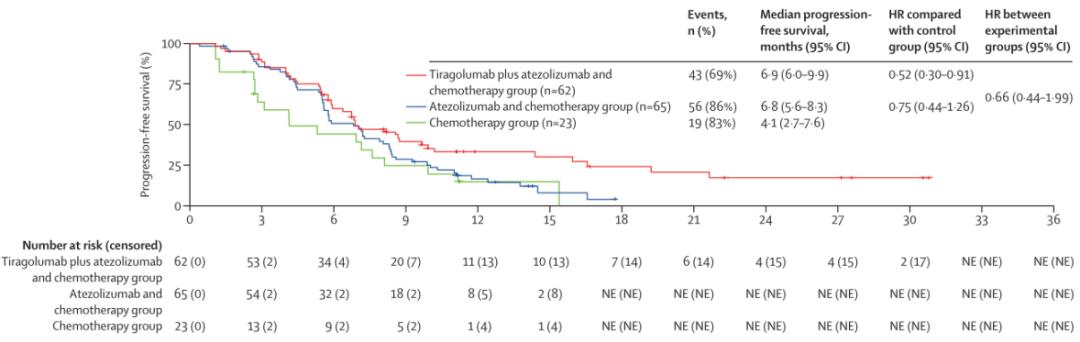
图2. 在疗效可评估人群中,研究者评估的PFS
Tiragolumab+阿替利珠单抗+化疗组的62名患者中有31名(50%)、阿替利珠单抗+化疗组的65名患者中有36名(55%)以及单独化疗组的23名患者中有15名(65%)发生了总生存事件。Tiragolumab+阿替利珠单抗+化疗组的中位OS为16.0个月(95%CI:11.3~21.7),阿替利珠单抗+化疗组为13.1个月(95%CI:12.2~16.3),单独化疗组为9.9个月(95%CI:7.6~23.2)(图3)。Tiragolumab+阿替利珠单抗+化疗组的6个月和12个月OS率分别为88.6%(95%CI:80.6~96.6)和62.7%(95%CI:49.6~75.9),阿替利珠单抗+化疗组分别为87.5%(95%CI:79.4~95.6)和63.0%(95%CI:50.6~75.5),单纯化疗组分别为77.8%(95%CI:60.5~95.0)和33.3%(95%CI:12.8~53.9)。
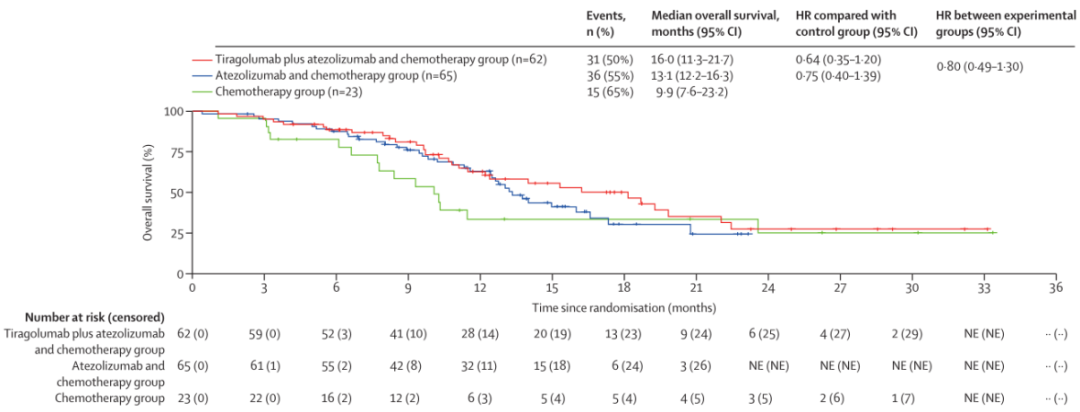
图3. 在疗效可评估人群中,研究者评估的OS
安全性方面,Tiragolumab+阿替利珠单抗+化疗组、阿替利珠单抗+化疗组和单纯化疗组分别有49例(79%)、52例(80%)和17例(74%)患者发生3~4级不良事件,分别有36例(58%)、33例(51%)和11例(48%)患者发生严重不良事件。最常见的治疗相关不良事件是恶心和食欲下降。无治疗相关死亡事件。
研究讨论与结论
在这项随机Ⅰb/Ⅱ期临床试验中,针对既往未经治疗的局部晚期不可切除或转移性食管癌患者,Tiragolumab联合阿替利珠单抗及化疗方案取得了67.7%(95%CI:54.7~79.1)的ORR;而阿替利珠单抗联合化疗组为53.8%(95%CI:41.0~66.3),单纯化疗组为47.8%(95%CI:26.8~69.4)。与单纯化疗相比,该三联方案表现出PFS获益,但与阿替利珠单抗联合化疗相比,其差异未达到统计学显著性。Kaplan-Meier生存曲线显示,Tiragolumab+阿替利珠单抗+化疗组的总生存曲线在约3个月时与单纯化疗组分离,并在12个月时与阿替利珠单抗联合化疗组分离。然而,至临床数据截止日期,各组总生存随访时间较短且不均衡,同时化疗组中有13例患者后续接受了Tiragolumab联合阿替利珠单抗治疗。因此,有必要通过更长时间的随访进一步分析总生存数据,以获得更可靠的结论。
安全性分析显示,Tiragolumab+阿替利珠单抗+化疗组与阿替利珠单抗+化疗组的3~4级治疗相关不良事件发生率相近,且两个含免疫治疗方案组中均未发生治疗相关死亡事件。此外,绝大多数特别关注的不良事件为免疫介导性且严重程度多为1~2级,与既往研究报告的安全性特征一致。总体而言,该联合方案的不良事件可控,Tiragolumab联合阿替利珠单抗及化疗的安全性可接受。
MORPHEUS-EC Ⅰb/Ⅱ期研究结果表明,与单纯化疗或阿替利珠单抗联合化疗相比,Tiragolumab联合阿替利珠单抗及化疗在ORR与PFS方面均显示出具有临床意义的改善。这些初步发现进一步拓展了抗TIGIT免疫联合疗法在食管癌治疗领域的认识,提示通过同时抑制TIGIT与PD-L1这两个免疫检查点,可增强初治不可切除食管癌患者对PD-L1抑制剂为基础的治疗反应。此外,与双联疗法(阿替利珠单抗+化疗)相比,三联疗法(Tiragolumab+阿替利珠单抗+化疗)在治疗相关不良事件及特别关注免疫介导不良事件的发生率方面相似,且未出现新的安全性信号。以上结果为后续在SKYSCRAPER-08 Ⅲ期研究中进一步评估TIGIT与PD-L1双免疫检查点抑制剂联合化疗用于食管癌患者提供了支持。
综上,与含或不含阿替利珠单抗的化疗方案相比,Tiragolumab联合阿替利珠单抗及化疗在抗肿瘤疗效方面表现出显著改善。该结果表明,在阿替利珠单抗联合化疗的基础上加用Tiragolumab,可为既往未经治疗的局部晚期不可切除或转移性食管癌患者带来额外临床获益。
参考文献:
[1]Sun JM, et al Lancet Oncol. 2026 Jan;27(1):90-102.- 推荐文章
