- 首页 > 正文
国际视角丨KRAS G12C突变结直肠癌最新进展:联合疗法开启治疗新纪元
发表时间:2026-01-25 17:26:33
编者按
在结直肠癌的治疗领域,KRAS G12C突变犹如一座难以攻克的“堡垒”,长期以来给患者和医疗界带来了巨大挑战。传统单一疗法在应对这种复杂突变时,往往效果有限,难以满足患者对更有效、更持久治疗方案的迫切需求。然而,医学的进步从未停止脚步。近年来,针对KRAS G12C突变型结直肠癌的联合疗法正逐渐崭露头角,为这一困境带来了新的曙光。联合疗法通过整合多种治疗手段的优势,从不同角度对癌细胞发起攻击,有望突破单一疗法的瓶颈,显著提升治疗效果,延长患者的生存期,并改善其生活质量。
近日,Dr. Muhammet Ozer、Dr. Amy Little Jones、Dr. Timothy J. Brown在ASCO每日新闻深入探讨了KRAS G12C突变型结直肠癌联合疗法的最新研究进展,详细介绍了不同联合策略的原理、临床试验结果以及潜在的应用前景。希望通过这篇文章,能让广大医疗工作者、科研人员以及患者和家属对这一前沿治疗领域有更全面、深入的了解,共同期待联合疗法为KRAS G12C突变型结直肠癌患者带来更多的生存希望和更好的生活未来。同时,也期待更多的科研力量能够投入到这一领域,加速联合疗法的研发与应用,推动结直肠癌治疗迈向新的高度。
KRAS G12C突变型结直肠癌现状
KRAS G12C突变存在于约3%~4%的转移性结直肠癌(mCRC)病例中。作为mCRC的一个独特分子亚群,该种类型肿瘤通常对化疗具有耐药性,且对表皮生长因子受体(EGFR)靶向治疗的反应不佳。而共价KRAS G12C抑制剂,如索托拉西布(sotorasib)和阿达格拉西布(adagrasib),为治疗效果不佳的患者提供了新的治疗方法。当前,索托拉西布和阿达格拉西布在非小细胞肺癌中已显示出临床获益,并已获美国食品药品监督管理局(FDA)批准用于二线及后续治疗。然而,索托拉西布单药治疗mCRC的临床疗效一般,主要原因是存在适应性耐药机制,如EGFR信号的反馈性重新激活。因此,随着治疗格局的演变,涉及KRAS G12C抑制剂的联合治疗方案正逐渐兴起,为这种传统上难治的癌症亚型患者带来了希望。
阿达格拉西布和索托拉西布在结直肠癌中的应用
Ⅰ/Ⅱ期KRYSTAL-1试验评估了阿达格拉西布单药治疗及与西妥昔单抗联合治疗的效果。阿达格拉西布单药治疗的客观缓解率(ORR)为19%,中位无进展生存期(PFS)为5.6个月。阿达格拉西布与西妥昔单抗联合治疗显著提高ORR至46%,PFS至6.9个月。联合治疗常见的治疗相关不良事件(TRAEs)包括腹泻、恶心、呕吐、疲劳、痤疮样皮炎和骨髓抑制,约30%的患者观察到≥3级不良事件。
与此同时,Ⅰb期CodeBreaK-101试验评估了索托拉西布、帕尼单抗和FOLFIRI方案联合治疗KRAS G12C突变且未接受过KRAS G12C抑制剂治疗的mCRC患者的效果。在2025年ASCO年会上,报告了40例既往接受过中位2种全身治疗方案治疗的患者的长期疗效结果。研究报告显示,ORR为57.5%,疾病控制率(DCR)为92.5%,中位PFS为8.2个月,经过近30个月的随访,中位总生存期(OS)为17.9个月(详细结果及其他2025年会议摘要中的显著结果见表1)。常见的TRAEs包括痤疮样皮炎、中性粒细胞减少和口腔炎,50%的患者出现可管理的≥3级毒性。值得注意的是,索托拉西布和帕尼单抗的停药率较低(各为2.5%),表明总体耐受性良好,尽管化疗相关停药率仍较高,为40%。此外,左侧肿瘤患者以及在病程早期使用该方案治疗的患者,其总生存期明显更长。这些结果支持将KRAS G12C靶向治疗扩展至双重阻断之外,并强化了靶向治疗联合化疗的作用。
CodeBreaK-300试验证实了这些发现,该试验评估了索托拉西布与帕尼单抗联合治疗的效果。联合治疗在既往接受过治疗的KRAS G12C突变mCRC患者中显示出优于化疗的疗效,突出了双重通路抑制的益处。正在进行的Ⅲ期CodeBreaK-301试验(NCT06252649)将在一线治疗环境中进一步评估这种联合治疗方案,比较索托拉西布联合帕尼单抗与KRAS G12C突变mCRC患者的标准护理化疗。
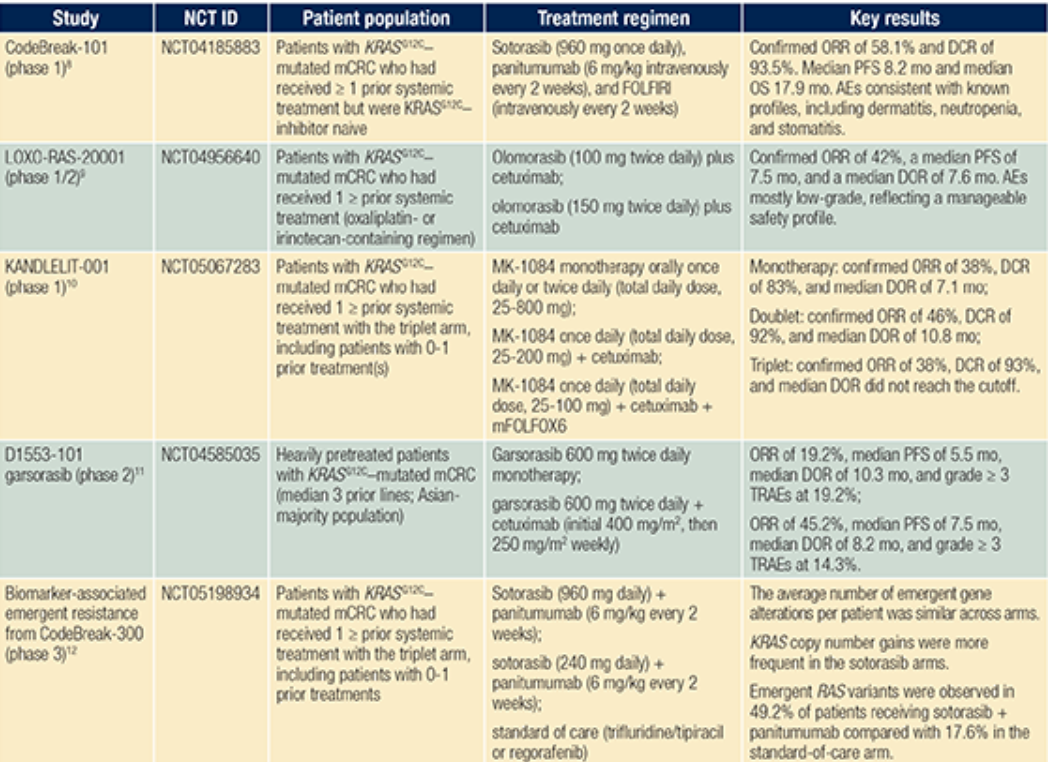
表1. KRAS G12C突变转移性结直肠癌中KRAS G12C靶向治疗及疗效的比较总结表
耐药机制
尽管基于生物标志物驱动的方法为这种传统上难治的结直肠癌亚群带来了希望,但耐药性仍不可避免地会出现。Ⅲ期CodeBreaK-300试验中配对血浆样本的生物标志物分析揭示了多种耐药机制,如TP53、DNMT3A、ERBB2和LRP1B的改变,以及KRAS拷贝数变异增加。这表明耐药性通过多种复杂机制产生,突显了KRAS G12C突变mCRC耐药性的复杂性。
正在进行的临床试验
索托拉西布和阿达格拉西布的毒性问题以及观察到的耐药机制,凸显了开发下一代KRAS抑制剂的迫切需求,以进一步推进索托拉西布和阿达格拉西布所取得的进展。
2025年ASCO年会上展示了多项阐述该领域进展的摘要(表1)。Ⅰ/Ⅱ期LOXO-RAS-20001试验展示了olomorasib(一种强效、选择性第二代KRAS G12C抑制剂,脱靶毒性有限)联合西妥昔单抗在既往接受过大量治疗的KRAS G12C突变mCRC患者中的良好疗效。该试验旨在确定这种联合治疗方案初步疗效、最佳剂量和安全性。先前的研究结果显示,该联合治疗脱靶毒性有限,且临床活性良好,为进一步评估提供了有力依据。在93例患者中,TRAEs大多为低级别,24%的患者出现≥3级毒性,与既往类似KRAS G12C靶向联合治疗研究报告的毒性发生率相当或略低,表明其安全性可控。此外,该联合治疗实现了42%的ORR、7.5个月的中位PFS和7.6个月的中位缓解持续时间。这些结果支持进一步研究该方案在既往接受过治疗的KRAS G12C突变结直肠癌中的作用。
另一种在研用于既往接受过治疗的mCRC的下一代KRAS G12C抑制剂格索雷塞(garsorasib)也显示出令人鼓舞的结果。格索雷塞具有更强的药效、药代动力学稳定性和更好的肿瘤穿透性,这可能有助于其临床活性。最近发表的Ⅱ期D1553-101试验评估了格索雷塞单药治疗及与西妥昔单抗联合治疗既往接受过治疗的KRAS G12C突变mCRC患者的效果。格索雷塞单药治疗疗效一般,但与西妥昔单抗联合治疗时疗效有所提高。14.3%的患者出现≥3级TRAEs,主要为皮疹和肝酶升高,表明其安全性可控。
最后,MK-1084 Ⅰ期KANDLELIT-001试验的早期结果也已公布。MK-1084是一种研究性、高选择性的下一代KRAS G12C抑制剂,旨在提供比早期药物更强的效力和更好的耐受性。这项首次人体试验招募了KRAS G12C突变mCRC患者,分为3个队列:单药治疗、MK-1084联合西妥昔单抗双药治疗以及MK-1084联合西妥昔单抗和mFOLFOX6三药治疗。主要终点是安全性和耐受性,次要终点包括初步疗效和药代动力学。单药治疗和双药治疗组纳入既往接受过≥1次全身治疗的患者,而三药治疗组纳入既往接受过0~1次治疗的患者。在单药治疗组的53例患者中,MK-1084显示出良好的耐受性。大多数TRAEs为低级别,皮疹和胃肠道症状最为常见。停药不常见,且未报告治疗相关死亡。此外,特别是在联合治疗组中,早期迹象显示出潜在疗效。这些结果支持在正在进行的Ⅲ期KANDLELIT-012试验(NCT06997497)中进一步评估MK-1084为基础的治疗方案在一线治疗中的效果。
综上所述,持续的临床试验探索对于优化疗效、控制耐药性以及确定这些药物在常规临床实践中的作用至关重要。各种联合治疗方案取得的良好结果凸显了KRAS G12C抑制剂的转化潜力。通过正在进行和未来将要进行的研究(尤其是在一线治疗中使用第二代KRAS抑制剂)的进一步验证,将明确其在KRAS G12C突变mCRC新治疗标准中的作用。随着治疗格局的不断演变,相信将分子学见解与临床结果相结合,对于为这一具有挑战性的结直肠癌亚群设计更有效、更持久和更个性化的治疗策略也至关重要。
参考资料:https://dailynews.ascopubs.org/do/beyond-monotherapy-evolving-combination-therapies-kras-g12c-mutant-colorectal-cancer
在结直肠癌的治疗领域,KRAS G12C突变犹如一座难以攻克的“堡垒”,长期以来给患者和医疗界带来了巨大挑战。传统单一疗法在应对这种复杂突变时,往往效果有限,难以满足患者对更有效、更持久治疗方案的迫切需求。然而,医学的进步从未停止脚步。近年来,针对KRAS G12C突变型结直肠癌的联合疗法正逐渐崭露头角,为这一困境带来了新的曙光。联合疗法通过整合多种治疗手段的优势,从不同角度对癌细胞发起攻击,有望突破单一疗法的瓶颈,显著提升治疗效果,延长患者的生存期,并改善其生活质量。
近日,Dr. Muhammet Ozer、Dr. Amy Little Jones、Dr. Timothy J. Brown在ASCO每日新闻深入探讨了KRAS G12C突变型结直肠癌联合疗法的最新研究进展,详细介绍了不同联合策略的原理、临床试验结果以及潜在的应用前景。希望通过这篇文章,能让广大医疗工作者、科研人员以及患者和家属对这一前沿治疗领域有更全面、深入的了解,共同期待联合疗法为KRAS G12C突变型结直肠癌患者带来更多的生存希望和更好的生活未来。同时,也期待更多的科研力量能够投入到这一领域,加速联合疗法的研发与应用,推动结直肠癌治疗迈向新的高度。

KRAS G12C突变型结直肠癌现状
KRAS G12C突变存在于约3%~4%的转移性结直肠癌(mCRC)病例中。作为mCRC的一个独特分子亚群,该种类型肿瘤通常对化疗具有耐药性,且对表皮生长因子受体(EGFR)靶向治疗的反应不佳。而共价KRAS G12C抑制剂,如索托拉西布(sotorasib)和阿达格拉西布(adagrasib),为治疗效果不佳的患者提供了新的治疗方法。当前,索托拉西布和阿达格拉西布在非小细胞肺癌中已显示出临床获益,并已获美国食品药品监督管理局(FDA)批准用于二线及后续治疗。然而,索托拉西布单药治疗mCRC的临床疗效一般,主要原因是存在适应性耐药机制,如EGFR信号的反馈性重新激活。因此,随着治疗格局的演变,涉及KRAS G12C抑制剂的联合治疗方案正逐渐兴起,为这种传统上难治的癌症亚型患者带来了希望。
阿达格拉西布和索托拉西布在结直肠癌中的应用
Ⅰ/Ⅱ期KRYSTAL-1试验评估了阿达格拉西布单药治疗及与西妥昔单抗联合治疗的效果。阿达格拉西布单药治疗的客观缓解率(ORR)为19%,中位无进展生存期(PFS)为5.6个月。阿达格拉西布与西妥昔单抗联合治疗显著提高ORR至46%,PFS至6.9个月。联合治疗常见的治疗相关不良事件(TRAEs)包括腹泻、恶心、呕吐、疲劳、痤疮样皮炎和骨髓抑制,约30%的患者观察到≥3级不良事件。
与此同时,Ⅰb期CodeBreaK-101试验评估了索托拉西布、帕尼单抗和FOLFIRI方案联合治疗KRAS G12C突变且未接受过KRAS G12C抑制剂治疗的mCRC患者的效果。在2025年ASCO年会上,报告了40例既往接受过中位2种全身治疗方案治疗的患者的长期疗效结果。研究报告显示,ORR为57.5%,疾病控制率(DCR)为92.5%,中位PFS为8.2个月,经过近30个月的随访,中位总生存期(OS)为17.9个月(详细结果及其他2025年会议摘要中的显著结果见表1)。常见的TRAEs包括痤疮样皮炎、中性粒细胞减少和口腔炎,50%的患者出现可管理的≥3级毒性。值得注意的是,索托拉西布和帕尼单抗的停药率较低(各为2.5%),表明总体耐受性良好,尽管化疗相关停药率仍较高,为40%。此外,左侧肿瘤患者以及在病程早期使用该方案治疗的患者,其总生存期明显更长。这些结果支持将KRAS G12C靶向治疗扩展至双重阻断之外,并强化了靶向治疗联合化疗的作用。
CodeBreaK-300试验证实了这些发现,该试验评估了索托拉西布与帕尼单抗联合治疗的效果。联合治疗在既往接受过治疗的KRAS G12C突变mCRC患者中显示出优于化疗的疗效,突出了双重通路抑制的益处。正在进行的Ⅲ期CodeBreaK-301试验(NCT06252649)将在一线治疗环境中进一步评估这种联合治疗方案,比较索托拉西布联合帕尼单抗与KRAS G12C突变mCRC患者的标准护理化疗。
表1. KRAS G12C突变转移性结直肠癌中KRAS G12C靶向治疗及疗效的比较总结表

耐药机制
尽管基于生物标志物驱动的方法为这种传统上难治的结直肠癌亚群带来了希望,但耐药性仍不可避免地会出现。Ⅲ期CodeBreaK-300试验中配对血浆样本的生物标志物分析揭示了多种耐药机制,如TP53、DNMT3A、ERBB2和LRP1B的改变,以及KRAS拷贝数变异增加。这表明耐药性通过多种复杂机制产生,突显了KRAS G12C突变mCRC耐药性的复杂性。
正在进行的临床试验
索托拉西布和阿达格拉西布的毒性问题以及观察到的耐药机制,凸显了开发下一代KRAS抑制剂的迫切需求,以进一步推进索托拉西布和阿达格拉西布所取得的进展。
2025年ASCO年会上展示了多项阐述该领域进展的摘要(表1)。Ⅰ/Ⅱ期LOXO-RAS-20001试验展示了olomorasib(一种强效、选择性第二代KRAS G12C抑制剂,脱靶毒性有限)联合西妥昔单抗在既往接受过大量治疗的KRAS G12C突变mCRC患者中的良好疗效。该试验旨在确定这种联合治疗方案初步疗效、最佳剂量和安全性。先前的研究结果显示,该联合治疗脱靶毒性有限,且临床活性良好,为进一步评估提供了有力依据。在93例患者中,TRAEs大多为低级别,24%的患者出现≥3级毒性,与既往类似KRAS G12C靶向联合治疗研究报告的毒性发生率相当或略低,表明其安全性可控。此外,该联合治疗实现了42%的ORR、7.5个月的中位PFS和7.6个月的中位缓解持续时间。这些结果支持进一步研究该方案在既往接受过治疗的KRAS G12C突变结直肠癌中的作用。
另一种在研用于既往接受过治疗的mCRC的下一代KRAS G12C抑制剂格索雷塞(garsorasib)也显示出令人鼓舞的结果。格索雷塞具有更强的药效、药代动力学稳定性和更好的肿瘤穿透性,这可能有助于其临床活性。最近发表的Ⅱ期D1553-101试验评估了格索雷塞单药治疗及与西妥昔单抗联合治疗既往接受过治疗的KRAS G12C突变mCRC患者的效果。格索雷塞单药治疗疗效一般,但与西妥昔单抗联合治疗时疗效有所提高。14.3%的患者出现≥3级TRAEs,主要为皮疹和肝酶升高,表明其安全性可控。
最后,MK-1084 Ⅰ期KANDLELIT-001试验的早期结果也已公布。MK-1084是一种研究性、高选择性的下一代KRAS G12C抑制剂,旨在提供比早期药物更强的效力和更好的耐受性。这项首次人体试验招募了KRAS G12C突变mCRC患者,分为3个队列:单药治疗、MK-1084联合西妥昔单抗双药治疗以及MK-1084联合西妥昔单抗和mFOLFOX6三药治疗。主要终点是安全性和耐受性,次要终点包括初步疗效和药代动力学。单药治疗和双药治疗组纳入既往接受过≥1次全身治疗的患者,而三药治疗组纳入既往接受过0~1次治疗的患者。在单药治疗组的53例患者中,MK-1084显示出良好的耐受性。大多数TRAEs为低级别,皮疹和胃肠道症状最为常见。停药不常见,且未报告治疗相关死亡。此外,特别是在联合治疗组中,早期迹象显示出潜在疗效。这些结果支持在正在进行的Ⅲ期KANDLELIT-012试验(NCT06997497)中进一步评估MK-1084为基础的治疗方案在一线治疗中的效果。
综上所述,持续的临床试验探索对于优化疗效、控制耐药性以及确定这些药物在常规临床实践中的作用至关重要。各种联合治疗方案取得的良好结果凸显了KRAS G12C抑制剂的转化潜力。通过正在进行和未来将要进行的研究(尤其是在一线治疗中使用第二代KRAS抑制剂)的进一步验证,将明确其在KRAS G12C突变mCRC新治疗标准中的作用。随着治疗格局的不断演变,相信将分子学见解与临床结果相结合,对于为这一具有挑战性的结直肠癌亚群设计更有效、更持久和更个性化的治疗策略也至关重要。
参考资料:https://dailynews.ascopubs.org/do/beyond-monotherapy-evolving-combination-therapies-kras-g12c-mutant-colorectal-cancer
- 推荐文章
高危胃肠道间质瘤(GIST)术后辅助治疗的五大争议与决策
胃食管交界部癌的多模式治疗:现状与未来方向丨2025韩国国际胃癌周
Jeeyun Lee教授解析多组学技术如何重塑胃癌免疫微环境丨2025韩国国际胃癌周
王绿化教授解析食管癌临床研究新进展:免疫治疗引领格局变革,中国原创方案重塑国际标准丨CSCO 2025
Nature Medicine丨AI赋能结直肠癌手术:个性化围手术期治疗的临床突破与未来方向
Joo Ha Hwang教授详解胃癌一、二级预防全球行动丨2025韩国国际胃癌周
食管鳞癌新辅助治疗迎来新突破!化免方案VS放化疗,生存、复发数据全面对比
李健教授:探索胃肠间质瘤联合治疗新策略,攻克TKIs耐药难关丨CACA东北整合肿瘤学大会 原创 肿瘤瞭望消化时讯 肿瘤瞭望消化时讯 2025-09-30 19:15:32 河北 手机阅读
共探胃癌诊疗新路径!2025韩国国际胃癌周中韩专场顺利举办,四大前沿研究擘画治疗未来
CACA东北整合肿瘤学大会丨徐泽宽教授:精准治疗时代胃癌诊疗机遇和挑战并存
应杰儿教授:以“整合”破局胃癌诊疗难题,以“康复”守护患者长期预后丨2025CACA东北整合肿瘤学大会
王峰教授展望未来食管癌精准免疫治疗新策略丨CSCO名家演讲集
ESMO 2025丨LBA重磅发布,消化道肿瘤领域最新进展一文纵览!
王峰教授:食管癌免疫治疗2.0时代:新联合策略+耐药探索丨CSCO名家演讲集
CACA东北整合肿瘤学大会丨李茂全教授:建立“诊、治、康、护、养”完整诊疗体系,推动胰腺癌个体化和规范化诊疗 原创 肿瘤瞭望消化时讯 肿瘤瞭望消化时讯 2025年9月25日 18:20
聚焦胃癌肝转移诊疗新进展:陈凛教授解析外科价值与多学科协作策略丨2025CACA东北整合肿瘤学大会
国际视角丨年轻人注意!早发性癌症发病率上升,肥胖和代谢差可能是“关键推手”
CSCO 2025丨吴胤瑛教授深度解读神经内分泌瘤诊疗指南更新,破局副神经节瘤精准诊疗新纪元
CSCO 2025丨方维佳教授详解肝癌围手术期免疫治疗新进展,这些突破值得关注!
CSCO 2025丨钱浩然主任医师解读高危GIST术后辅助治疗指南推荐与五大争议热点的破局之道
CSCO 2025丨王理伟教授解析晚期胰腺癌新药研究进展,精准治疗开启多靶点探索新时代
CSCO 2025丨邓艳红教授:结直肠癌中FOLFOXIRI三药方案临床应用进展
“瘤瘤”新知丨真实世界研究表明风险分层工具可提高上消化道肿瘤检出率
CSCO 2025丨项晓军教授:免疫治疗重塑胃癌“慢病化”全程管理新范式
岂有此“例”丨一例CLDN18.2阳性晚期胃癌患者接受含佐妥昔单抗治疗后出现胃炎的病例分析
CSCO名家视点丨李恩孝教授:胆道恶性肿瘤中国专家共识发布,加速我国胆道肿瘤诊疗规范化和精准化进程
CSCO 2025丨从“千人一方”到“量体裁衣",唐勇教授揭秘胃癌免疫治疗的精准标尺与分层策略
CSCO 2025丨勾红峰教授:免疫治疗时代下局部进展期胃癌诊治策略革新,豁免手术或成为可能
国际视角丨KRAS G12C突变结直肠癌最新进展:联合疗法开启治疗新纪元
术前贫血对直肠癌保肛手术近期及远期疗效有哪些影响?一项回顾性研究揭晓答案
革故鼎新,步召德教授详解直肠癌新辅助治疗的进展、挑战与未来变革|华夏结直肠病学论坛
利用真实世界数据提升临床试验结果普适性:一项前瞻性研究带来的洞见
杨林教授解读结直肠癌免疫治疗进展:精准分层与动态监测是未来方向|华夏结直肠病学论坛
沈琳教授团队:非V600E BRAF突变转移性结直肠癌的持续挑战与前沿治疗策略
华夏结直肠病学论坛丨孙立峰教授:聚焦结直肠癌腹膜转移个体化和精准化治疗策略
素食防癌再添实锤!最新研究表明吃素可降低癌症风险
“瘤瘤”新知丨AI导致内镜医师技能退化?《柳叶刀》研究揭示医疗AI的双刃剑效应
“冷肿瘤”破局之道:胡志前教授解读MSS型结直肠癌免疫治疗困境及探索|华夏结直肠病学论坛
岂有此“例”丨从脂肪肝到肝癌——一例MASH相关肝细胞癌的长期管理与成功移植
老年Ⅱ~Ⅲ期结直肠癌患者能否从奥沙利铂辅助化疗中获益?大型回顾性研究为您答疑解惑
血液or组织?转移性结直肠癌生物标志物检测最佳标本如何选择
谋“防”重“治”,毛友生教授详解中国食管癌防治优化之路与青年医师培养新策|2025CACA华中整合肿瘤学大会
心灵驿站丨生与死的奇妙共舞
肿瘤学年鉴:BFR14长期随访结果表明,13% GIST患者生存超过20年!
晚期HCC生存与生活质量兼得的治疗方案是什么?这项荟萃分析给出提示
多学科协同筑基石,创新实践领前沿——交大一附院李恩孝教授团队胃癌诊疗之路探微
令人鼓舞!PD-1联合基于短程放疗的TNT使pMMR局部晚期直肠癌CR率近翻倍
谋“效”思“变”,王峰教授阐述食管癌免疫治疗时代下的生存之变与未来之策|2025CACA华中整合肿瘤学大会
大数据揭示!男性肝硬化患者肝癌风险是女性的2倍
主席说丨西北地区胃癌诊疗经验与探索:从差异中寻共识,以协作促发展
樊嘉院士团队最新突破性研究成果见刊STTT:双免联合化疗或为晚期BTC一线治疗开辟新方向,有望改写临床实践指南
全程、精准、以人为本,陈小兵教授畅谈食管癌整合诊疗新范式|2025CACA华中整合肿瘤学大会
量体裁衣,居来提教授详解食管癌不同分期的MDT“排兵布阵”与功能保留之道|2025CACA华中整合肿瘤学大会
国际视角丨知名肿瘤专家为您解析2025年胆道癌治疗现状
“瘤瘤”新知丨多吃十字花科蔬菜可以降低结直肠癌的风险
