- 首页 > 正文
Joo Ha Hwang教授详解胃癌一、二级预防全球行动丨2025韩国国际胃癌周
发表时间:2026-01-30 17:47:11
编者按:
由韩国胃癌协会主办2025年韩国国际胃癌周(KINGCA WEEK 2025)于9月25日至27日在韩国首尔召开。本次大会上,斯坦福大学医学院Joo Ha Hwang教授做了以“胃癌一级与二级预防的全球行动”为题的专题报告。报告围绕全球视角下的胃癌现状、一级预防行动、二级预防行动三大板块展开,既整合了最新循证数据,也覆盖了不同地区的实践差异,为全球胃癌防控提供了从数据到策略的完整参考。以下为报告核心内容的完整梳理。
一、全球胃癌现状:循证数据锚定防 控方向
在过去的几十年中,胃癌的发病率在全球范围内一直在下降。尽管如此,GC仍然是第五大最常见的癌症,2018年病例超过1 000 000例,其中几乎三分之二发生在发展中国家。在所有人群中,男性的年龄标准化风险大约是女性的2~3倍,且患病风险随着年龄的增长而稳步上升,发病率最高的年龄段为生命的第六和第七个十年。GC的死亡率较高,全世界的存活率约为30%。值得注意的是,影响5年生存率的主要因素是诊断时的疾病阶段。实际上,早期检测到GC可使5年生存率达到80%。一级预防策略旨在减少风险因素并促进保护性因素,并联合通过检测和诊断存在癌前状态和病变(例如萎缩性胃炎,肠上皮化生和发育异常)的患者,从而可进行GC早期诊断的二级预防策略,来降低GC的发生率和死亡率,并降低医疗费用。
二、胃癌一级预防:以幽门螺杆菌根除为核心,区域指南各有侧重
在亚洲地区,各国指南呈现“聚焦高风险人群、部分待完善”的特点:韩国目前尚无现行国家指南,相关的HELPER研究(探索幽门螺杆菌根除对胃癌预防的作用)正在推进中;日本明确推荐对胃镜(EGD)检查显示存在慢性萎缩性胃炎的患者开展干预;中国暂无国家层面指南,正处于积极评估阶段;中国台湾地区则将50~69岁接受结肠癌筛查粪便检测的人群,同步纳入胃癌相关评估范围。
欧洲通过MAPS II指南提出明确建议:胃癌一级亲属应在20~30岁之间进行幽门螺杆菌无创筛查与根除,这一推荐属于条件推荐,基于中等质量证据,且达成了100%的专家共识。
为验证幽门螺杆菌根除的有效性,Joo Ha Hwang教授还重点介绍了两项关键研究:HELPER研究是韩国开展的大规模随机对照试验,2014年由韩国国家癌症中心联合国际癌症研究机构(IARC)发起,共纳入11 799例40~65岁参与者(50%为女性),按1:1随机分为干预组(接受10天铋剂四联疗法:甲硝唑500 mgqid+四环素500 mg qid+铋剂300 mg qid+兰索拉唑30 mg bid)与对照组(安慰剂),计划随访10年观察胃癌发病率,每两年进行内镜随访并开展中期分析,2019年已完成12个研究中心的招募。另一项GISTAR研究是多中心随机研究,旨在确定“幽门螺杆菌根除联合胃蛋白酶原检测”是否降低40~64岁人群的胃癌死亡率,干预组需接受幽门螺杆菌检测与胃蛋白酶原I/II检测(阳性者根除治疗),对照组不进行根除,随访周期为15年,相关结果已发表于BMJ Open。
此外,国际癌症研究机构(IARC)也推出相关工作组报告为全球策略提供指导:2014年则发布《幽门螺杆菌根除作为胃癌预防策略》,2025年发布《基于人群的幽门螺杆菌筛查与治疗策略用于胃癌预防:实施指南》(图1),2025年2月17~19日,IARC还在法国召开胃癌工作组会议,进一步细化防控方向。

图1. 基于人群的幽门螺杆菌筛查与治疗策略用于胃癌预防:实施指南
三、胃癌二级预防:内镜筛查为核心,平衡效果与经济成本
从早期胃癌诊断比例来看,韩国与美国的差异显著。根据Huang等的研究,韩国因普及胃癌筛查,2002年早期胃癌诊断比例约47%,此后逐年上升,2010年后稳定在70%左右(2016年达73%);而美国2002年该比例仅约26%,2010年后始终维持在24%~26%的较低水平(图2),这种差距主要源于韩国推行基于人群的胃癌筛查项目,美国则以机会性筛查为主。
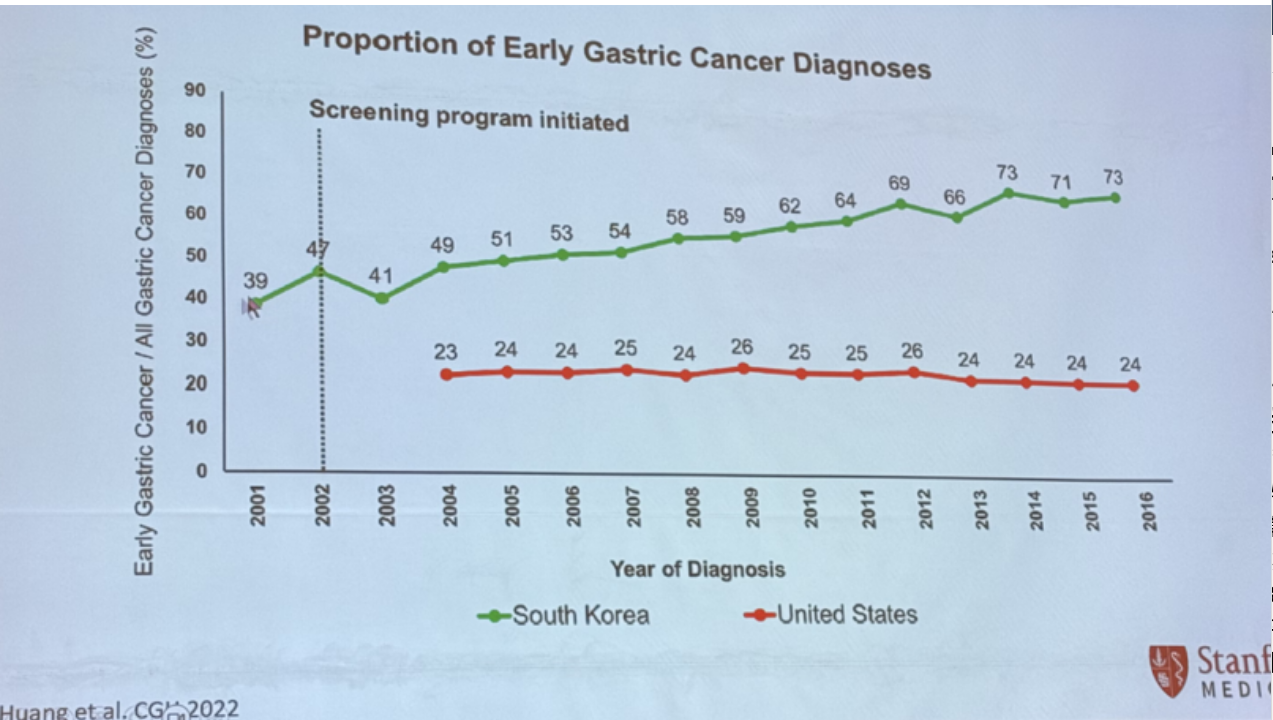
图2. 韩国和美国早期胃癌诊断比例
不过韩国的胃癌筛查也面临显著经济负担:2022年韩国胃癌筛查支出达7511亿韩元(约合5.778亿美元),占国家癌症筛查项目(NCPP)总支出的63%。从2010~2022年趋势来看,筛查支出从2010年的222.4亿韩元增至2022年的751.1亿韩元,涨幅超3倍;占NCPP总支出的比例也从2010年的56.6%波动上升,2021年达77.2%,2022年回落至63%(图3),相关数据由韩国国家癌症中心Il Ju Choi教授提供,且受欧盟共同资助项目EUR HELICAN支持。
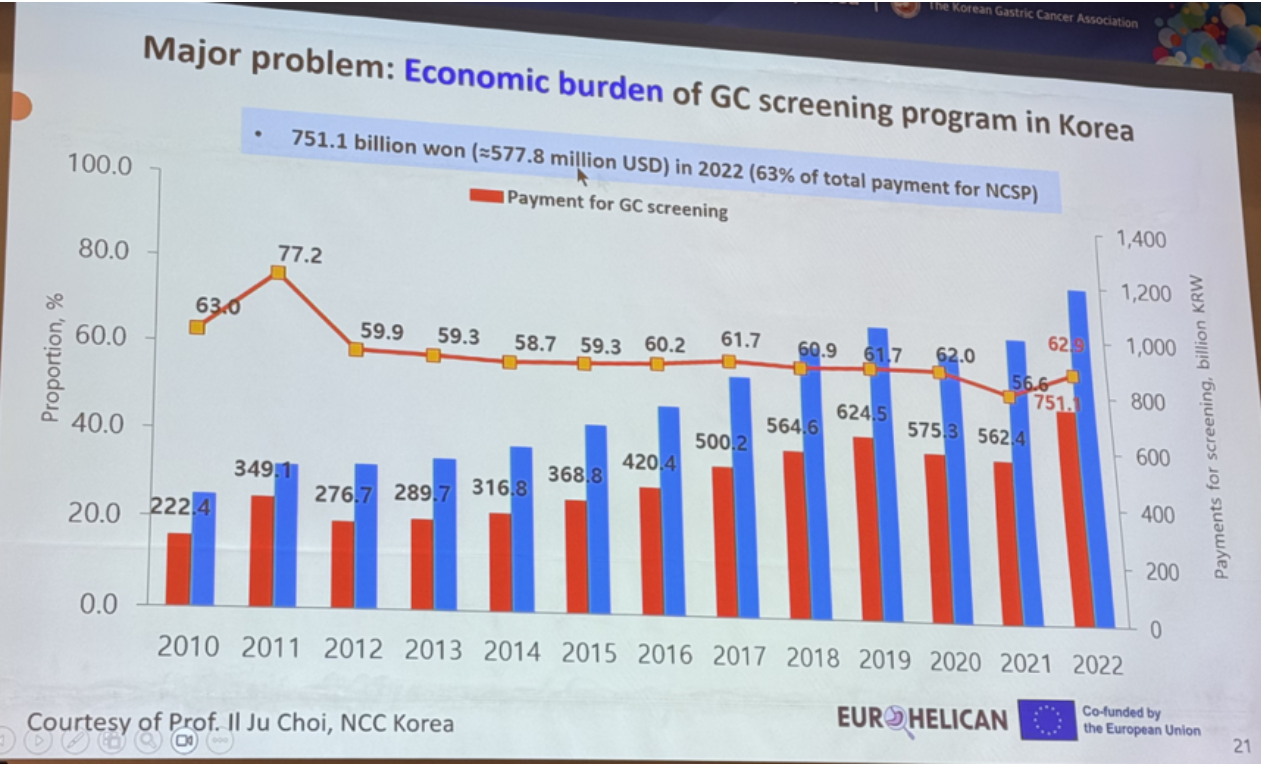
图3. 韩国筛查项目的经济支出
当然,不同种族/族群的筛查成本效益也存在差异,Monica Saumoy等在Gastroenterology发表的研究,基于Markov模型模拟了50岁人群的胃癌筛查成本效益。结果显示,采用“胃镜+mapping活检(±癌前病变监测)”对比“无筛查”,亚洲人群成本效益最优,而非西班牙裔白人因成本过高,该筛查策略并不适用。模型设计时还考虑了幽门螺杆菌感染状态、胃炎类型(正常、萎缩性胃炎、肠化生、异型增生)、胃癌分期(局部、区域、转移),以及三种筛查方案(肠化生者每3年监测、无论病理每2年筛查、无筛查)。
为了平衡内镜筛查的效果与经济成本,Joo Ha Hwang教授重点关注了非异型增生性胃黏膜癌前病变(GPMC)的管理,基于Morgan等人的研究,核心思路是“风险分层管理”。具体而言,胃黏膜肠化生(GIM)的低风险者无需进一步监测,若持续低风险则维持该方案;高风险者需在3年内复查以重新评估风险,若存在多个风险因素,还需考虑缩短复查间隔。而非肠化生萎缩性胃炎的低风险者无需监测,高风险者则需每3年进行内镜监测(图4)。其中,高风险因素包括:有胃癌家族史、属于高风险种族/族群(东亚人、拉丁裔、黑人及美洲印第安人/阿拉斯加原住民),以及胃窦和/或胃体活检显示重度GIM或重度萎缩性胃炎(“重度”定义为腺体受累≥2/3)。

图4. GPMC管理
2025年Endoscopy发布的欧洲MAPS III指南,进一步细化了胃癌二级预防的内镜筛查策略。指南明确,所有诊断性上消化道内镜(如因胃痛、反酸等症状进行的胃镜),均应同步开展胃癌筛查及癌前病变风险分层,且无论患者原籍国,这一推荐属于强烈推荐,基于中等质量证据,达成92%的专家共识。在人群筛查范围上,高风险地区(年龄标化发病率ASR>20/10万人年)需开展基于人群的筛查;中风险地区(ASR 10~20/10万人年)若成本效益可行,也应推进人群筛查;针对胃癌一级亲属的个体化筛查,间隔需根据ASR调整(ASR>20者每2~3年1次,ASR 10~20者每5年1次)。此外,指南还对高质量胃镜提出要求,需包含胃癌筛查、风险分层(使用虚拟染色内镜)、活检,以及早期胃癌分期和癌前病变评估;筛查停止时机则需根据患者整体健康状况与预期寿命综合判断,未明确具体年龄阈值。
Joo Ha Hwang教授指出,当前胃癌预防仍有两大核心问题待突破:一是风险分层细化,即明确哪些胃黏膜肠化生(GIM)患者真正存在进展为胃癌的风险;二是筛查间隔确定,需量化不同风险等级患者的最佳内镜筛查间隔。
为推动风险分层精准化,Joo Ha Hwang教授介绍了两种核心评估工具——悉尼协议活检和OLGIM分期。Gonzalo Latorre等在Gut发布的研究,验证了OLGIM分期的预测价值:OLGIM 0-I级的501例患者随访48个月,无1例进展为高度异型增生(HGD)或胃癌(CA);OLGIM II级的101例患者随访48个月,仅2例进展;OLGIM III-IV级的83例患者随访48个月,共8例进展(风险显著高于低级别),统计结果接近显著水平。
Joo Ha Hwang教授最后在报告总结中为全球胃癌防控明确路径:首先,全球胃癌分布处于动态变化中,需根据不同地区流行程度调整防控策略;其次,一级预防的核心已明确,幽门螺杆菌检测与根除可降低胃癌发病率,高流行区适合“基于人群的筛查”,低至中流行区则需“针对性筛查”;再者,二级预防通过内镜筛查可改善胃癌死亡率,高流行区人群筛查效果突出,但需平衡经济负担,低至中流行区应聚焦高风险人群;未来,二级预防亟需更精准的风险分层方法,以优化筛查间隔与成本效益。
- 推荐文章
