- 首页 > 正文
ASCO GI热点追踪|HER2检测新证据:一致性评估与动态变化对上消化肿瘤治疗决策的启示
发表时间:2026-03-04 15:30:37

两项研究PI:Kohei Shitara教授(左)和Brandon E. Rose教授(右)
本地检测与中心实验室总体一致,但IHC 2+人群需提高警惕
由日本国立癌症研究中心的Kohei Shitara教授领衔的研究团队,在DESTINY-Gastric04研究中评估了GC/GEJA患者本地实验室与中心实验室HER2检测结果的一致性(摘要号:434)。DESTINY-Gastric04研究显示,在HER2阳性转移性胃癌患者的二线治疗中,德曲妥珠单抗较雷莫芦单抗联合紫杉醇显著改善了总生存期。因此,研究者指出,准确判定HER2状态对于精准筛选可从该治疗方案中获益的患者至关重要。
在DESTINY-Gastric04研究中,共有833例患者在随机分组前接受了中心实验室的HER2检测,其中68%被判定为HER2阳性,包括59%为免疫组化(IHC)3+,以及9%为IHC 2+/原位杂交(ISH)阳性。在依据本地HER2检测结果被随机入组的133例患者中,有122例接受了回顾性的中心实验室HER2检测,其中82例检测样本来自原发灶肿瘤组织,40例来自转移灶组织。在同时接受本地与中心实验室检测的122例患者中,阳性一致率为80%;无论活检取自原发灶(79%)还是转移灶(80%),检测结果均表现出相似的一致性(表1)。
表1. 研究结果
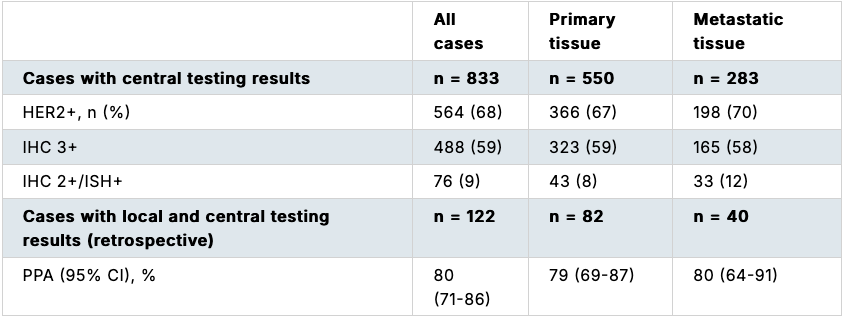
Kohei Shitara教授表示:“在二线治疗阶段对GC/GEJA患者进行HER2表达筛查时,本地实验室检测结果通常与中心实验室检测结果一致。”值得注意的是,一致性在不同HER2表达水平之间存在差异。本地检测判定为IHC 3+的样本中,阳性一致率为91%;而在IHC 2+/ISH阳性的样本中,该一致率仅为43%。Kohei Shitara教授指出,这与既往研究报道一致,提示IHC 2+人群需给予额外关注。
他进一步解释道:“总体而言,临床医生可以使用目前可获得的HER2检测方法对患者进行筛查,以识别可能从HER2靶向治疗中获益的人群。”同时,他也指出,本研究中所涉及的具体检测方法数量相对有限,这在一定程度上限制了对不同检测手段一致性分析的结论外推性。“此外,本研究仅分析了检测结果的一致性,并不能用于预测患者对HER2靶向治疗的潜在疗效反应。”Kohei Shitara教授补充道。
重复活检显示HER2易丢失,动态评估或具临床价值
HER2过表达约见于20%~30%的晚期上消化道肿瘤,在一线治疗中可通过化疗联合曲妥珠单抗±帕博利珠单抗进行有效靶向治疗。基于初始病理检测结果,HER2过表达也常被用于指导二线或更后线治疗,但其表达是否持续存在,既往并未得到充分认识。由美国德克萨斯大学西南医学中心的Brandon E. Rose教授团队领衔的研究,利用Flatiron Health真实世界研究数据库中2011~2025年的数据,评估了美国人群中HER2过表达持续存在的比例(摘要号:436)。
在纳入评估的17 305例上消化道肿瘤患者中,696例在初次检测至少7周后接受过至少1次HER2评估;其中333例符合研究纳入标准。共有83例患者(25%)在基线时被判定为HER2阳性。这部分患者男性比例更高(73%),既往或当前吸烟者比例更高(70%),且更可能在一线治疗中接受HER2靶向治疗(59%)。最常见的活检部位为原发灶,无论是在初次活检(88%)还是再次活检(67%)中均是如此。在后续活检中,36%的患者出现了HER2过表达的丢失。在IHC 2+/荧光原位杂交(FISH)扩增的患者中,该丢失比例高达83%,明显高于基线为IHC 3+的患者(28%)。
Brandon E. Rose教授表示:“对于HER2检测阳性的上消化道肿瘤患者,如果条件允许,在继续HER2靶向治疗前,可以考虑重复进行生物标志物评估,尤其是在IHC 2+/FISH扩增的情况下。我们在美国队列中观察到的HER2丢失比例,与来自亚洲的小样本研究结果总体一致。”
研究者推测,HER2过表达的丢失可能与HER2靶向治疗所产生的克隆选择压力有关,也可能源于肿瘤异质性或其他未知因素。尽管研究结果提示应更加重视重复活检和生物标志物评估的价值,Brandon E. Rose教授也指出,该研究仍存在一定局限性。他表示:“由于重复活检目前尚未纳入标准诊疗流程,研究中接受再次活检的患者可能存在选择性,这一点在解读结果时仍需加以考虑。真实世界研究本身存在诸多局限,但它仍然是挑战既有认知、提出新假设并最终改善患者照护的重要工具。”
小结
综合来看,这两项在ASCO GI上公布的研究,从不同维度深化了对HER2检测临床价值的认识。DESTINY-Gastric04的探索性分析提示,在当前临床实践中,本地实验室HER2检测总体具有较好的实用性,能够支持大多数患者的治疗决策,但在IHC 2+等边缘表达人群中,检测结果的不确定性仍不容忽视。与此同时,基于真实世界数据的研究进一步表明,HER2表达具有动态变化特征,部分患者在疾病进展或治疗过程中可能出现HER2过表达的丢失,这一现象在特定亚组中更为显著。
上述发现提示,HER2不仅是一个“静态”的入组或分层指标,其检测时间、检测方法及必要时的重复评估,都可能对后续治疗选择产生重要影响。随着抗HER2治疗策略不断丰富,如何在保证检测可及性的同时,实现更加精准、动态的HER2评估,将成为上消化道肿瘤精准治疗实践中值得进一步探索的重要方向。
参考文献:
[1]Kohei Shitara, et al. J Clin Oncol 44, 2026 (suppl 2; abstr 434)[2]Brandon Rose, et al. J Clin Oncol 44, 2026 (suppl 2; abstr 436)
- 推荐文章
