- 首页 > 正文
岂有此“例”|新辅助免疫治疗实现pCR:dMMR/MSI-H转移性结直肠癌的突破性病例分享
发表时间:2026-03-07 09:20:35
编者按
结直肠癌(CRC)是全球癌症相关死亡的主要原因之一,约20%的CRC患者在确诊时已发生远处转移,预后通常较差。尽管系统性化疗已将转移性CRC(mCRC)患者的中位总生存期提升至约30个月,但实现长期缓解的病例仍较罕见。值得注意的是,其中部分患者存在DNA错配修复缺陷及微卫星高度不稳定性(dMMR/MSI-H),这类肿瘤约占mCRC的4~5%,此类患者对免疫检查点抑制剂治疗高度敏感。dMMR/MSI-H型肿瘤因具有高肿瘤突变负荷及新生抗原负载,免疫原性较强,对PD-1抑制剂通常能产生显著反应。多项临床研究证实,免疫治疗显著改善了该类患者的治疗结局。KEYNOTE-177试验表明,帕博利珠单抗治疗组相比化疗组可显著延长dMMR/MSI-H型mCRC患者的无进展生存期,且影像学完全缓解率可达11%(化疗组仅为4%)。CHECKMATE与GARNET等研究也进一步验证了免疫治疗在dMMR/MSI-H型mCRC中的优势,使其被列为该人群的一线治疗选择。
本期《岂有此“例”》栏目报告一例dMMR/MSI-H型mCRC患者,在接受帕博利珠单抗新辅助免疫治疗后实现病理完全缓解(pCR)。该案例不仅凸显了免疫疗法在肿瘤降期方面的显著作用,也引发了关于免疫治疗后手术的必要性及pCR后辅助治疗策略的深入思考。
病例信息
1.患者信息
患者,男性,49岁,有长期吸烟史(35包/年),因排便习惯改变数月就诊。患者自述便秘加重,伴频繁少量排便、间歇性直肠出血、腹痛及体重减轻。既往无CRC或其他林奇综合征相关肿瘤病史及家族史,无其他明显合并症。初步腹部及盆腔CT提示直肠乙状结肠区域炎性改变,未见明确肿块(图1)。

图1. CT影像(轴位A、C,冠状位B)显示直肠乙状结肠区域炎症
随访时,患者自述症状持续存在,体格检查发现左下腹轻度压痛,未触及肿块。结肠镜检查发现乙状结肠中下段存在一环周肿块,近乎阻塞肠腔,形态呈恶性表现。结肠镜无法通过该肿块,肿块质地脆弱,有溃疡,接触后出血。取活检组织送病理检查。
病理检查显示高级别异型增生腺上皮,腺体结构紊乱伴固有层浅表浸润,提示为高分化腺癌(图2)。未见淋巴血管侵犯或神经周围肿瘤浸润。免疫组织化学检测显示MLH-1与PMS-2表达保留,MSH2与MSH6表达缺失,提示错配修复缺陷状态。分子检测检出KRAS G12D突变,BRAF、NRAS、PIK3CA、PTEN及AKT1均未见突变(图3)。
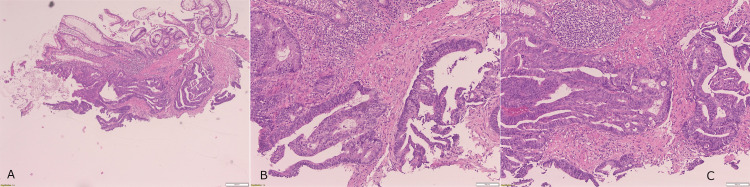
图2. 组织切片 H&E 染色结果,(A) 4倍镜视野,(B、C) 10倍镜视野
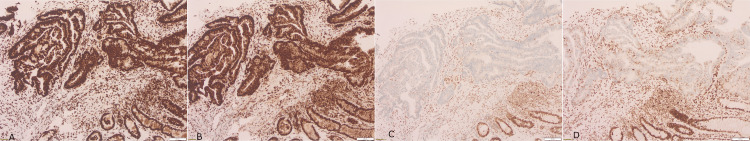
图3. 免疫组织化学切片,(A)MLH1、(B)PMS2、(C)MSH2 和 (D)MSH6
再次复查胸部、腹部及盆腔CT(图4)显示乙状结肠长段肠壁增厚伴管腔狭窄,区域淋巴结肿大,肝脏多发转移灶,最大直径3.2 cm,右肺上叶见一6 mm可疑小结节。原发肿瘤与膀胱及左侧盆壁分界不清,提示局部侵犯可能。
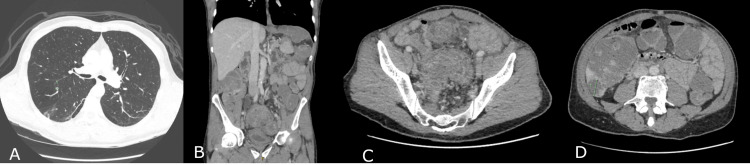
图4. CT 成像,(A)轴位 CT 切片显示肺部病变,(B)冠状位 CT 切片显示乙状结肠肿块,(C)轴位切片显示乙状结肠肿块,(D)轴位切片显示肝转移
2.治疗经过
患者因大肠梗阻风险而紧急入院并行手术治疗。术中施行剖腹探查及乙状结肠造口术作为姑息性处理,旨在为后续全身治疗创造条件。术中所见提示肿瘤与邻近组织(包括膀胱、盆腔侧壁及腹膜后间隙)广泛粘连,确认为局部晚期不可切除的病变。
基于其dMMR/MSI-H型分子特征,患者开始接受帕博利珠单抗免疫治疗,剂量为200 mg每三周静脉输注。治疗两个月后复查影像评估提示:腹部及盆腔病灶呈部分缓解,区域淋巴结肿大较前缩小,肝脏转移灶保持稳定,肺部结节无明显变化。免疫治疗期间,患者曾反复发生小肠梗阻,经保守治疗后缓解。此外,患者还出现了右侧尿路梗阻,经硬性膀胱镜引导下右侧输尿管双J管置入术后成功解除。
免疫治疗开始四个月后,患者出现高热及盆腔疼痛,复查CT显示原肿瘤区域新发多房性盆腔脓肿,伴广泛炎性改变及气液平面(图5)。患者随即入院,接受影像引导下脓肿引流及抗生素治疗。住院期间患者整体情况有所改善,但因盆腔感染持续存在,免疫治疗暂时中断。
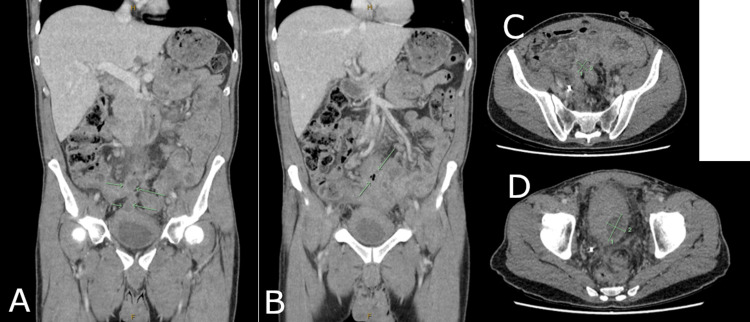
图5. CT影像冠状位(A、B)与轴位(C、D)扫描所示盆腔脓肿
经多学科会诊讨论,一致建议行手术治疗,以完成对残留盆腔病灶的挽救性切除并控制盆腔感染。患者接受了剖腹探查术,同期实施了超低位前切除术(ULAR)、受累小肠及回结肠整块切除术、肝脏可见转移灶的楔形切除术以及结肠造口还纳术。术后恢复过程顺利,患者于术后第10天出院。
术后病理学评估显示,患者达到pCR。直肠乙状结肠切除标本仅见纤维组织增生、炎性细胞浸润及治疗相关改变,未见存活腺癌细胞。清扫的直肠系膜及结肠系膜区域共计50枚淋巴结均未检出恶性肿瘤。小肠及回结肠标本未见癌残留,肝楔形切除组织仅显示坏死及纤维瘢痕形成,未见转移性肿瘤成分。综上,该结果证实新辅助免疫治疗在原发灶及转移灶均实现了pCR(ypT0N0)。
后续多学科团队建议患者恢复帕博利珠单抗治疗,以完成总计两年的免疫治疗疗程。术后10个月随访,患者无临床或影像学复发征象。近期全身氟代脱氧葡萄糖(FDG)PET-CT检查未见代谢活跃病灶,患者持续接受帕博利珠单抗治疗,未出现其他免疫相关不良事件。术后主要问题为肠道功能障碍,符合低位前切除综合征表现,目前予以保守治疗管理。患者目前仍在密切随访中,定期接受肿瘤标志物检测及影像学评估。患者自觉生活质量良好,并对整体治疗结果表示认可。
病例总结与分析
本文报告了一例独特病例:一名49岁男性患者,初诊为不可切除的dMMR/MSI-H型mCRC,在接受帕博利珠单抗新辅助免疫治疗及后续挽救性手术后,达到pCR。这一结果进一步证实了免疫检查点抑制剂在部分预后不良的dMMR/MSI-H型mCRC患者中具有显著疗效。
本病例中,免疫治疗期间出现的盆腔脓肿可能反映了肿瘤快速坏死后的继发性改变。值得注意的是,尽管治疗过程中出现并发症并需多学科团队介入处理,但并未影响最终治疗结局。如本例所示,在dMMR/MSI-H型mCRC的免疫治疗时代,肿瘤降期至可切除状态并伴显著缓解甚至术前根除的情况,可能逐渐成为临床常见现象。
本病例的重要探讨方向在于全身治疗达到pCR后的最佳管理策略。特别是对于术后实现pCR的患者,免疫治疗的巩固作用尚未明确。经多学科团队讨论,建议患者继续使用帕博利珠单抗以巩固疗效。该阶段缺乏明确临床指南的现状,突显了持续开展相关研究以优化完全缓解患者管理策略的必要性。
最后,本病例强调了全面的分子检测与协调有序的多学科诊疗在晚期CRC管理中的关键作用。通过快速明确肿瘤dMMR/MSI-H状态,患者得以接受免疫治疗,从而改变了疾病进程,从既往近乎终末期的预后转变为获得pCR可能。同时,多学科团队在并发症处理与手术时机决策中的协作也至关重要。综上所述,在本病例中,先进的诊断技术、新型全身治疗策略与多学科协作的共同作用,实现了以往在mCRC治疗中难以达到的卓越疗效。
参考文献:Hanekom BL, et al. Cureus. 2025 Dec 26;17(12):e100109.
- 推荐文章
