- 首页 > 正文
ASCO GI|可切除胃癌新辅助治疗策略探索:化疗序贯放化疗方案综合获益更优
发表时间:2026-03-07 09:27:06

从左至右依次为Marcel Verheij教授(研究讲者)、Christopher Leigh Hallemeier教授(研究讨论者)
研究要点总结
目前针对胃癌患者的证据支持围手术期化疗、术后放化疗或单纯化疗。然而,患者对术后治疗依从性较低,影响疗效。
Ⅱ期CRITICS-Ⅱ研究结果显示对于可切除胃癌患者,新辅助化疗序贯放化疗可能优于单纯新辅助化疗或新辅助放化疗。在随访1年时,采用新辅助化疗序贯放化疗方案的患者,无事件生存期(EFS)率达84%,而单纯化疗组为68%,单纯放化疗组为78%;联合治疗组的总生存(OS)率为89%,单纯化疗组为74%,单纯放化疗组为84%。
探索与优化:聚焦术前治疗,探寻改善可切除胃癌预后的新策略
根治性手术仍然是治疗非转移性可切除胃癌的基石,但患者生存率较差。围手术期化疗、术后放化疗和术后化疗可以改善预后,但患者依从性尤其是术后治疗依从性很低。术前治疗能够提高患者治疗依从性、诱导肿瘤降期并提高R0切除率。Marcel Verheij教授表示“鉴于已有充分报道显示患者在术后治疗阶段的依从性较差,我们认为,任何辅助手术治疗的益处都应来自强化术前治疗方案,同时省略术后治疗。这与在食管癌、直肠癌和胰腺癌中观察到的趋势相似。”在此背景下,Marcel Verheij教授团队开展了CRITICS-Ⅱ研究,比较了三种术前治疗方案(均未使用辅助治疗):新辅助化疗(方案1)、新辅助化疗序贯放化疗(方案2)以及新辅助放化疗(方案3),旨在确定最具疗效且安全的策略,以推进至Ⅲ期临床研究,从而适应当前治疗发展的趋势。
革新与突破:多方面评估,新辅助化疗序贯放化疗展现综合治疗优势
研究纳入临床分期为ⅠB~ⅢC期(TNM第8版)的可切除、无远处转移的胃腺癌患者,随机分配接受:4个周期的多西他赛+奥沙利铂+卡培他滨(DOC)(组1);2个周期DOC后序贯放化疗(45 Gy/25次+每周紫杉醇/卡铂)治疗(组2);或单纯上述相同的放化疗方案治疗(组3)。研究主要终点为1年EFS率,判定标准为:EFS率≤60%视为活性不足,≥75%视为具有足够的临床活性。次要终点包括毒性、并发症、手术结果、R0切除率、肿瘤退缩分级、复发率、OS、依从性和健康相关生活质量。
2017~2024年间,来自16家荷兰参与中心的201例患者接受随机分组(组1包括68例患者、组2包括65例患者、组3包括68例患者)。患者基线特征整体均衡,但组3中胃部肿瘤(而非胃食管结合部或其他部位肿瘤)患者比例(93%)高于组1(85%)与组2(78%)。全队列中位年龄为67岁,63%为男性。中位随访时间为40.4个月。
在治疗完成情况与手术质量方面,组1、组2、组3分别有81%、65%、84%的患者完成术前治疗。三组分别有60例、58例和63例患者接受了根治性手术,R0切除率分别为98%、98%和94%。完成全部治疗(包括手术)的患者比例分别为79%、63%和78%。Marcel Verheij教授强调,该研究中手术质量优异,全队列中91%的患者接受了D1+或D2淋巴结清扫(组1为93%,组2为90%,组3为90%)。全队列中位淋巴结清扫数量为25枚,其中组1中位数为31枚,组2为23枚,组3为21枚。全队列住院期间死亡率相对较低,仅为4%。
在疗效方面,EFS分析显示组2获益最显著(见图1)。治疗1年后,组2的EFS率为84%,而组1与组3分别为68%和78%。总生存数据呈现相似趋势,1年OS率在组1、组2、组3分别为74%、89%和84%,组2仍为最高。在病理缓解方面,组2的pCR率达20%,明显高于组1的8%与组3的13%。综合上述结果,组2的术前治疗方案在生存获益与肿瘤退缩方面均展现出更优潜力,具有进一步研究的价值。
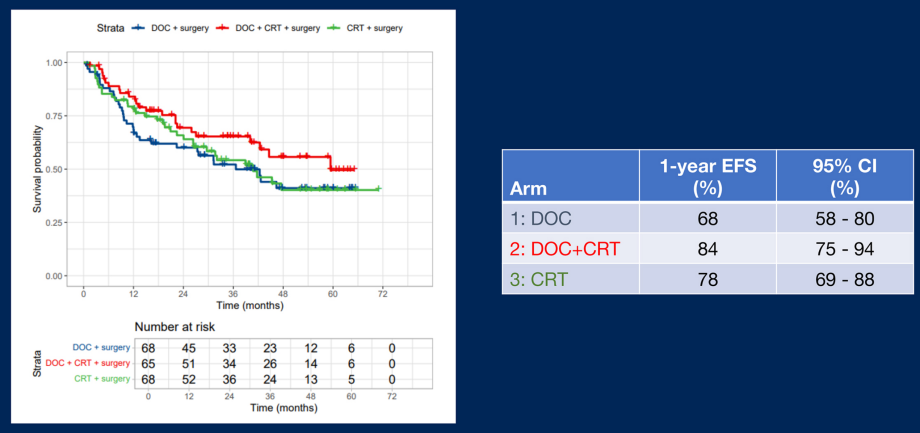
图1. EFS分析结果
在安全性方面,组1、组2、组3的3~5级术前不良事件发生率分别为56%、55%、43%。手术相关并发症(任何类型)发生率在组1与组3均为21%,组2为15%。
Marcel Verheij教授表示,尽管新辅助化疗序贯放化疗的整体优势在意料之中,但其EFS优于CRITICS与TOPGEAR等其他研究的结果则出乎预料[2,3]。不过他同时强调,后两者为随机Ⅲ期研究,因此无法直接进行比较。
专家评论
Marcel Verheij教授在总结时指出:“对于可切除胃癌患者,新辅助化疗序贯放化疗作为术前方案,在初步结果中显示出优于单纯化疗或单纯放化疗的趋势。”但他同时指出:“由于该研究采用Ⅱ期‘优选策略’设计,三组之间进行直接的统计学比较存在挑战。此外,研究未纳入当前标准治疗作为对照,主要基于胃癌临床研究入组速度较慢、且治疗标准在研究期间可能更新的现实考量。尽管如此,综合考虑生存结局、手术并发症及病理缓解率等指标,新辅助化疗序贯放化疗这一策略具备进一步深入研究的价值。”
在随后的讨论环节中,梅奥医学中心的Christopher Leigh Hallemeier教授对此表示认同。他指出,该治疗方案有望成为提升患者治疗依从性与治疗反应率的有效策略。并补充道:“尽管CRITICS-Ⅱ研究所采用的新辅助化疗联合放化疗方案取得了令人鼓舞的结果,其疗效与安全性仍需在更严谨的前瞻性研究中进一步验证。”
小结
基于CRITICS-Ⅱ研究结果,单纯术前化疗方案因其未能达到预设的EFS阈值,并呈现出相对较低的生存率与较高的治疗相关毒性,故不推荐作为后续重点研究方向。相比之下,新辅助化疗序贯放化疗(方案2)与单纯新辅助放化疗(方案3)均表现出足够的临床活性,展现出进一步研究的潜力。其中,方案2在EFS、OS、pCR、手术并发症等方面表现更优,提示其可能带来更显著的生存获益与肿瘤退缩效果;而方案3则在治疗依从性与安全性方面具有一定优势。
综合评估疗效、安全性及手术相关结局,新辅助化疗序贯放化疗展现出相对均衡且积极的趋势,因而被遴选为最具潜力的候选方案,值得在未来开展更深入的Ⅲ期临床研究。尤其是在当前胃癌治疗向精准化与器官保留策略发展的背景下,该方案为优化可切除胃癌的术前治疗模式提供了有价值的新方向,但其最终临床地位仍需通过大规模前瞻性研究进一步确认。
《肿瘤瞭望消化时讯》在2026 ASCO GI现场报道
参考文献
[1].Marcel Verheij, et al. ASCO GI 2026. Abstract:283.[2].Cats A, et al. Lancet Oncol. 2018;19(5):616-628.
[3].Leong T, et al. N Engl J Med. 2024;391(19):1810-1821.
- 推荐文章
