- 首页 > 正文
JCO丨可切除及临界可切除胰腺癌围术期VTE发生率达9%,死亡风险翻倍
发表时间:2026-03-07 12:43:12
编者按
静脉血栓栓塞(VTE)是胰腺导管腺癌(PDAC)患者常见的严重并发症,与较差的总生存期(OS)相关,常预示着更强的肿瘤侵袭性。PDAC是癌症相关死亡的第四大原因,仅约20%的患者在诊断时具备手术切除条件。既往直接手术是可切除PDAC的标准治疗方案,但PREOPANC-1研究证实,新辅助放化疗将可切除及临界可切除PDAC患者的5年OS率从6.5%提升至20.5%,推动了新辅助治疗策略的临床推广。
然而,关于可切除及临界可切除PDAC患者在新辅助治疗期间VTE发生率的数据仍比较少。现有指南基于对转移性疾病患者的研究,建议对所有PDAC患者考虑全身治疗期间的血栓预防,但其在新辅助治疗人群中的适用性尚未明确。PREOPANC-2研究比较了两种新辅助方案在可切除及临界可切除PDAC患者中的疗效,结果显示两组OS无显著差异。本研究基于PREOPANC-2试验,旨在系统评估该人群在新辅助治疗期间及术后1年内VTE的发生率,并探讨VTE与患者生存结局的相关性,相关结果近期发表于Journal of Clinical Oncology杂志。本文将对该研究的设计、结果及其临床意义进行系统解读。

研究设计
PREOPANC-2是一项研究者发起的多中心、随机对照Ⅲ期试验,于2018年6月~2021年1月在荷兰纳入了可切除和临界可切除PDAC患者。入选标准为经影像学检查确认无远处转移、经组织学或细胞学证实的PDAC。患者被随机分配至新辅助化疗(5-氟尿嘧啶、亚叶酸钙、伊立替康和奥沙利铂)后行手术(FFX组)或新辅助吉西他滨为基础的放化疗(CRT)后行手术及辅助吉西他滨治疗(CRT组)(图1)。本二次分析的主要结局指标为静脉血栓栓塞(VTE),次要结局指标为动脉血栓栓塞(ATE)。
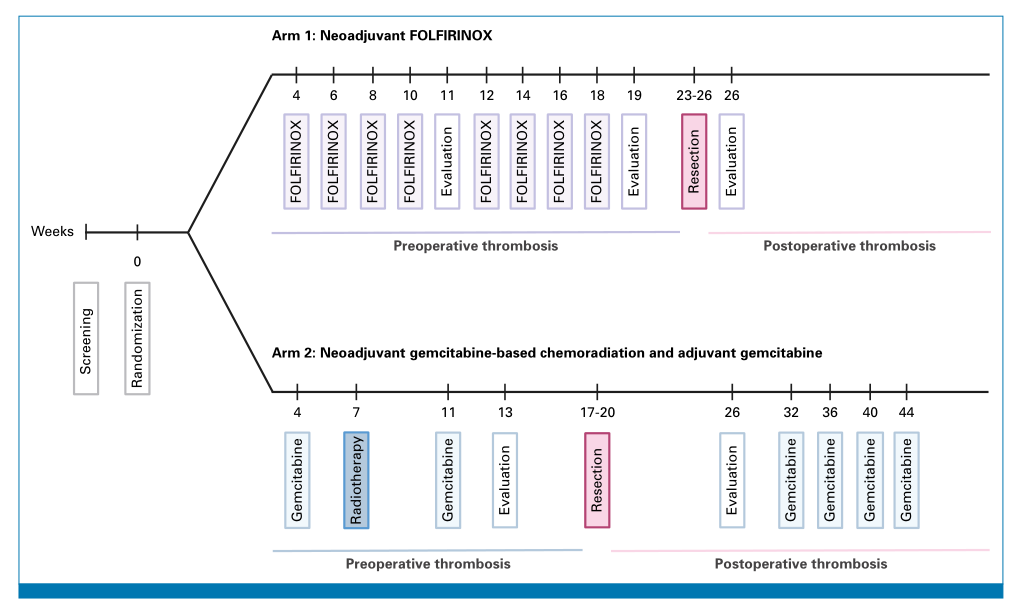
图1. PREOPANC-2研究设计,包括术前和术后血栓栓塞事件的时间线。PREOPANC-2试验两组的治疗方案概述。术前期定义为从随机分组到手术或疾病进展的时间;术后期定义为从肿瘤切除到随机分组后1年。FOLFIRINOX方案,包括5-氟尿嘧啶联合亚叶酸钙、伊立替康和奥沙利铂
研究结果
共325例患者纳入二次分析,其中FFX组158例,CRT组167例。其中,FFX组120例(76%),CRT组127例(76%)接受了切除术。FFX组从随机分组至手术的中位时间显著长于CRT组(22周 vs. 16周,P=0.001),而两组从手术切除至随访结束的中位时间无统计学差异(FFX组17周 vs. CRT组18周,P=0.17)。
VTE发生率
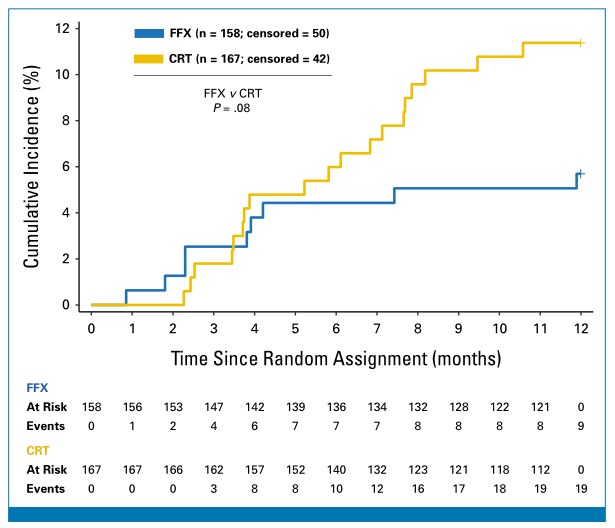
随机分组后1年内,全队列共28例患者(9%)发生VTE,其中FFX组9例(6%),CRT组19例(11%)(表1;图2)。全队列3个月VTE累积发生率为2%(95%CI:1%~4%),两组间无显著差异(FFX组3% vs. CRT组2%,P=0.67);12个月VTE累积发生率为9%(95%CI:6%~12%),两组间差异接近统计学意义(FFX组6% vs. CRT组11%,P=0.059)。
表1. 静脉和动脉血栓栓塞事件:术前和术后
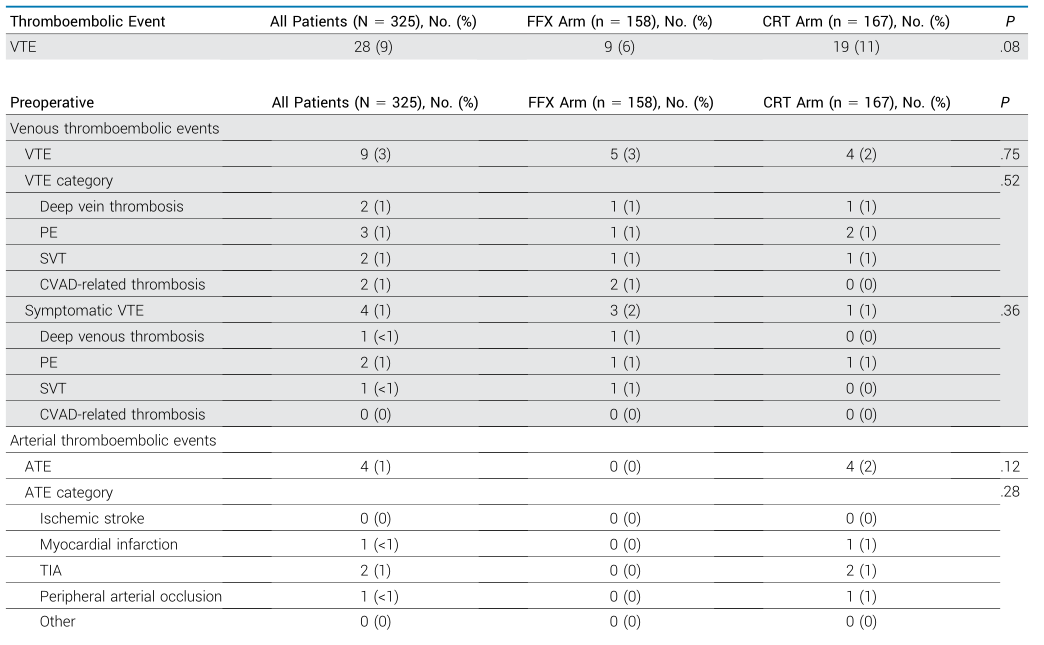
术前VTE发生率
新辅助治疗期间,325例患者中9例(3%)发生VTE,其中FFX组5例(3%),CRT组4例(2%),两组间无统计学差异(P=0.75;表1)。从随机分组至VTE发生的中位时间为术前阶段的75天。VTE类型包括肺栓塞(PE)3例(1%)、深静脉血栓形成(DVT)2例(1%)、浅表静脉血栓(SVT)2例(1%)及中心静脉通路(CVAD)相关血栓2例(1%)。新辅助治疗阶段发生的9例VTE中,4例(44%)为有症状性事件;2例(22%)患者因VTE导致后续化疗周期延迟,但没有患者因VTE导致化疗永久中断。术前发生VTE的患者切除率显著低于未发生VTE的患者(44% vs. 77%,P=0.02)。
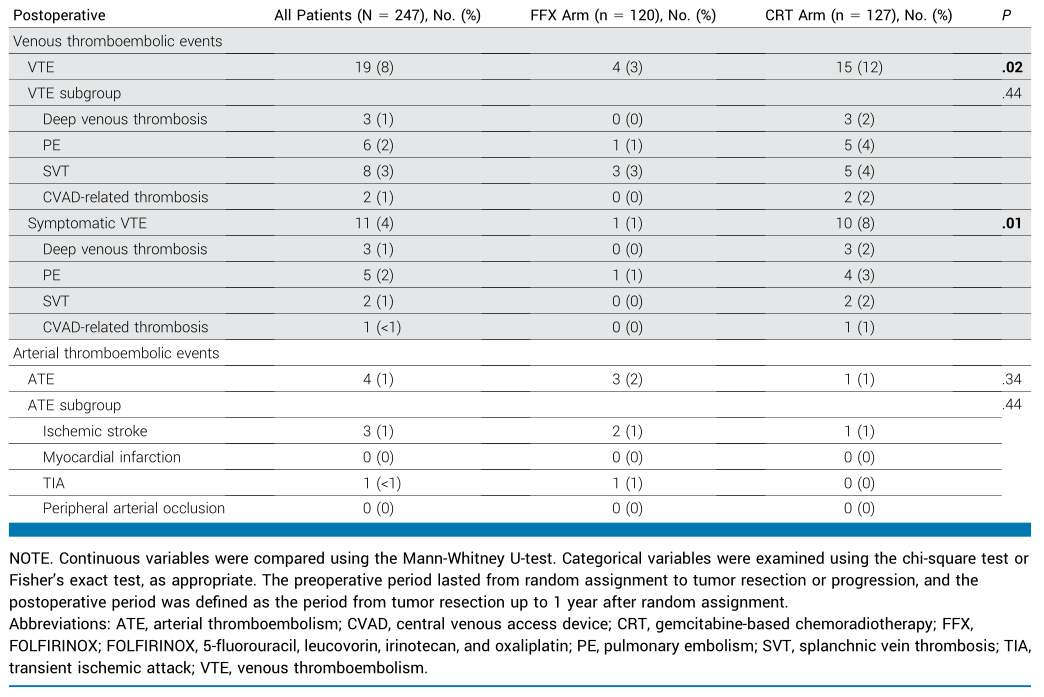
术后VTE发生率
247例接受手术切除的患者中,19例(8%)在切除术后至随机分组后1年内发生VTE(表1)。从手术切除至VTE发生的中位时间为60天(四分位距,9~144天)。其中FFX组4例(3%),CRT组15例(12%,P=0.02)。术后VTE中,11例(58%)为有症状性事件;4例(21%)患者发生VTE时接受了抗凝治疗(3例为预防性抗凝,1例为治疗性抗凝)。CRT组15例术后VTE患者中,4例在吉西他滨辅助治疗前发生,4例在治疗期间发生,2例在完成治疗后发生,5例未启动辅助治疗。化疗期间发生的1例VTE导致治疗延迟。2例患者因PE相关原因死亡:1例于切除术后2天发生循环骤停,经溶栓治疗无效死亡;另1例于术后4个月确诊疾病进展合并PE,因PE相关呼吸困难接受姑息镇静治疗后死亡。接受手术切除且未接受治疗性抗凝的患者中,89例(36%)接受了延长术后血栓预防(FFX组41例[34%] vs. CRT组48例[38%]),中位持续时间为4周(四分位距,4~6周),自手术切除之日起计算。
VTE治疗
术前或术后发生VTE的患者中,89%接受了抗凝治疗(图3)。所有PE、DVT及CVAD相关血栓患者均接受抗凝治疗,而SVT患者接受抗凝治疗的比例为70%。抗凝药物选择包括:52%的患者使用治疗剂量的低分子肝素(LMWH)、19%的患者使用直接口服抗凝药(DOAC)、4%的患者使用普通肝素,15%的患者使用LMWH序贯DOAC。
28例VTE患者的抗凝治疗疗程:10例(36%)接受无限期抗凝,4例(14%)治疗24周,3例(11%)治疗12周,2例(7%)治疗6周,2例(7%)治疗4周(7例患者数据缺失)。
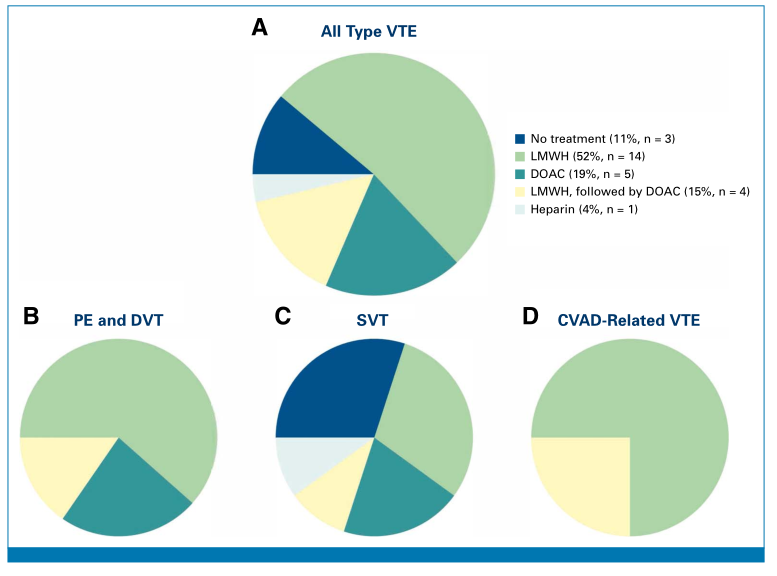
图3. 静脉血栓栓塞事件的治疗:(A)所有类型的VTE,(B)PE和DVT,(C)SVT,以及(D)CVAD相关性VTE
VTE发生的风险因素
单变量Fine-Gray模型分析显示,较高的体重指数(BMI)、较低的WHO体力状态评分及CA 19-9>500 U/mL与VTE发生风险显著相关(BMI 25~30 kg/m2:亚分布风险比[sHR]=2.65,95%CI:1.03~6.83;BMI≥30 kg/m2:sHR=5.21,95%CI:1.77~15.30;WHO体力状态1级:sHR=0.38,95%CI:0.16~0.95;CA 19-9>500 U/mL:sHR=2.13,95%CI:1.01~4.48)。
VTE与生存期的关联
全队列患者中位OS为21个月(95%CI:11~36个月),70%的患者在随访期间死亡(229/325)。多因素分析显示,在校正年龄、性别、肿瘤分期、肿瘤位置、手术切除状态、治疗组及基线CA 19-9水平后,VTE发生仍与OS显著降低独立相关(调整后HR=2.13,95%CI:1.31~3.46,P=0.002),且与无进展生存期(PFS)显著降低相关(调整后HR=1.94,95%CI:1.18~3.20,P=0.009;图4)。
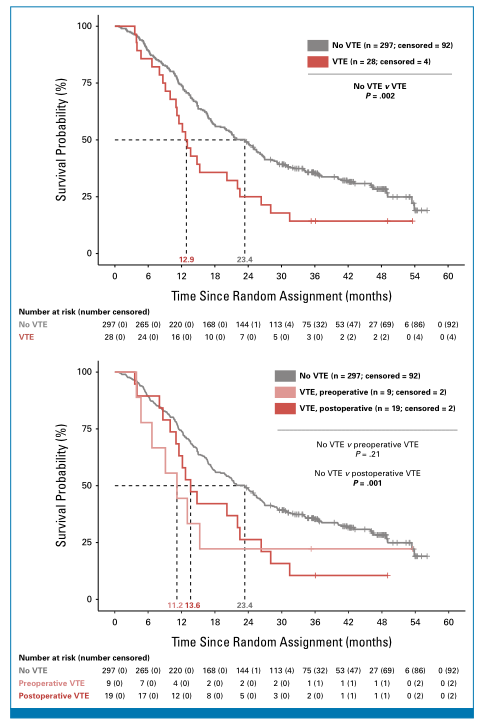
图4. 可切除和临界可切除胰腺癌患者的OS:按VTE发生情况进行的Kaplan-Meier分析:(A)随机分组后12个月内未发生VTE(灰色)和发生VTE(红色)患者的OS。(B)按VTE发生时间分层的OS:无VTE(灰色)、术前VTE(粉色)和术后VTE(红色)。每张图下方显示风险人数
时间依赖性单变量Cox回归模型显示,术前VTE与OS(HR=1.68,95%CI:0.75~3.80,P=0.21)或PFS(HR=1.37,95%CI:0.51~3.69,P=0.53)无显著关联;而术后VTE与OS(HR=2.29,95%CI:1.39~3.76,P<0.001)及PFS显著降低(HR=3.82,95%CI:1.23~3.66,P=0.007)相关。
研究结论
在PREOPANC-2研究纳入的可切除及临界可切除PDAC患者中,新辅助放化疗期间VTE发生率为3%,手术切除后1年内VTE发生率为8%。VTE发生与患者OS降低显著相关,这一关联可能反映了VTE作为生物学侵袭性更强的肿瘤的附带现象。本研究结果强调,需进一步开展针对性研究以评估该类患者群体的VTE风险分层及预防策略。
讨论
本研究为PREOPANC-2试验的二次分析,共纳入325例接受新辅助治疗的可切除及临界可切除PDAC患者,随机分组后1年内围手术期VTE总发生率为9%,其中术前VTE发生率3%,术后VTE发生率8%。CRT组术后VTE风险显著高于FFX组,而两组总体VTE累积发生率无统计学差异。超过半数的VTE为有症状性事件。
随机分组后1年内发生围手术期VTE的患者OS显著降低,这与Frere等人的研究结果一致——该研究纳入所有分期PDAC患者,发现VTE发生与OS较差显著相关(HR=2.02,95%CI:1.57~2.60,P<0.001)。但与Krepline等人的研究结果不同,后者纳入可切除及临界可切除PDAC患者,未发现新辅助阶段VTE与OS存在关联(17个月 vs. 24.6个月,P=0.11)。本研究中仅2例患者死于PE相关原因,且VTE与PFS降低相关,提示VTE更可能是肿瘤侵袭性更强的标志,而非直接死因。这一解释得到既往研究支持:尽管血栓预防可降低VTE发生率,但在PDAC患者中并未转化为生存获益。
既往研究报道,接受新辅助放化疗的可切除及临界可切除PDAC患者术前VTE发生率为6%~14%。相比之下,本研究队列术前VTE发生率为3%(含PE/DVT 2%、SVT 1%、CVAD相关血栓1%),低于既往报道范围。可能的原因包括:随机分组前筛查阶段确诊的SVT未被纳入统计,导致SVT发生率低估;此外,VTE定义、事件判定标准及病例组合的差异也可能导致不同研究间发生率的异质性。因此,未来肿瘤学试验中需结构化、前瞻性地报告血栓栓塞事件,尤其在PDAC等高危肿瘤中,以提高研究间的可比性与结果可靠性。
PREOPANC-2试验中仅0.8%的患者根据欧洲肿瘤内科学会(ESMO)指南接受门诊全身治疗期间的血栓预防。美国临床肿瘤学会(ASCO)、美国国立综合癌症网络(NCCN)及美国血液学会(ASH)指南均建议,Khorana评分≥2分且启动化疗的患者应进行血栓预防。由于PDAC诊断本身在Khorana评分中赋予2分,上述指南实际上隐含对所有PDAC化疗患者进行血栓预防的建议,但这些建议主要基于晚期疾病研究证据。本研究显示,接受新辅助治疗的可切除/临界可切除PDAC患者VTE发生率较低,提示当前指南在该人群中的应用需谨慎,需结合患者个体风险因素进行综合评估。
参考文献:
Willems RAL, et al. J Clin Oncol. 2026 Jan 29:JCO2501935.- 推荐文章
