- 首页 > 正文
年度盘点丨胃肠研途,智领前沿——沈琳教授团队2025学术攻坚实录
发表时间:2026-03-07 12:12:37
编者按
在消化道肿瘤这一全球性健康挑战面前,精准医学与创新疗法的探索从未止步。北京大学肿瘤医院沈琳教授及其团队,作为该领域的中坚力量,2025年持续迸发强劲的科研活力、展现扎实的学术引领力,研究工作贯穿基础探索至临床转化全链条。团队全年的研究实践,清晰勾勒出以临床需求为根本驱动、以多学科协作为坚实基石、以攻克关键科学问题为核心导向的创新路径。这些探索与努力,不仅为破解胃癌、结直肠癌(CRC)等疾病的治疗瓶颈提供了中国智慧与中国方案,更向全球消化系统肿瘤精准治疗领域注入了强劲的中国动力。本文旨在系统梳理沈琳教授团队在2025年的关键学术贡献,并展望其引领的未来方向。
1月

沈琳教授受邀做客Med平台,深度解析了转化研究在肿瘤治疗创新中的核心价值及其具体应用实例,并揭秘了她当前引领的多项前沿研究项目。此外,沈琳教授还深刻剖析了中国创新药物研发所面临的挑战与机遇,并对肿瘤精准治疗的未来发展趋势提出了独到见解。作为兼具科学家、临床医师及团队领导多重身份的她,亦慷慨分享了如何在研究、临床实践及人才培养之间寻求平衡的经验之道。
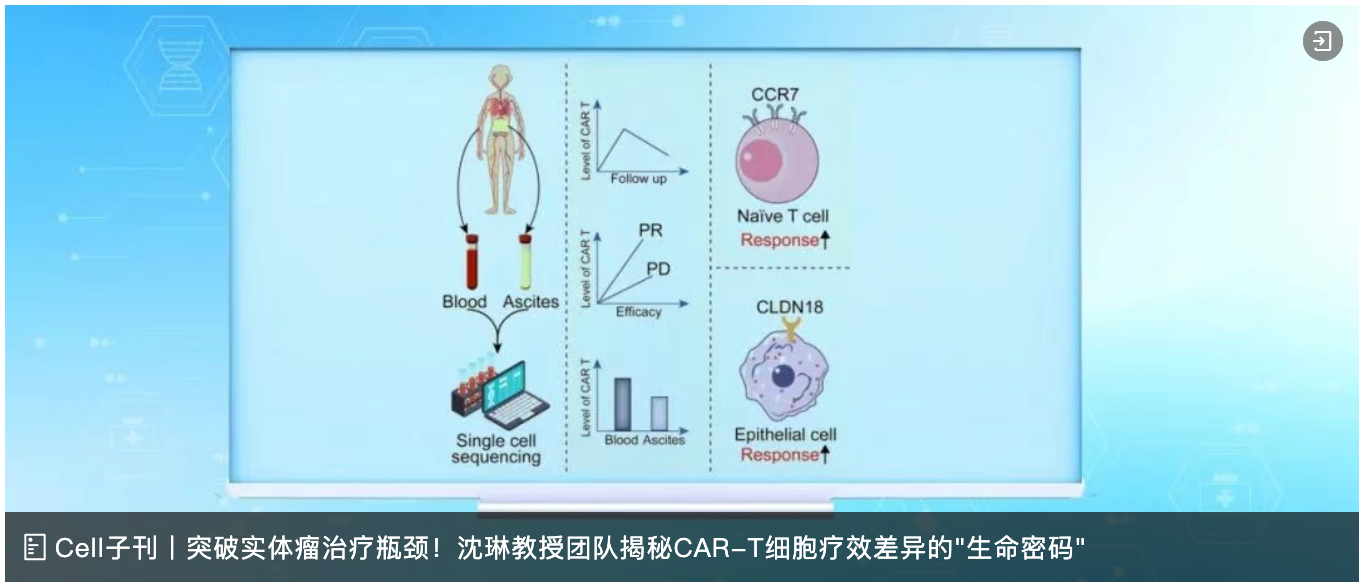
2月
4月

临床研究根据发起者的不同,分为研究者发起的临床研究(IIT)和制药企业发起申办的临床研究(IST)两大类。近年来,IIT蓬勃发展,在临床研究体系中的地位和作用日益提升。IIT具体而言主要包括基于临床问题的研究、基于科学问题的研究、基于新产品IND局限性的新药研究、基于企业考量局限性研究、细胞治疗IIT五类。其中基于临床问题的IIT最贴合临床医生。那么这类IIT该如何开展?有哪些方法可以借鉴?沈琳教授通过对几个IIT案例分析,为大家详尽解析了这一问题。沈琳教授表示,在其团队近年来发起的临床研究中,IIT占据了很大一部分。这些IIT绝大部分是基于临床实践中的问题发起,并以解决这些问题为最终目的,从而形成了一个从临床前到临床研究再回归临床前的完整闭环。因此,在进行临床研究时,临床医生应善于发挥自身优势、规避不足,明确研究目标。希望上述研究成果能为大家提供一些有价值的参考与启示。

6月

2025年6月10日~15日,北京大学消化肿瘤论坛暨中国胃肠肿瘤临床研究协作组(CGOG)第十五届年会在北京隆重举行。本次会议以“创新、精准、聚力”为宗旨,立足消化系统肿瘤的精准诊疗与转化研究,聚焦最新研究进展与方向,汇集临床实践的难点与热点。在此次大会上,沈琳教授针对以下问题进行了解答:①CGOG年会持续15届的核心生命力是什么?未来CGOG的工作重点是什么?②2025年ASCO大会上团队主导的全球首个实体瘤领域的CART随机对照临床实验引发全场关注,该研究的主要结果以及重要临床意义是什么?以及如何看待Claudin 18.2 CART治疗在胃癌领域的应用前景?③AI目前已经或即将在哪些方面改变实践?未来我们的临床与科研工作应如何积极应对这些新趋势?④在今年的ASCO年会消化肿瘤领域,中国学者11项研究入选LBA报告,北肿6项独占鳌头,团队在该领域的整体研究布局和重点攻关方向是什么?
7月

Claudin18.2(CLDN18.2)的异常表达常见于胃癌及胃食管交界处(G/GEJ)腺癌,是该侵袭性癌症的潜在治疗靶点。当前已有针对CLDN18.2的单克隆抗体获批用于G/GEJ腺癌,而抗体药物偶联物(ADC)也在该领域展现出治疗潜力。2025年7月16日,沈琳教授团队在国际顶级医学期刊Nature Medicine发表了一项研究,报告了新型CLDN18.2靶向ADC IBI343的Ⅰ期剂量递增及扩展试验结果。该研究首次验证了IBI343的安全性及初步疗效,其里程碑意义不仅在于验证了CLDN18.2作为胃癌核心靶点的价值,更通过ADC技术的革新树立了精准治疗新标杆。相信未来随着全球多中心Ⅲ期试验的进行,IBI343有望改写晚期胃癌治疗指南,为患者带来更长效、更安全的生存获益。
9月

特别值得关注的是携带非V600E BRAF突变的转移性CRC亚群,其呈现三重核心特征:独特的分子生物学特征、差异化的治疗反应谱及多样的预后结局。由于RAF激酶存在组成性二聚化特性,该类肿瘤对传统BRAF单体抑制剂疗效有限。尽管第三代BRAF抑制剂的研发为非V600E BRAF突变肿瘤的靶向治疗开辟了新可能,但目前临床证据仍显不足,CRC的最佳联合治疗策略亟需深入探索。针对非V600E BRAF突变转移性CRC的持续挑战与前沿治疗策略,北京大学肿瘤医院沈琳教授、李健教授及许婷教授受邀于ASCO Daily News针对这一问题进行权威综述。
12月

总结
纵观沈琳教授团队2025年的科研轨迹,其核心特征凸显为“临床问题导向”与“转化研究驱动”的深度融合。团队的研究布局宏大而精准:在治疗策略上,实现了从传统疗法到靶向治疗、细胞治疗及ADC药物等前沿领域的全面覆盖与重点突破;在研究方法上,大力倡导并实践基于临床问题的研究者发起研究,构建了从临床前探索到大规模随机对照试验的完整证据链。未来,随着对肿瘤异质性、免疫微环境、耐药机制等核心问题的持续深耕,以及更精准的生物标志物筛选和个体化治疗方案的优化,团队必将在推动消化系统肿瘤诊疗水平提升的征程中贡献更多开创性的力量。
- 推荐文章
