- 首页 > 正文
系统评价与荟萃分析揭示围手术期免疫联合化疗为可切除胃/胃食管结合部癌患者带来明确获益
发表时间:2026-03-07 12:06:08
近期一项发表于JNCI Cancer Spectrum的研究通过系统评价和荟萃分析系统评估了围手术期化疗联合ICIs在可切除G/GEJ癌患者中的疗效与安全性,为该治疗模式的临床应用提供了综合评估。结果表明,相比于单纯化疗,化疗联合ICIs可显著改善患者的病理学缓解率与生存结局,尤其在PD-L1阳性人群中获益更为明显,且未显著增加≥3级治疗相关不良事件(TRAEs)的发生风险。这些发现提示,化免联合疗法是一种具有前景的根治性治疗策略,为局部晚期胃癌患者的围手术期治疗提供了新的循证方向。
从治疗瓶颈到免疫新机:局部晚期胃癌围手术期疗法的演进与争议
G/GEJ癌是全球范围内发病率和死亡率均位居前列的恶性肿瘤。尽管诊断技术和治疗策略不断进展,但局部晚期患者的预后仍然较差。目前,手术切除仍是根治性治疗的主要手段,但仅接受手术治疗的患者预后不佳,近75%的患者在三年内出现复发。为改善长期疗效,围手术期化疗已成为可切除G/GEJ癌的标准治疗方案。然而,单纯化疗取得的病理完全缓解率(pCR)仍然较低(约5%~10%),长期生存效果有限。研究显示,近半数患者在三年内出现疾病进展,五年总生存(OS)率仅为36%~45%。这凸显了探索更有效治疗策略的迫切性。
近年来,ICIs在G/GEJ癌的治疗中取得重要进展。早期研究显示,其在晚期或转移性G/GEJ癌的后线治疗中,尤其是对PD-L1高表达患者具有显著疗效。随后,多项临床试验进一步证实,在晚期或复发性G/GEJ癌一线治疗中,免疫联合化疗相较于单纯化疗能显著改善患者生存。这些进展推动了免疫治疗向更早期应用拓展,当前多项研究正探索将其纳入围手术期治疗。值得注意的是,近期两项关键随机研究(KEYNOTE-585研究、MATTERHORN研究)评估了在围手术期化疗基础上联合免疫治疗的效果。两项研究均显示pCR有所提高,但在生存结局上结果不一致。KEYNOTE-585研究中,帕博利珠单抗联合化疗未能显著改善无事件生存期(EFS)和OS;而MATTERHORN研究则表明,度伐利尤单抗联合化疗可显著提高EFS和OS。这些差异提示,免疫联合化疗在围手术期治疗中的长期获益仍存在不确定性,有待进一步研究明确。
鉴于上述背景,研究人员开展了一项系统评价和荟萃分析,旨在评估新辅助或围手术期化疗联合免疫治疗在可切除G/GEJ癌患者中的生存获益、病理缓解结局及安全性特征。
综合证据揭示获益:ICIs联合化疗显著提升pCR率与生存获益,PD-L1阳性人群尤其获益且安全性可控
研究通过系统检索PubMed、Embase数据库及主要肿瘤学会议摘要,筛选出比较ICIs联合化疗与单纯化疗治疗可切除G/GEJ癌的随机对照试验。评估结局指标涵盖pCR、EFS、OS以及TRAEs,并采用固定效应模型进行荟萃分析,合并风险差(RD)与风险比(HR)。
经系统性文献回顾后,共纳入7项研究,涉及2510例G/GEJ癌患者。其中,1256例患者接受新辅助化免联合治疗,1254例患者仅接受化疗。研究包含2项Ⅲ期研究、5项Ⅱ期研究,4项可按PD-L1表达情况进行亚组分析。在ICIs使用方面,4项研究采用抗PD-1药物,3项研究采用抗PD-L1药物。
pCR率分析
本荟萃分析纳入的7项研究均报告了pCR率数据。在接受化免联合治疗的1256例患者中,221例达到pCR(17.6%),而仅接受化疗的1254例患者中,77例达到pCR(6.1%)。合并分析显示,化免联合治疗组pCR率显著更高(RD=0.11,95%CI:0.09~0.14,P<0.001)。统计学异质性较低(I2=0%)。pCR率比较的森林图见图1。
基于PD-L1表达的亚组分析显示,在PD-L1阳性亚组中,化免联合治疗组pCR率显著高于仅化疗组(19.2% vs. 6.5%,RD=0.13,95%CI:0.10~0.16,P<0.001)。相反,在PD-L1阴性亚组中,改善情况无统计学意义(11.8% vs. 6.7%,P=0.10)。这些发现表明,化免联合治疗在PD-L1阳性患者中的病理获益可能更显著。亚组分析间异质性中等(I2=51%)(图1)。

图1. pCR率风险差的森林图
其他亚组分析,包括化疗方案(双药 vs. 三药)、错配修复(MMR)状态、肿瘤位置(胃 vs. 胃食管结合部)和ICIs类型(抗PD-1 vs. 抗PD-L1),均显示化免联合治疗组pCR率始终高于仅化疗组。
EFS分析
MATTERHORN研究和KEYNOTE-585研究报告了EFS数据,可进行合并分析。在纳入的1955例患者中,与仅化疗相比,化免联合治疗与EFS显著改善相关(合并HR=0.76,95%CI:0.66~0.86,P<0.001),表明事件风险降低24%。研究间异质性低(I2=0%)(图2)。然而,这两项试验的结论不同:MATTERHORN研究达到其主要EFS终点,并显示以度伐利尤单抗为基础的化免联合治疗具有统计学显著获益;而KEYNOTE-585研究未达到统计学显著改善,仅显示以帕博利珠单抗为基础的治疗有数值上的优势趋势。
基于PD-L1表达的亚组分析显示,在PD-L1阳性亚组中,与仅化疗相比,化免联合治疗显著改善EFS(合并HR=0.74,95%CI:0.64~0.86,P<0.001)。相反,PD-L1阴性亚组未显示统计学显著差异(HR=0.84,95%CI:0.60~1.17,P=0.29)。两个亚组间异质性低(I2=0%)(图2)。由于纳入试验报告不足,未进行基于MMR状态等其他亚组的EFS分析。
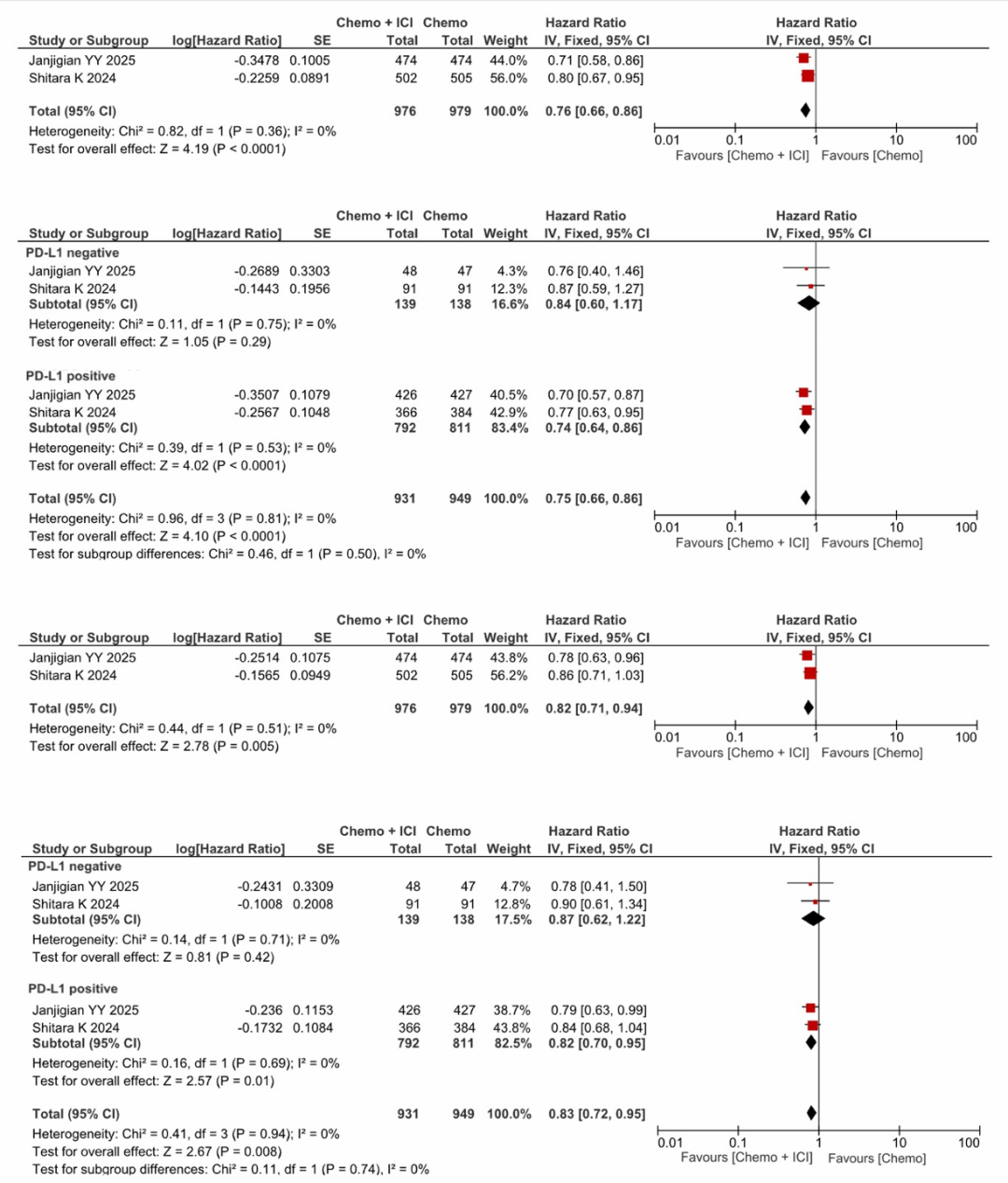
图2. 生存结局风险比的森林图
OS分析
两项研究报告了OS数据,可进行合并分析。在1955例患者中,与仅化疗相比,化免联合治疗与显著生存获益相关(HR=0.82,95%CI:0.71~0.94,P=0.005),表明死亡风险降低18%。研究间异质性低(I2=0%)(图2)。值得注意的是,这两项关键试验结果相反。最终MATTERHORN研究分析显示,度伐利尤单抗联合化疗具有统计学显著的OS优势,证实了该方法的长期生存获益。相反,KEYNOTE-585研究未达到统计学显著性,仅显示帕博利珠单抗为基础的化疗免疫治疗有适度的数值优势趋势。
在PD-L1阳性亚组中,与仅化疗相比,化疗免疫治疗与明显的OS获益相关(合并HR=0.82,95%CI:0.70~0.95,P=0.01)。相反,在PD-L1阴性亚组中未观察到显著的生存差异(HR=0.87,95%CI:0.62~1.22,P=0.71)。两个亚组间的异质性均较低(I2=0%)(图2)。由于纳入试验报告不足,未进行基于MMR状态等其他亚组的OS分析。
安全性结局
在安全性结局方面,四项研究提供了TRAEs数据(图3)。合并分析显示,化免联合治疗组与单纯化疗组的总体TRAEs发生率相近(97.2% vs. 96.8%)。然而,化免联合治疗组的≥3级TRAEs发生率较高(66.1% vs. 62.7%),但合并风险差(RD=0.04,95%CI:0.00~0.08,P=0.08)未达到统计学显著性,研究间异质性低(I2=0%)。进一步分析表明,联合免疫治疗显著增加了导致治疗中断的TRAEs发生率(25.7% vs. 19.2%,RD=0.06,95%CI:0.03~0.10,P<0.001)。在死亡结局方面,四项研究报告了全因死亡率数据。化免联合治疗组死亡发生率为4.2%(44/1039例),单纯化疗组为3.0%(31/1038例)。同时,这四项研究也报告了术后30天死亡率:化免联合治疗组为1.8%(5/272例),单纯化疗组为0.7%(2/268例)。
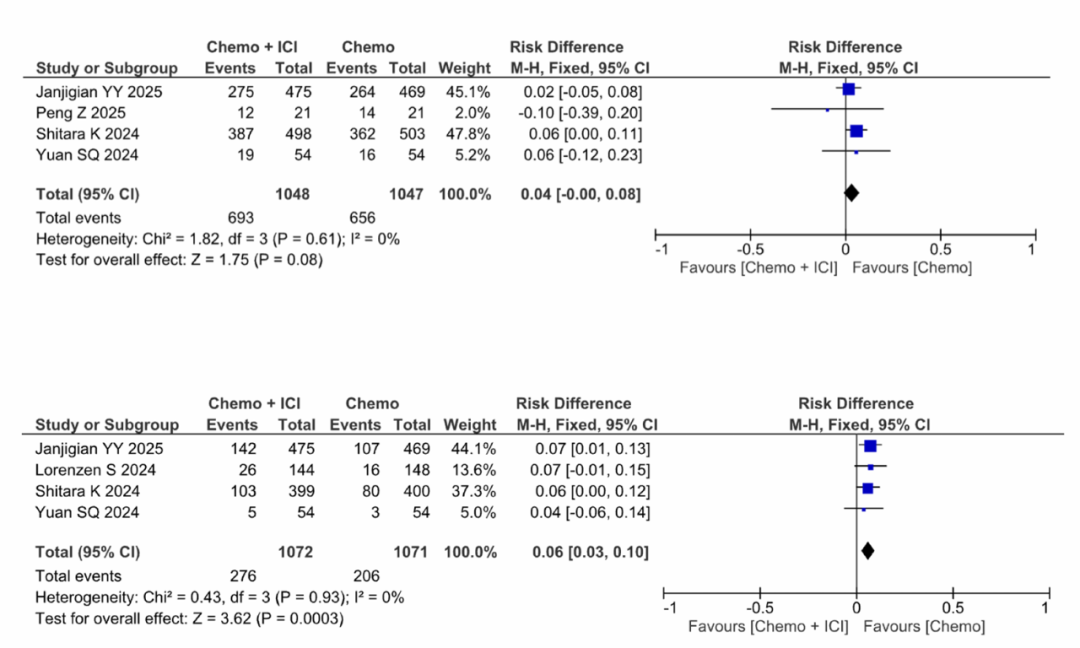
图3. 安全性结局风险差的森林图
小结
总而言之,本次荟萃分析表明,对于可切除的G/GEJ癌患者,在围手术期化疗基础上联合ICIs治疗,可改善pCR率,延长EFS和OS,且安全性可控。这些发现支持化疗免疫联合疗法作为一种根治性治疗策略的潜在作用,并强调了需要进一步收集长期生存数据以确认其临床获益。
参考文献
Reo Omori, et al. Perioperative chemoimmunotherapy for patients with gastric or gastroesophageal junction cancer: a systematic review and meta-analysis. JNCI Cancer Spectrum. 2026 Jan.- 推荐文章
