- 首页 > 正文
JCO丨许剑民教授牵头NEOTERIC研究新突破:双免新辅助治疗LARC,pCR率达35.7%!
发表时间:2026-03-07 11:12:33

NEOTERIC研究是一项随机、开放标签、平行组Ⅱ期临床试验,在中国五家医疗中心开展。符合条件的患者≥18岁,经组织学或细胞学确诊为直肠腺癌,根据RECIST v1.1标准至少有一个可测量病灶,临床分期为cT3N+M0或cT4NanyM0,且肿瘤下缘距肛缘≤10 cm。其他纳入标准包括:美国东部肿瘤协作组体能状态评分(ECOG PS)0~1分,器官功能良好,且既往未接受过直肠癌抗癌治疗。研究包含安全导入期及后续随机阶段。入组患者接受长程nCRT(总剂量45~50.4 Gy,分25~28次完成,同步口服卡培他滨),后续接受为期3个周期(每周期21天)的阿替利珠单抗治疗(Atezo,每周期第1天给药,剂量为1200 mg),其中一组联合替瑞利尤单抗治疗(Tira,剂量600 mg;即Atezo+Tira组),另一组则单独使用阿替利珠单抗(即Atezo组)。末次给药2周后进行根治性手术。研究主要终点为病理完全缓解率(pCR)。次要终点包括1年无事件生存期(EFS)及安全性。研究结果将与历史对照进行比较。
研究结果
患者特征
2022年3月18日~2023年7月6日,共筛选了71例LARC患者,其中58例入组本研究。3例患者根据“3+3”方法完成了安全导入期,接受了Atezo+Tira治疗。在后续随机化阶段,55例患者被随机分配至Atezo+Tira组(n=28)或Atezo组(n=27)。随机化阶段的所有患者均为pMMR/MSS肿瘤。基线时,两组分别有92.9%和88.9%的患者为Ⅲ期LARC。
疗效结局
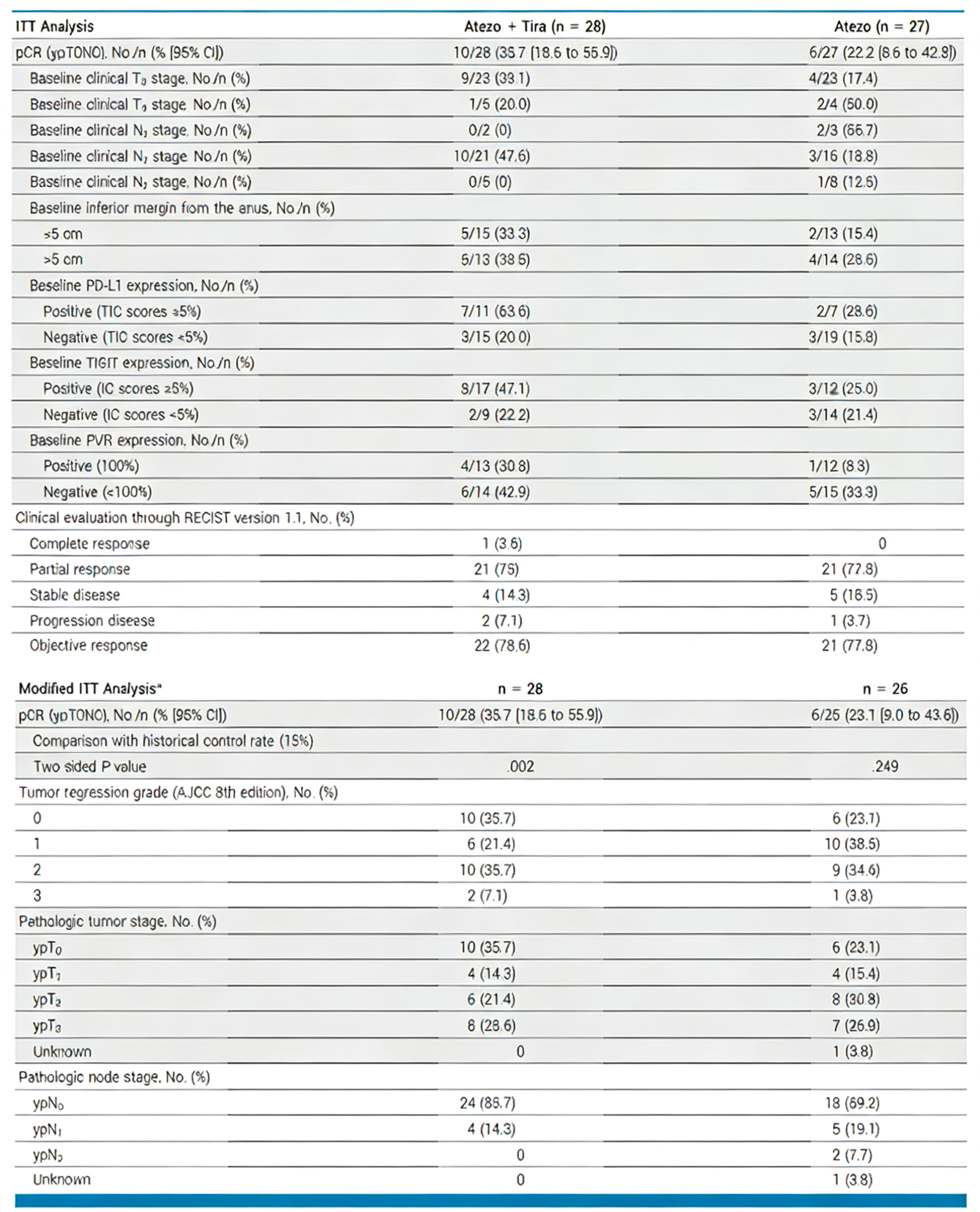
所有55例随机分组的患者均纳入意向治疗(ITT)分析集。Atezo+Tira组的pCR率为35.7%(10/28;95%CI:18.6%~55.9%),显著高于历史对照组的15%(P=0.002);Atezo组的pCR率为22.2%(6/27;95%CI:8.6%~42.3%),较历史对照组的15%有数值上的改善(P=0.293)(表1)。
改良的ITT(mITT)分析集包括所有接受手术切除的随机分组患者,用于主要终点的支持性分析以及无复发生存期(RFS)和R0切除率的汇总。Atezo组有1例患者拒绝手术,因此被排除在ITT人群之外,最终Atezo+Tira组纳入28例患者,Atezo组纳入26例患者。mITT分析显示,Atezo+Tira组pCR率仍为35.7%(P=0.002),Atezo组为23.1%(P=0.249)(表1)。Atezo+Tira组和Atezo组的R0切除率均为100%。
表1. 疗效结局
至数据截止日期(2025年1月6日),中位随访时间为21.55个月(范围:20.67~22.24个月),Atezo+Tira组和Atezo组的1年EFS率分别为96.3%(95%CI:76.5%~99.5%)和92.1%(95%CI:72.1%~98.0%)(图1)。
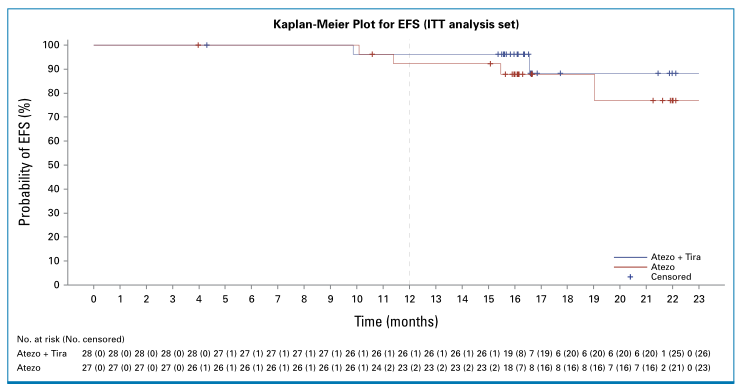
图1. EFS的Kaplan-Meier生存曲线(ITT分析集)
Atezo+Tira组的1年RFS率为96.3%(95%CI:76.5%~99.5%),Atezo组为88.1%(95%CI:67.6%~96.0%)(图2)。未发生死亡病例。
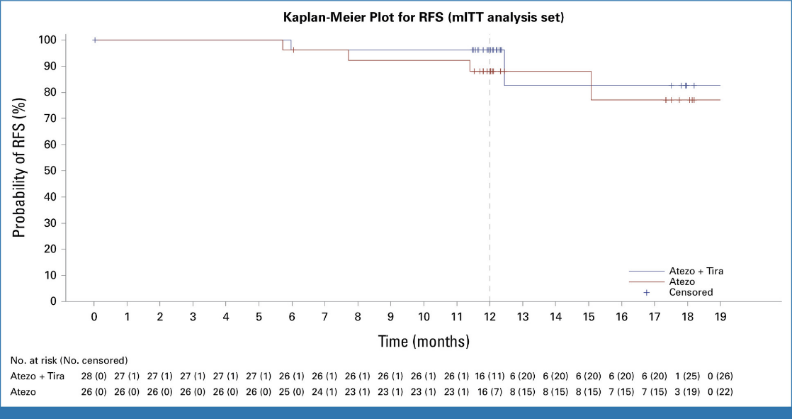
图2. RFS的Kaplan-Meier生存曲线(mITT分析集)
安全性结局
两个治疗组的所有患者均至少发生过一次治疗期间不良事件(TEAE)。表2列出了任一治疗组中发生率≥10%的任何级别的TEAE。Atezo+Tira组和Atezo单药组中分别有89.7%和80.8%的患者发生与放疗或化疗相关的TEAE。两组分别有75.9%和57.7%的患者观察到与手术相关的TEAE。两组均未报告术中手术并发症。Atezo+Tira组和Atezo单药组中分别有48.3%和61.5%的患者报告了与Atezo/Tira相关的TEAE。
表2. 任一治疗组中发生率≥10%的AE(安全性分析集)

在Atezo+Tira组中,31.0%的患者发生治疗相关的3~4级TEAE,而在Atezo单药组中,这一比例为26.9%。与放疗/化疗相关的3~4级TEAE在Atezo+Tira组中的发生率为24.1%,在Atezo单药组中为11.5%;与Atezo/Tira相关的3~4级TEAE在Atezo+Tira组中的发生率为10.3%,在Atezo单药组中为11.5%;与手术相关的3~4级TEAE在Atezo+Tira组中的发生率为17.2%,在Atezo组中为15.4%。严重TEAE的发生率分别为10.3%和7.7%,其中包括与放疗/化疗(6.9% vs. 0%)和Atezo/Tira(3.4% vs. 0%)相关的严重TEAE。
导致停药或中断治疗的TEAE发生率分别为10.3%和11.5%,主要发生在免疫治疗期间。两组均无TEAE导致的治疗终止事件发生。最常见的≥3级治疗相关不良事件为淋巴细胞计数降低(Atezo+Tira组为27.6%,Atezo组为19.2%)、天冬氨酸氨基转移酶升高(分别为3.4%和3.8%)以及高血糖(分别为3.4%和3.8%)。
研究讨论与结论
从目前数据分析,NEOTERIC研究是首个全球报道的评估nCRT后Atezo联合或不联合Tira治疗LARC患者的安全性和有效性的随机Ⅱ期临床试验。值得注意的是,Atezo+Tira组达到了主要终点,与历史数据相比,pCR率显著提高,且具有临床意义。
NEOTERIC研究中的所有患者均为pMMR/MSS肿瘤,其中90.9%属于临床Ⅲ期。既往研究表明,将免疫检查点抑制剂与长程放化疗联合作为新辅助治疗,可在pMMR/MSS患者中获得良好的pCR率。然而,由于不同研究间临床特征的异质性,此类数据需谨慎解读。在NEOTERIC研究中,患者被随机分配至Atezo+Tira组或Atezo单药组,每个治疗组均与历史对照数据独立比较。两个治疗组间的基线特征均衡可比。与历史对照相比,Atezo+Tira组显著提高了pCR率,而Atezo单药组也显示出数值上的增加,这表明双免疫治疗可能具有诱导良好病理反应的潜力。Atezo+Tira组观察到的抗肿瘤疗效增强,可能归因于放化疗的免疫调节效应,其促进了更高的免疫活性微环境。放疗可能通过增加肿瘤免疫原性、刺激抗原特异性CD8+T细胞反应以及上调肿瘤微环境中肿瘤浸润性淋巴细胞上的PD-L1表达,从而增强难治性肿瘤对PD-1/PD-L1阻断的应答。
在本研究中,虽然Atezo+Tira组的1年RFS率为96.3%,Atezo单药组为88.1%,但仍需继续随访以进一步评估pCR与长期无复发生存之间的关联。此外,REAL研究证实,与传统腹腔镜手术相比,机器人手术与中低位直肠癌患者长期肿瘤学结局的显著改善相关。在NEOTERIC研究中,Atezo+Tira组和Atezo单药组分别有55.2%和50.0%的患者接受了机器人手术,这可能有助于获得良好的长期生存结局。本研究的目标是肿瘤降期,达到pCR阳性结局可能提供具有临床意义的信息。
NEOTERIC研究的方案于2021年2月获得批准。符合条件的患者为可切除的LARC(cT3N+M0或cT4NanyM0)患者,研究重点在于肿瘤降期而非器官保留。由于完全新辅助治疗涉及额外的化疗周期并延长放疗与手术的间隔时间,出于安全性考虑、患者潜在不耐受以及缩短放疗-手术间隔时间的目的,本探索性研究未采纳该模式;根据现有数据评估,这是全球首个评估nCRT后TIGIT联合PD-1/PD-L1抑制剂在LARC中疗效和安全性的随机试验。尽管跨试验比较需谨慎解读,但本研究取得了35.7%的pCR率和31.0%的≥3级TEAE发生率,表明双免疫治疗可能提供与完全新辅助治疗相当的病理反应,且安全性更佳。这种治疗方案可能代表了一种针对旨在实现肿瘤降期和R0切除的LARC患者的新辅助治疗策略。
总之,与历史对照相比,nCRT后使用Atezo+Tira显示出显著更高的pCR率,且安全性可控。这表明该联合方案可能代表一种有前景且可行的LARC患者治疗策略。
参考文献:
[1]Tang W, et al. J Clin Oncol. 2026 Jan 13:JCO2501883.- 推荐文章
