- 首页 > 正文
国产双抗Anbenitamab为HER2阳性胃癌后线治疗带来新希望:Ⅲ期KC-WISE研究的预设中期分析结果
发表时间:2026-03-07 12:58:37

困局拓新:HER2阳性晚期胃癌的后线治疗挑战与双抗破局
胃癌是全球范围内常见的恶性肿瘤之一,在我国其发病率和死亡率尤为突出。中国人口基数庞大,胃癌病例约占全球总数的44%,且患者生存率相对较低,使其成为一项严峻的公共卫生挑战。晚期或转移性胃癌患者的预后较差,五年总OS率仅为5%~20%,中位OS约为1~2年,具体生存结局在很大程度上取决于其生物标志物特征。
在胃癌中,约15%~20%的患者存在HER2过表达。目前,针对HER2阳性晚期胃癌的一线标准治疗方案为化疗联合曲妥珠单抗,该方案已显著改善患者生存。然而,患者在接受一线含曲妥珠单抗方案治疗发生进展后,后续治疗选择十分有限。尽管新型抗体偶联药物(如德曲妥珠单抗)为后线治疗带来了新的希望,但针对中国患者群体探索更优治疗策略,尤其是基于本土研发的创新疗法,对突破当前治疗瓶颈、改善患者生存具有重要意义。
Anbenitamab是一种新型双特异性抗体,可同时结合HER2的两个不同表位,涵盖曲妥珠单抗(靶向胞外域Ⅳ)和帕妥珠单抗(靶向胞外域Ⅱ)的作用区域,为克服曲妥珠单抗耐药提供了全新机制。虽然曲妥珠单抗联合帕妥珠单抗在HER2阳性晚期胃癌中未能显著改善生存,但Anbenitamab展现出对HER2信号通路更全面的抑制作用。一项Ⅱ期研究显示,Anbenitamab联合化疗二线治疗HER2阳性转移性胃癌中表现出良好疗效。作为一种在中国自主研发的创新药物,其未来若获批上市,将有望填补曲妥珠单抗治疗后对高效治疗的明确未满足需求。
在此背景下,中国人民解放军总医院徐建明教授团队牵头开展了多中心、随机、双盲、Ⅲ期KC-WISE研究。该研究旨在评估Anbenitamab联合化疗在接受含曲妥珠单抗方案治疗失败的HER2阳性晚期GC/GEJ腺癌患者中的安全性和有效性。
多维突破:Anbenitamab联合化疗带来PFS与OS双重获益、肿瘤应答提升且安全性总体可控
KC-WISE研究在中国51家医院开展。研究纳入既往接受含曲妥珠单抗方案治疗后进展的HER2阳性GC/GEJ腺癌患者,并按1:1比例随机分配至试验组或对照组:试验组接受Anbenitamab(30 mg/kg,每3周1次)联合化疗(紫杉醇/多西他赛/伊立替康),对照组则接受安慰剂联合相同化疗方案。分层因素包括化疗类型、HER2表达状态(免疫组化[IHC]3+或IHC 2+/荧光原位杂交[FISH]+)及既往治疗线数(1线或≥2线)。治疗持续至疾病进展、不可耐受毒性或退出。主要研究终点为独立评审委员会(IRC)评估的意向性治疗人群的PFS和OS。本中期分析计划在观察到约120例PFS事件时进行。
研究共纳入188例患者(Anbenitamab组95例,对照组93例),两组基线人口统计学和疾病特征均衡。Anbenitamab组中位随访时间为9.7个月,对照组为9.8个月。
PFS显著改善,亚组获益广泛:经IRC评估,Anbenitamab组中位PFS达到7.1个月,显著优于对照组的2.7个月,使疾病进展或死亡风险降低75%(HR=0.25,95%CI:0.17~0.39,P<0.0001)(图1A),其6、9、12个月预估PFS率分别为54%、39%和24%,均显著高于对照组(12%、4%和0%)。研究者评估的PFS结果与此一致(HR=0.23,95%CI:0.15~0.35,P<0.0001)(图1B)。值得注意的是,在既往仅接受过1线治疗的患者(N=157)中,联合治疗亦显著延长中位PFS(7.1 vs. 2.8个月,HR=0.29)。除IHC 2+/FISH+亚组外,各预设亚组分析均支持这一获益趋势(图2A)。
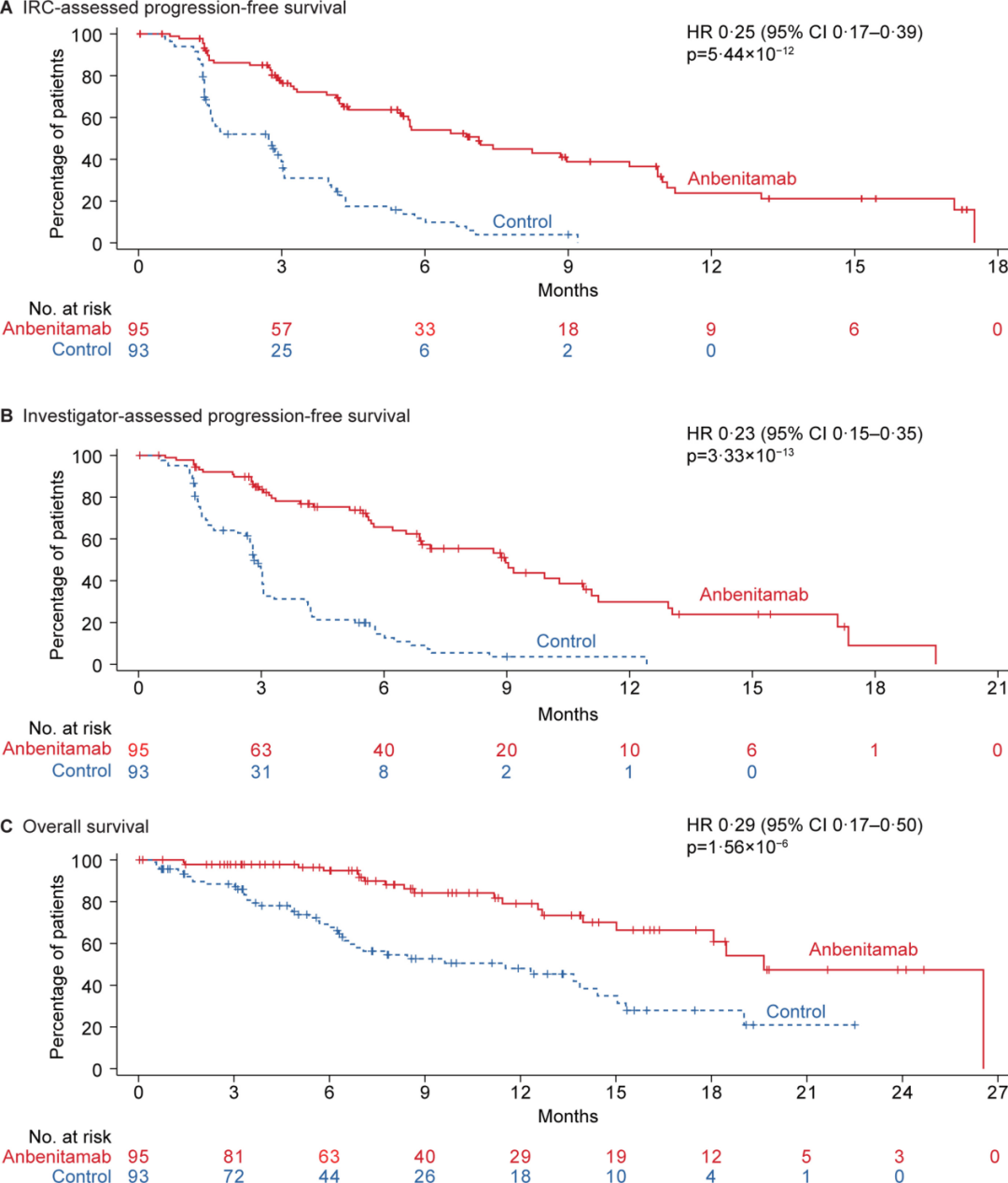
图1. PFS与OS的Kaplan-Meier分析(意向性治疗分析集):(A)由IRC评估的PFS;(B)由研究者评估的PFS;(C)OS
OS显著延长,生存获益明确:在OS方面,Anbenitamab组中位OS达19.6个月,较对照组的11.5个月显著延长,使死亡风险降低71%(HR=0.29,95%CI:0.17~0.50,P<0.0001)(图1C),其15、18、24个月的预估OS率分别为70%、66%和47%,明显优于对照组的35%、28%及不可评估(NE)。各亚组分析显示OS获益具有普遍一致性(图2B)。
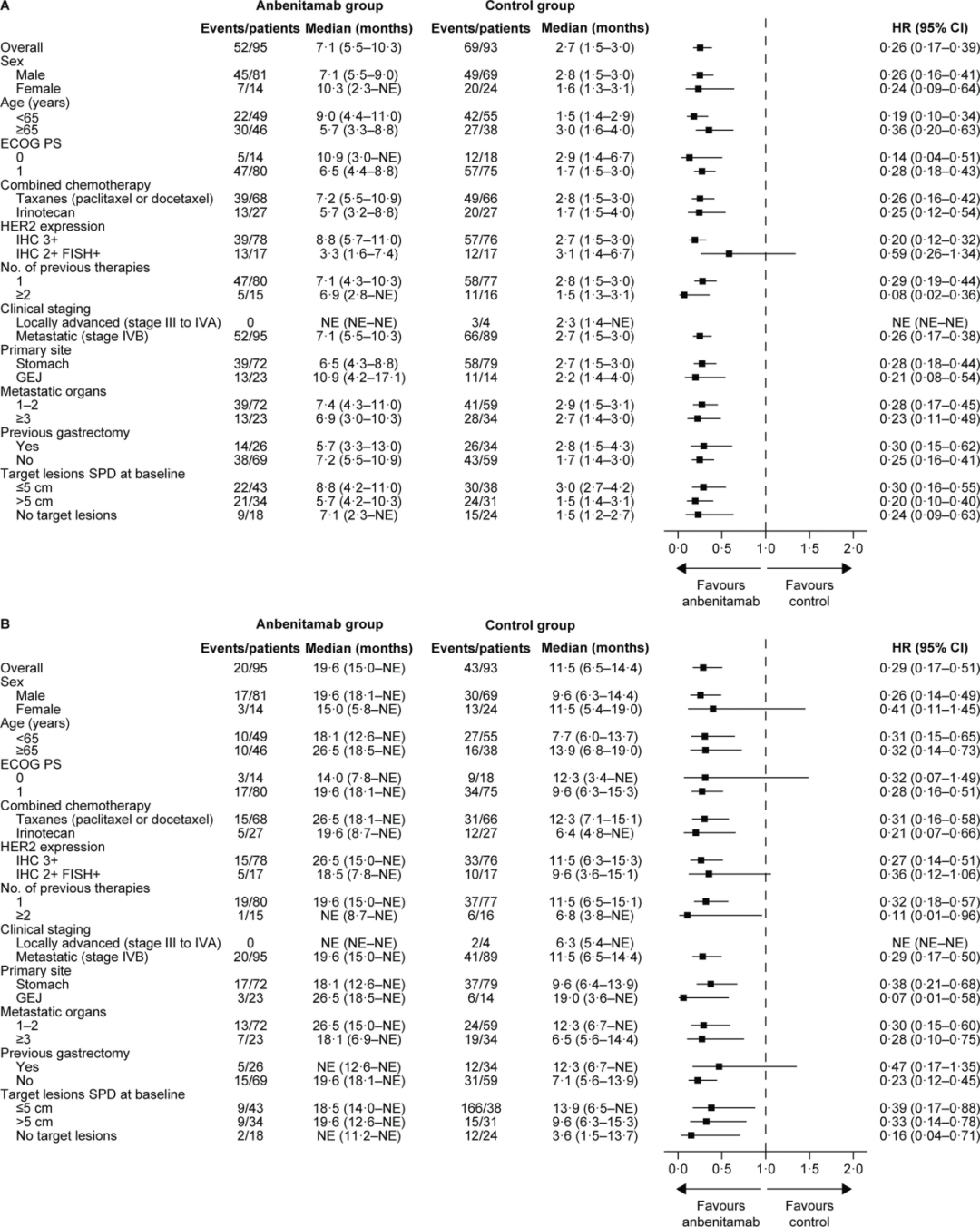
图2. PFS和OS的亚组分析:(A)由IRC评估的的预设亚组中的PFS;(B)预设亚组中的OS
肿瘤应答提升,缓解更为持久:此外,Anbenitamab联合化疗显著提升了肿瘤应答:IRC评估的客观缓解率(ORR,56% vs. 11%)和疾病控制率(DCR,80% vs. 42%)均优于单纯化疗,研究者评估结果与之吻合。Anbenitamab联合化疗的中位缓解持续时间(DOR)达8.2个月,较对照组(2.9个月)亦显著延长。
安全性总体可控:Anbenitamab组对比化疗组的≥3级治疗相关不良事件发生率分别为60%和45%,最常见的包括中性粒细胞减少(30% vs. 22%)、白细胞减少(21% vs. 25%)和贫血(18% vs. 11%);两组严重治疗相关不良事件发生率分别为26%和23%。虽然Anbenitamab组组因不良事件导致的剂量调整(44% vs. 31%)、治疗中断(45% vs. 32%)及停药(11% vs. 2%)比例较高,但无治疗相关死亡发生,对照组有5例(5%)死亡,其中1例死于多器官功能障碍综合征,4例死因不明。
小结
Ⅲ期KC-WISE研究预设中期分析结果显示,对于既往接受含曲妥珠单抗方案治疗失败的HER2阳性GC/GEJ腺癌患者,与单纯化疗相比,Anbenitamab联合化疗可显著改善PFS、OS和ORR,获益幅度具有明确临床意义。这些积极结果以及良好的安全性特征表明,Anbenitamab联合化疗有望成为该人群极具前景的后线治疗新选择。该研究不仅验证了这一国产双特异性抗体的治疗潜力,也为后续开展与现有标准治疗方案的头对头对比研究奠定了扎实基础。未来,随着更长期随访数据的积累以及其在更广泛人群中的进一步探索,Anbenitamab有望为HER2阳性胃癌的治疗格局带来重要变革。
- 推荐文章
