- 首页 > 正文
ctDNA作为早期临床研究的生物标志物:现状、挑战与未来展望
发表时间:2026-03-07 09:41:37
随着分子生物标志物与精准医疗的深度融合,新型癌症疗法的临床研发进程正快速演进。循环肿瘤DNA(ctDNA)作为一种多功能工具,可用于检测可靶向的基因改变、预测治疗反应、监测肿瘤演变,并揭示药代动力学与药效学特征。其应用有望加速早期药物研发进程,深化对治疗反应与耐药性生物学驱动机制的理解。对此,研究人员系统阐述了ctDNA作为多功能生物标志物在早期临床研究中的当前应用、未来前景及面临的挑战[1]。
ctDNA在早期临床研究中的当前应用
基于分子生物标志物进行患者筛选
ctDNA分析正日益成为精准筛选临床研究患者的关键工具。该方法通过识别可干预的基因组改变,将患者与合理的在研治疗方案相匹配,从而富集更可能获益的研究人群,提升研究质量。
基于基线肿瘤分数进行分层
肿瘤分数(TF),即ctDNA中源自肿瘤细胞的比例,已逐渐成为早期临床研究中的预后生物标志物。在各种肿瘤类型和治疗类别中,较高的基线TF与较低的客观缓解率(ORR)、较短的无进展生存期(PFS)和总生存期(OS)相关。这些关联表明,TF可作为疾病负荷的替代指标,反映肿瘤的侵袭性或治疗耐药性。但要将TF广泛用作分层或富集生物标志物,仍需建立标准化界值并实现跨平台检测的一致化。
治疗反应监测
在早期临床研究中,ctDNA动力学已成为监测临床疗效的敏感生物标志物。其半衰期短,能动态追踪肿瘤负荷,且常早于影像学变化。多项靶向治疗Ⅰ期研究均证实,ctDNA分子反应(ctDNA平均变异等位基因频率比降低≥50%)与RECIST疗效评估及更长的PFS具有一致性。除预后评估外,ctDNA分析还有助于区分免疫治疗中真正的疾病进展与假性进展这一关键诊断难题。需注意的是,基于ctDNA指导治疗时须确保检测特异性,建议通过白细胞匹配测序排除克隆性造血变异,并采用正交验证及生物信息学过滤以提高结果可靠性。若无临床或影像学进展,不应仅依据ctDNA阳性改变治疗方案,而应结合系列ctDNA与定期影像进行综合监测。目前,仅依靠ctDNA调整治疗仍属探索性范畴,需前瞻性研究进一步验证。
阐明药效学效应
在早期临床研究中,ctDNA检测可通过确认药物作用机制及界定生物学有效剂量,为药效学评估提供重要依据。通过连续血浆采样,能够动态追踪TF及等位基因变异频率(VAF)的变化,从而反映治疗过程中的分子水平响应。例如,在使用PI3K抑制剂治疗后,若PIK3CA基因的VAF水平下降,通常表明药物有效作用于靶点并促使肿瘤退缩;而稳定或上升的水平则提示通路抑制不足或已产生耐药。
治疗耐药及克隆演化的动态监测
连续的ctDNA评估可在影像学证据出现之前预测疾病进展。在一项涉及39例接受靶向治疗的晚期实体瘤患者的前瞻性研究中,VAF的升高比影像学检查中位提前63天预测疾病进展。纵向ctDNA分析还能揭示克隆演化,包括原始克隆的抑制及耐药亚克隆的出现,反映了治疗压力下的肿瘤演化过程。肿瘤不知情ctDNA分析可广泛检测耐药性改变,包括新发突变、拷贝数增加和基因融合等可能被组织活检遗漏的改变。通过实时捕获这些耐药事件,ctDNA可为治疗调整及后续治疗方案选择提供依据。
毒性监测
ctDNA分析也可作为治疗相关毒性的早期预警指标。在抗体药物偶联物诱导的间质性肺病患者中,组织特异性甲基化分析检测到了肺源性ctDNA。这些发现表明,ctDNA可揭示毒性的早期分子信号,从而实现主动干预并加强安全性监测,这对于尚未充分了解新型药物全面不良反应谱的早期临床研究尤为宝贵。
ctDNA在早期临床研究中的未来应用
联合治疗研究
开发新型联合疗法的一个主要挑战在于明确各药物对疗效的具体贡献。通过比较联合疗法与其单一组分在ctDNA分子应答上的差异,可初步评估药物间是否存在叠加或协同效应,为早期研发决策提供依据。除识别单一改变外,ctDNA还能揭示共存突变和耐药通路,为合理的联合方案设计提供信息。例如,对同时存在驱动突变和耐药突变的肿瘤,双重靶向治疗可能带来临床获益;而随时间监测VAF可指导添加相应药物以对抗出现的克隆。相较于难以连续进行的组织活检,ctDNA提供了一种实时、无创的基因组监测手段,既支持适应性临床研究设计,也有助于制定逆转耐药的个体化治疗策略。
通过整合ctDNA克服RECIST标准局限性
ctDNA可作为疗效评估的补充手段,尤其适用于RECIST判定为疾病稳定的患者,其影像学变化常不明显或延迟。通过将基于ctDNA的指标与常规影像学检查相结合,研究人员能够更动态、更精细地理解抗肿瘤活性和药效学作用。展望未来,连续的ctDNA监测有望减少对横断面影像学的依赖,实现更早期的治疗疗效评估,并拓宽研究入组标准,纳入无明显可测量病灶的患者。然而,广泛的临床整合仍需要统一ctDNA疗效评价标准,在不同瘤种中进行验证,并与监管审批终点达成协调。
剂量优化与监管决策
在Ⅰ期临床研究中,连续的ctDNA动力学数据结合安全性、药代动力学/药效学及疗效数据,有助于确定生物学有效剂量。这一思路与美国食品药品监督管理局(FDA)“Project Optimus”的宗旨一致,即强调基于整体证据而非仅依据最大耐受剂量来选择剂量。一项研究显示,生物有效剂量下的ctDNA分子反应与RECIST评估结果及PFS具有相关性,可为确定和建立Ⅱ期临床研究推荐剂量提供依据。
ctDNA应用的现有局限性与未来改进方向
尽管ctDNA技术已取得重大进展,但仍有几个关键领域需要完善,以充分发挥其在早期临床研究中的应用价值。
克服灵敏度限制
ctDNA在早期研究中广泛应用面临的一个主要障碍是其在各瘤种间检测灵敏度的差异。许多实体瘤仅释放少量ctDNA进入循环,限制了评估的准确性。为克服这一挑战,业界正致力于通过新方法提高检测灵敏度,例如使用可减缓ctDNA从外周循环中清除的“启动剂”;新一代的、更具针对性的微小残留病灶(MRD)检测技术的进步已提高了基线ctDNA检出率,从而扩大了适合进行分子反应监测的患者人群;此外,优化计算工具,并将ctDNA与互补性循环生物标志物(如循环肿瘤细胞、外泌体和游离RNA)整合,可为评估肿瘤反应提供更稳健和全面的策略。
明确检测限:整合TF与检测灵敏度
对于肿瘤未知样本检测,TF≥1%是可靠分子评估的实用阈值,其与组织基因分型一致性高,可稳健检出临床相关变异。此范围内,0.5%的95%检测限足以捕获主要突变和耐药事件。然而,治疗过程中若ctDNA负荷降低,TF和VAF可能会降至此阈值以下,此时需要检测限≤0.01%的更灵敏检测方法来识别早期分子反应。虽然低基线TF(<1%)与良好预后相关,但对此类患者群体进行分子反应评估的效用仍需进一步研究。
技术与分析壁垒
除了技术灵敏度,ctDNA的应用还面临显著的分析可变性。主要障碍在于分析前、中、后各阶段缺乏标准化。样本采集、制备、处理、测序及生物信息学分析流程中的差异会导致检测性能出现重大偏差,造成结果不一致且难以重复。这些差异阻碍了结果解读和跨平台比较。为提高可靠性和临床实用性,建立通用标准至关重要,包括经验证的ctDNA阈值、参考检测方法以及用于培训与数据解读的标准化框架。标准化在早期多中心研究中尤为重要,数据的可比性是研究完整性和临床转化的基础。
确定ctDNA采样的最佳时机
基于ctDNA评估的最佳时间点应根据治疗和肿瘤特异性数据来确定,目前尚无标准化方法。近期RECIST工作组指南建议早期进行治疗中ctDNA检测,指出治疗第1周期结束(约3~4周)是最具信息量的时间点。早期的ctDNA分析先于影像学反应数据出现,可支持剂量递增决策并提高研究入组效率。相反,延迟采样可能引入脱落偏倚,排除早期进展者,从而人为夸大分子反应率。为优化ctDNA应用,采样间隔应根据药物类别、作用机制和肿瘤生物学特点进行标准化和个体化设计。
肿瘤脱落的生物学变异性
肿瘤脱落因组织学类型和部位而异,直接影响ctDNA产量。低脱落性肿瘤,由于增殖率低、血管完整性或物理屏障等原因,通常释放极少量的ctDNA。这可能导致假阴性结果并降低检测灵敏度。在此类情况下,应谨慎解读ctDNA阴性结果,并可能需要采用替代策略,例如甲基化谱分析、片段组学或基于非单核苷酸变异的检测方法。
肿瘤基因组背景的挑战
大多数ctDNA检测聚焦于检测体细胞单核苷酸变异,这限制了其在突变负荷低或非典型基因组谱肿瘤中的应用。在此情况下,采用非整倍性分析、结构变异检测、片段组学或甲基化分析等替代策略可提高灵敏度,并允许在没有典型驱动突变的情况下估算TF。目前,临床获益所需的VAF阈值尚未明确,且很可能取决于变异是主干克隆还是亚克隆性质,这凸显了在更广泛的TF背景下解读VAF的重要性。尽管研究通常将可操作改变视为二元事件,但进一步分析应考虑其相对丰度及与预后的关联,因为针对次要亚克隆的治疗可能获益有限。最终,ctDNA检测可能并非普遍适用。为确保获得具有临床意义的洞察,必须谨慎选择检测方法并结合具体背景进行解读。
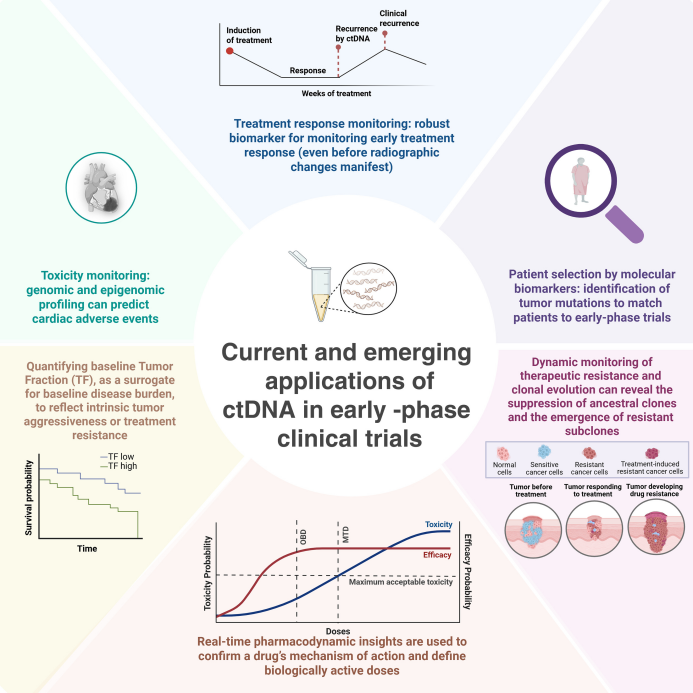
ctDNA在早期临床研究中的当前应用
在早期临床研究中,ctDNA检测已应用于患者筛选、预后分层、疗效监测、药效评估、耐药追踪及毒性预警等多个关键环节。
基于分子生物标志物进行患者筛选
ctDNA分析正日益成为精准筛选临床研究患者的关键工具。该方法通过识别可干预的基因组改变,将患者与合理的在研治疗方案相匹配,从而富集更可能获益的研究人群,提升研究质量。
基于基线肿瘤分数进行分层
肿瘤分数(TF),即ctDNA中源自肿瘤细胞的比例,已逐渐成为早期临床研究中的预后生物标志物。在各种肿瘤类型和治疗类别中,较高的基线TF与较低的客观缓解率(ORR)、较短的无进展生存期(PFS)和总生存期(OS)相关。这些关联表明,TF可作为疾病负荷的替代指标,反映肿瘤的侵袭性或治疗耐药性。但要将TF广泛用作分层或富集生物标志物,仍需建立标准化界值并实现跨平台检测的一致化。
治疗反应监测
在早期临床研究中,ctDNA动力学已成为监测临床疗效的敏感生物标志物。其半衰期短,能动态追踪肿瘤负荷,且常早于影像学变化。多项靶向治疗Ⅰ期研究均证实,ctDNA分子反应(ctDNA平均变异等位基因频率比降低≥50%)与RECIST疗效评估及更长的PFS具有一致性。除预后评估外,ctDNA分析还有助于区分免疫治疗中真正的疾病进展与假性进展这一关键诊断难题。需注意的是,基于ctDNA指导治疗时须确保检测特异性,建议通过白细胞匹配测序排除克隆性造血变异,并采用正交验证及生物信息学过滤以提高结果可靠性。若无临床或影像学进展,不应仅依据ctDNA阳性改变治疗方案,而应结合系列ctDNA与定期影像进行综合监测。目前,仅依靠ctDNA调整治疗仍属探索性范畴,需前瞻性研究进一步验证。
阐明药效学效应
在早期临床研究中,ctDNA检测可通过确认药物作用机制及界定生物学有效剂量,为药效学评估提供重要依据。通过连续血浆采样,能够动态追踪TF及等位基因变异频率(VAF)的变化,从而反映治疗过程中的分子水平响应。例如,在使用PI3K抑制剂治疗后,若PIK3CA基因的VAF水平下降,通常表明药物有效作用于靶点并促使肿瘤退缩;而稳定或上升的水平则提示通路抑制不足或已产生耐药。
治疗耐药及克隆演化的动态监测
连续的ctDNA评估可在影像学证据出现之前预测疾病进展。在一项涉及39例接受靶向治疗的晚期实体瘤患者的前瞻性研究中,VAF的升高比影像学检查中位提前63天预测疾病进展。纵向ctDNA分析还能揭示克隆演化,包括原始克隆的抑制及耐药亚克隆的出现,反映了治疗压力下的肿瘤演化过程。肿瘤不知情ctDNA分析可广泛检测耐药性改变,包括新发突变、拷贝数增加和基因融合等可能被组织活检遗漏的改变。通过实时捕获这些耐药事件,ctDNA可为治疗调整及后续治疗方案选择提供依据。
毒性监测
ctDNA分析也可作为治疗相关毒性的早期预警指标。在抗体药物偶联物诱导的间质性肺病患者中,组织特异性甲基化分析检测到了肺源性ctDNA。这些发现表明,ctDNA可揭示毒性的早期分子信号,从而实现主动干预并加强安全性监测,这对于尚未充分了解新型药物全面不良反应谱的早期临床研究尤为宝贵。
ctDNA在早期临床研究中的未来应用
联合治疗研究
开发新型联合疗法的一个主要挑战在于明确各药物对疗效的具体贡献。通过比较联合疗法与其单一组分在ctDNA分子应答上的差异,可初步评估药物间是否存在叠加或协同效应,为早期研发决策提供依据。除识别单一改变外,ctDNA还能揭示共存突变和耐药通路,为合理的联合方案设计提供信息。例如,对同时存在驱动突变和耐药突变的肿瘤,双重靶向治疗可能带来临床获益;而随时间监测VAF可指导添加相应药物以对抗出现的克隆。相较于难以连续进行的组织活检,ctDNA提供了一种实时、无创的基因组监测手段,既支持适应性临床研究设计,也有助于制定逆转耐药的个体化治疗策略。

图2. ctDNA在早期临床研究中的整合应用展望
通过整合ctDNA克服RECIST标准局限性
ctDNA可作为疗效评估的补充手段,尤其适用于RECIST判定为疾病稳定的患者,其影像学变化常不明显或延迟。通过将基于ctDNA的指标与常规影像学检查相结合,研究人员能够更动态、更精细地理解抗肿瘤活性和药效学作用。展望未来,连续的ctDNA监测有望减少对横断面影像学的依赖,实现更早期的治疗疗效评估,并拓宽研究入组标准,纳入无明显可测量病灶的患者。然而,广泛的临床整合仍需要统一ctDNA疗效评价标准,在不同瘤种中进行验证,并与监管审批终点达成协调。
剂量优化与监管决策
在Ⅰ期临床研究中,连续的ctDNA动力学数据结合安全性、药代动力学/药效学及疗效数据,有助于确定生物学有效剂量。这一思路与美国食品药品监督管理局(FDA)“Project Optimus”的宗旨一致,即强调基于整体证据而非仅依据最大耐受剂量来选择剂量。一项研究显示,生物有效剂量下的ctDNA分子反应与RECIST评估结果及PFS具有相关性,可为确定和建立Ⅱ期临床研究推荐剂量提供依据。
ctDNA应用的现有局限性与未来改进方向
尽管ctDNA技术已取得重大进展,但仍有几个关键领域需要完善,以充分发挥其在早期临床研究中的应用价值。
克服灵敏度限制
ctDNA在早期研究中广泛应用面临的一个主要障碍是其在各瘤种间检测灵敏度的差异。许多实体瘤仅释放少量ctDNA进入循环,限制了评估的准确性。为克服这一挑战,业界正致力于通过新方法提高检测灵敏度,例如使用可减缓ctDNA从外周循环中清除的“启动剂”;新一代的、更具针对性的微小残留病灶(MRD)检测技术的进步已提高了基线ctDNA检出率,从而扩大了适合进行分子反应监测的患者人群;此外,优化计算工具,并将ctDNA与互补性循环生物标志物(如循环肿瘤细胞、外泌体和游离RNA)整合,可为评估肿瘤反应提供更稳健和全面的策略。
明确检测限:整合TF与检测灵敏度
对于肿瘤未知样本检测,TF≥1%是可靠分子评估的实用阈值,其与组织基因分型一致性高,可稳健检出临床相关变异。此范围内,0.5%的95%检测限足以捕获主要突变和耐药事件。然而,治疗过程中若ctDNA负荷降低,TF和VAF可能会降至此阈值以下,此时需要检测限≤0.01%的更灵敏检测方法来识别早期分子反应。虽然低基线TF(<1%)与良好预后相关,但对此类患者群体进行分子反应评估的效用仍需进一步研究。
关键在于,必须结合解读TF和检测限:TF反映生物学的输入量,而检测限定义了分析的“地板”。高TF允许在中等检测灵敏度下实现可靠检测,而低TF则需要高灵敏度平台以避免假阴性结果。TF还进一步受到肿瘤组织学、解剖部位、检测平台及ctDNA释放动力学的影响。因此,定义TF和检测限的最佳阈值需要同时进行技术基准测试和临床背景分析。透明报告并协调这些参数对于充分实现ctDNA作为动态生物标志物的潜力至关重要。
技术与分析壁垒
除了技术灵敏度,ctDNA的应用还面临显著的分析可变性。主要障碍在于分析前、中、后各阶段缺乏标准化。样本采集、制备、处理、测序及生物信息学分析流程中的差异会导致检测性能出现重大偏差,造成结果不一致且难以重复。这些差异阻碍了结果解读和跨平台比较。为提高可靠性和临床实用性,建立通用标准至关重要,包括经验证的ctDNA阈值、参考检测方法以及用于培训与数据解读的标准化框架。标准化在早期多中心研究中尤为重要,数据的可比性是研究完整性和临床转化的基础。
确定ctDNA采样的最佳时机
基于ctDNA评估的最佳时间点应根据治疗和肿瘤特异性数据来确定,目前尚无标准化方法。近期RECIST工作组指南建议早期进行治疗中ctDNA检测,指出治疗第1周期结束(约3~4周)是最具信息量的时间点。早期的ctDNA分析先于影像学反应数据出现,可支持剂量递增决策并提高研究入组效率。相反,延迟采样可能引入脱落偏倚,排除早期进展者,从而人为夸大分子反应率。为优化ctDNA应用,采样间隔应根据药物类别、作用机制和肿瘤生物学特点进行标准化和个体化设计。
肿瘤脱落的生物学变异性
肿瘤脱落因组织学类型和部位而异,直接影响ctDNA产量。低脱落性肿瘤,由于增殖率低、血管完整性或物理屏障等原因,通常释放极少量的ctDNA。这可能导致假阴性结果并降低检测灵敏度。在此类情况下,应谨慎解读ctDNA阴性结果,并可能需要采用替代策略,例如甲基化谱分析、片段组学或基于非单核苷酸变异的检测方法。
肿瘤基因组背景的挑战
大多数ctDNA检测聚焦于检测体细胞单核苷酸变异,这限制了其在突变负荷低或非典型基因组谱肿瘤中的应用。在此情况下,采用非整倍性分析、结构变异检测、片段组学或甲基化分析等替代策略可提高灵敏度,并允许在没有典型驱动突变的情况下估算TF。目前,临床获益所需的VAF阈值尚未明确,且很可能取决于变异是主干克隆还是亚克隆性质,这凸显了在更广泛的TF背景下解读VAF的重要性。尽管研究通常将可操作改变视为二元事件,但进一步分析应考虑其相对丰度及与预后的关联,因为针对次要亚克隆的治疗可能获益有限。最终,ctDNA检测可能并非普遍适用。为确保获得具有临床意义的洞察,必须谨慎选择检测方法并结合具体背景进行解读。
小结
ctDNA正迅速成为癌症药物研发中的关键工具,其应用贯穿从首次人体试验到监管批准的全流程。在早期临床研究中,ctDNA可用于患者分子分型筛选、基线肿瘤负荷分层、以及动态监测治疗反应,同时为药效动力学研究、肿瘤演化追踪和毒性评估提供关键信息。此外,ctDNA数据还能指导合理的联合用药策略,并为监管决策提供支持。随着分析技术的标准化与验证不断完善,基于ctDNA的终点指标有望成为公认的疗效替代标志物,从而加速药物获批并降低研发风险。
总体而言,ctDNA的全面整合将推动早期临床研究向动态、个体化模式转变,实现根据患者实时分子谱进行适应性治疗,进一步促进精准肿瘤药物研发的发展。
参考文献
Tan, H. N, et al. Cancer Cell. 2025 Dec.- 推荐文章
Nature Medicine丨27万人大数据,瑞典SCREESCO试验证实开展CRC筛查能有效提升早癌检出率
英国获批!Zanidatamab为HER2高表达胆道癌患者带来精准治疗新选择
JCO重磅发表CHANCE2005/CARES-005研究!TACE联合靶免为不可切除HCC治疗带来新希望
Ann Oncol丨CheckMate 649研究5年随访结果:纳武利尤单抗联合化疗一线治疗晚期胃癌患者生存获益持久,安全性可控
心灵驿站丨当医生直面自身健康危机:在恐惧与希望交织中的探寻与顿悟
“瘤瘤”新知丨TP53状态如何左右一碳代谢相关营养素与结直肠癌风险关联的“天平”?
长期使用质子泵抑制剂真的会增加胃腺癌风险吗?近20万人随访26年的大数据给出新答案!
这几类癌症幸存者需警惕!既往肿瘤史成为影响食管鳞癌患者生存的重要因素!
《肿瘤瞭望消化时讯》给大家拜年啦!
除夕献礼!2025消化时讯十大年度热文盘点:致敬过往,共启新章
国产双抗Anbenitamab为HER2阳性胃癌后线治疗带来新希望:Ⅲ期KC-WISE研究的预设中期分析结果
JCO丨可切除及临界可切除胰腺癌围术期VTE发生率达9%,死亡风险翻倍
心灵驿站丨生死无言:一位医生与四代女性的未竟之语
JCO:JCOG0603研究长期随访结果发布,辅助mFOLFOX6未改善结直肠癌肝转移患者OS
岂有此“例”|晚期HCC能否“绝处逢生”?——肝静脉瘤栓+双肺转移患者经治生存14年的启示
JCO重磅:超600万人队列研究提示,年轻人群重度饮酒显著增加早发性胰腺癌风险
年度盘点丨胃肠研途,智领前沿——沈琳教授团队2025学术攻坚实录
系统评价与荟萃分析揭示围手术期免疫联合化疗为可切除胃/胃食管结合部癌患者带来明确获益
心灵驿站丨当医生成为生命重负的承载者:在生死交织中的坚守与思索
秦叔逵教授:2025胰腺癌诊疗进展盘点|2025肝胆胰肿瘤年终盘点暨第2届临床热词发布会
“瘤瘤”新知丨何时“动”起来最有益?研究揭示不同治疗阶段结直肠癌患者进行体力活动的“生存密码”
食管胃结合部腺癌根治术的前瞻性评估:CLAEG研究带来的真实世界见解
1/3的癌症可以预防!这份科学防癌行动清单要收藏丨世界癌症日
STTT丨文天夫教授团队合作取得新进展:仑伐替尼+经肝动脉化疗栓塞+PD-1单抗三联转化治疗可显著提高不可切除HCC转化手术率
mFOLFOXIRI联合帕尼单抗一线治疗不可切除RAS/BRAF野生型转移性结直肠癌:Ⅲ期TRIPLETE研究的最终结果
喜报!爱思唯尔2025年度“中国高被引学者”榜单揭晓,肿瘤领域百余位专家入选
惕这6类“促癌食物”,你可能每天都在吃!
最新研究揭示晚期HCC患者系统治疗模式的演变与生存现状
心灵驿站丨当医生成为临终患者见证者:一场身份交织下的感悟与思索
JCO丨许剑民教授牵头NEOTERIC研究新突破:双免新辅助治疗LARC,pCR率达35.7%!
最新研究显示新辅助放化疗联合手术与术后辅助放化疗在局部晚期食管鳞癌患者中的长期生存结局相当,个体化精准决策是关键
岂有此“例”|警报未解除:一例EOCRC患者根治术后11年罕见复发带来的长期随访启示
早期单发HCC一线治疗再评估:TACE联合放疗的获益人群和最佳时机
国之脊梁,风范永存:沉痛送别中国肿瘤内科学奠基人孙燕院士
ASCO GI现场|HCC术后辅助治疗受挫:KEYNOTE-937研究RFS结果阴性
ASCO GI国际视角|肝癌治疗进展速递:两项研究同证免疫联合方案治疗获益
ASCO GI大咖点评|陈功教授解读BREAKWATER研究:Encorafenib+西妥昔单抗+FOLFIRI方案一线治疗BRAF V600E突变型mCRC结局更优
ASCO GI中国之声|林榕波教授团队:替雷利珠单抗联合多药化疗治疗晚期胃癌的前沿进展
ASCO GI现场直击|国际视角:真实世界研究数据证实肝移植在不可切除结直肠癌肝转移治疗中的潜力
APTNM新分期:肿瘤标志物联合TNM分期,实现肝癌手术预后精准分层
“瘤瘤”新知丨警惕!溃疡性结肠炎伴背景黏膜炎症竟是结直肠癌患者不良预后“警报器”
ASCO GI现场直击|国际视角:精准医疗时代下的MRD检测新进展
ASCO GI中国之声|王峰教授:呋喹替尼联合特瑞普利单抗及SOX一线治疗晚期胃癌的数据更新
ASCO GI中国之声丨崔玖洁医生解读ALTER-PA-001研究:靶免联合一线治疗mPC,ORR达40%!
ASCO GI热评|可切除胃癌全程新辅助治疗显现潜力,聂润聪副主任医师解读CRITICS-Ⅱ研究
首项头对头随机研究揭示ESD vs. TAMIS治疗早期直肠肿瘤,ESD更具综合优势
ASCO GI大咖点评|李恩孝教授解读:两项亚洲研究聚焦免疫联合化疗(GCD)方案,全方位优化晚期BTC治疗策略
ctDNA作为早期临床研究的生物标志物:现状、挑战与未来展望
ASCO GI中国之声|胰腺癌治疗新路径:天肿两项Ⅱ期研究公布CLDN18.2联合疗法新数据
ASCO GI热点追踪|Ⅲ期COMMIT研究证实靶免化三联方案一线治治疗dMMR/MSI-H型mCRC患者,PFS显著优于免疫单药
ASCO GI中国之声|聂润聪副主任医师解读CAPITAL研究:SOX辅助治疗对比S-1改善Ⅱ~Ⅲ期胃癌长期生存
ASCO GI|可切除胃癌新辅助治疗策略探索:化疗序贯放化疗方案综合获益更优
ASCO GI热点追踪丨新方案,新突破:免疫联合PARP抑制剂在DDR突变型转移性胰腺癌中初显潜力
岂有此“例”|新辅助免疫治疗实现pCR:dMMR/MSI-H转移性结直肠癌的突破性病例分享
ASCO GI现场直击|魏嘉教授解读TERRIFIC研究:免疫联合放化疗在局晚期胃癌中显示出疗效获益
