- 首页 > 正文
“瘤瘤”新知丨警惕!溃疡性结肠炎伴背景黏膜炎症竟是结直肠癌患者不良预后“警报器”
发表时间:2026-03-07 10:22:01
引 言
随着药物治疗的不断进步,溃疡性结肠炎(UC)日益被视为一种长期持续的慢性疾病。据报道,其进展为结直肠癌(CRC)的风险也相应增加。近期研究显示,与普通人群相比,UC患者发生CRC的风险高出1.66倍,癌症相关死亡率亦高出1.59倍。此外,一项来自荷兰的全国性研究表明,在接受结直肠切除术的UC患者中,CRC的发病率从1991年的11.3%显著上升至2020年的22.8%。这些发现支持了UC中的慢性炎症可能为CRC的发展奠定基础的假设,并强调了CRC仍然是直接影响UC患者预后的重大临床问题这一事实。
UC患者发生CRC的风险很大程度上受到背景黏膜炎症的存在及其严重程度的影响。既往研究已证实,全结肠炎以及结肠炎的严重程度是CRC发生的主要风险因素。此外,越来越多的证据表明,适当控制背景黏膜炎症或许能够降低癌变风险。然而,尽管炎症通常被认为会促进肿瘤生长与进展,但背景黏膜炎症对UC患者CRC肿瘤学结局(包括预后、病理分期和组织学类型)的影响程度尚未完全阐明。
在此背景下,研究人员开展了一项回顾性研究。该研究根据肿瘤位置与癌症确诊时内镜记录的UC病变范围的相对关系,将CRC病例分为“UC累及区域内CRC”和“UC累及区域外CRC”两组,主要旨在评估背景黏膜炎症对UC合并CRC患者肿瘤学结局的影响。研究结果显示,确诊时存在的基础黏膜炎症与UC患者CRC的不良预后显著相关。在确诊癌症时进行系统的内镜评估,可能有助于预后分层,并为治疗决策提供依据。
研究一览
研究方法
本研究是一项由日本大肠癌研究会主导的全国性、多中心、回顾性队列研究,旨在探讨背景黏膜炎症对UC合并CRC患者肿瘤学预后的影响。研究纳入了1983~2020年间日本43家机构确诊的UC合并CRC患者,并回顾性收集患者临床与病理数据。
研究的核心方法是根据肿瘤与确诊时内镜所见UC炎症范围的相对位置,将CRC分为“UC病变区域内”和“UC病变区域外”两类。针对区域内病例,进一步使用梅奥内镜评分(MES)评估非肿瘤性背景黏膜的炎症严重程度,并将其分为非活动性(MES:0)、轻-中度(MES:1~2)、重度(MES:3)三组,而UC病变区域外病例不进行此评分。研究的主要终点是5年无复发生存率(RFS),次要终点是5年癌症特异性生存率(CSS)。
研究结果
在1983~2020年间,共有1189例UC患者被确诊为CRC。经过筛选,排除经手术或内镜切除后诊断为0期CRC的患者,以及缺乏肿瘤分期、诊断日期或UC病变范围信息的患者后,最终纳入723例患者进行分析。其中,683例患者被归为“UC病变区域内”组,40例归为“UC病变区域外”组。
在“UC病变区域内”组中,根据癌症诊断时的炎症活动程度分类:非活动性占88例,轻中度占389例,重度占28例。另有178例患者无MES记录,未纳入与炎症活动程度相关的分析。从治疗(手术或内镜切除)或诊断(未切除病例)开始的中位随访时间为51个月。在CSS分析中,排除了1例缺乏死亡原因信息的“UC病变区域内”组患者。
两组患者的基线特征存在显著差异。“UC病变区域内”组患者平均年龄显著更小(51.8岁 vs. 61.1岁,P<0.001)。UC病变范围的分布也有显著差异(P<0.001):广泛性结肠炎在“区域内”组中占81.3%,而“区域外”组中左侧结肠炎和直肠炎合计占87.5%。
在肿瘤特征方面,肿瘤位置分布差异显著:“区域外”组中右侧结肠癌的比例显著更高(75.0% vs. 16.8%),而“区域内”组中左侧结肠癌(42.2% vs. 22.5%)和直肠癌(40.3% vs. 2.5%)更常见(P<0.001)。在组织学类型上,“区域内”组的低分化腺癌(Por)、黏液腺癌(Muc)和印戒细胞癌(Sig)发生率显著更高(23.3% vs. 10.0%,P=0.019)。
然而,在UC药物治疗史、多发病灶的存在、病理分期分布、R0切除率、CRC一级家族史或手术年份方面,两组间未观察到显著差异。在治疗方式上,两组差异显著:“区域内”组86.3%的患者接受了全结肠切除术,而“区域外”组接受全结肠切除术和部分结肠切除术的比例分别为37.5%和52.5%(P<0.001)。
无复发生存率分析与“UC病变区域外”组相比,“UC病变区域内”组的5年RFS率显著更低(75.1% vs. 87.6%,P=0.022)(图1A)。这种预后差异在所有病理分期(Ⅰ~Ⅳ期)中均持续存在(图2)。
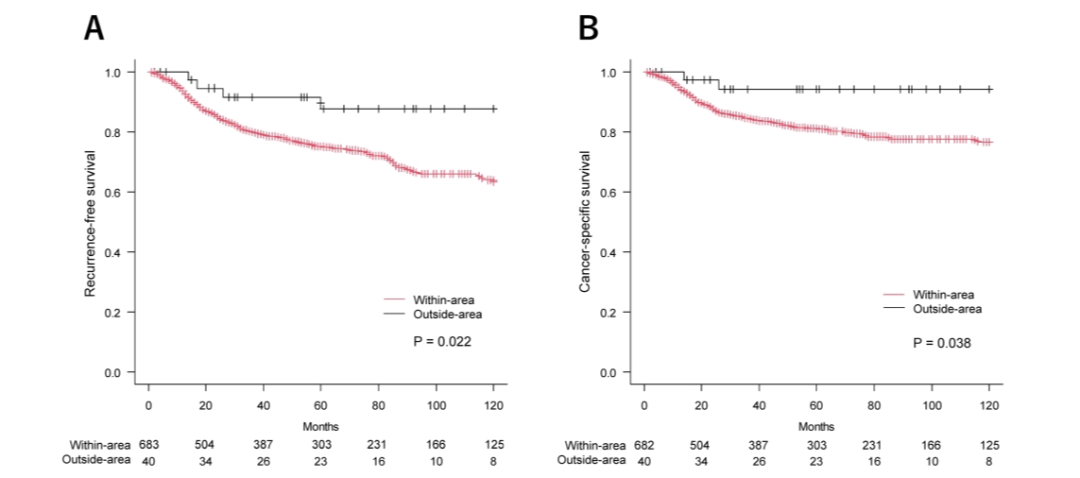
图1. 根据肿瘤相对位置(区域内 vs. 区域外)绘制的Kaplan-Meier生存曲线:(A)RFS;(B)CCS
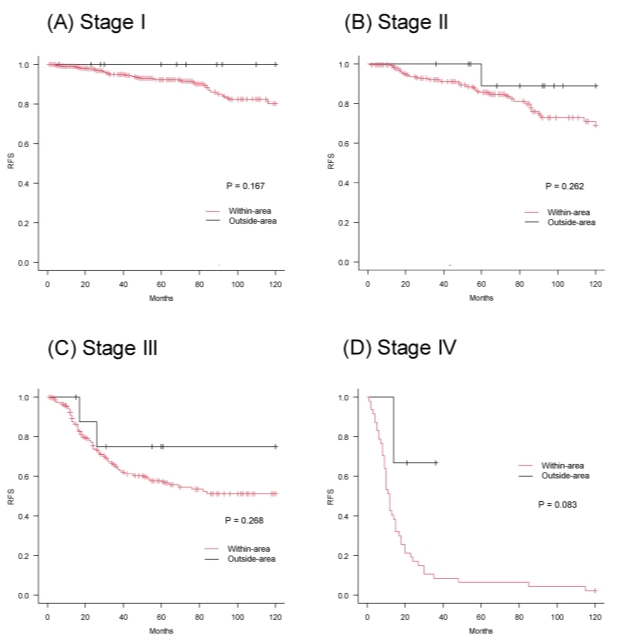
图2. 按病理分期(Ⅰ~Ⅳ期)绘制的两组RFS Kaplan-Meier曲线
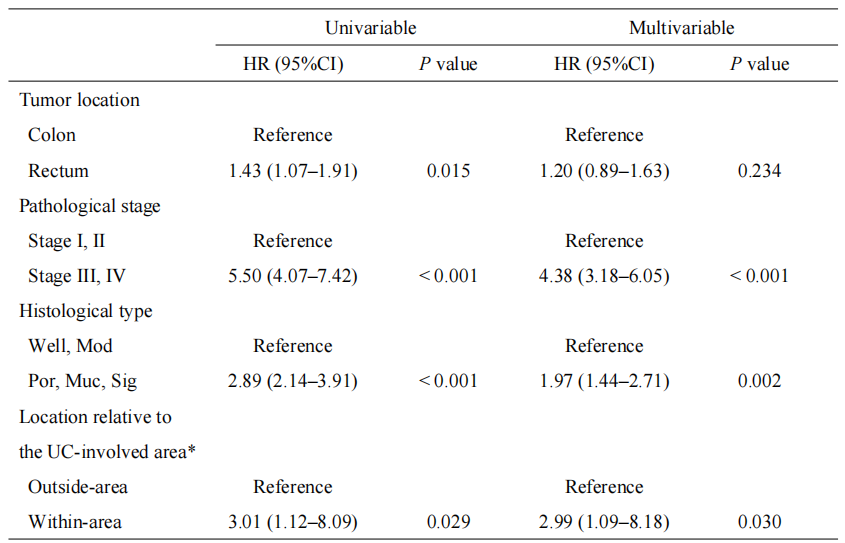
进一步的Cox回归分析显示,在单变量分析中,“区域内”分组与较差的RFS显著相关(HR=3.01,95%CI:1.12~8.09,P=0.029)。在调整了病理分期和组织学类型等预设协变量后的多变量分析中,“区域内”分组(vs. 区域外)仍是独立的预后不良因素(HR=2.99,95%CI:1.09~8.18,P=0.030)(表1)。
表1.影响RFS的多变量Cox回归分析
癌症特异性生存率分析
“UC病变区域内”组的5年CSS率同样显著低于“区域外”组(81.1% vs. 94.3%,P=0.038)(图1B)。在所有病理分期中,“区域内”组的CSS率也持续表现出更差的趋势(图3)。
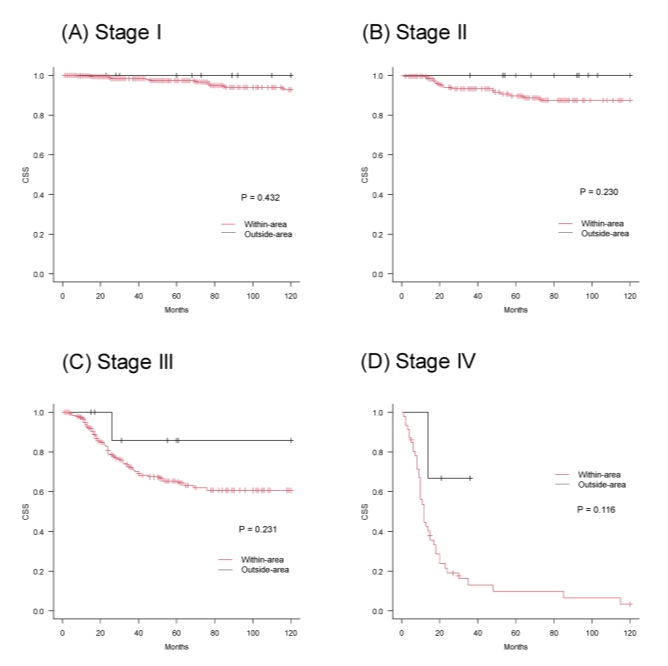
图3. 按病理分期(Ⅰ~Ⅳ期)划分的两组CSS Kaplan-Meier曲线
背景黏膜炎症严重程度与预后的关联
在“UC病变区域内”患者中,根据MES进行分层分析发现,RFS率随着炎症严重程度增加呈下降趋势(非活动性:84.4%,轻-中度:79.4%,重度:73.8%,P=0.150),但差异未达到统计学显著性(图4)。在CSS分析中,观察到了类似的梯度变化,且具有统计学显著性,重度炎症组预后明显更差(非活动性:89.0%,轻-中度:84.8%,重度:73.8%,P=0.048)(图5)。
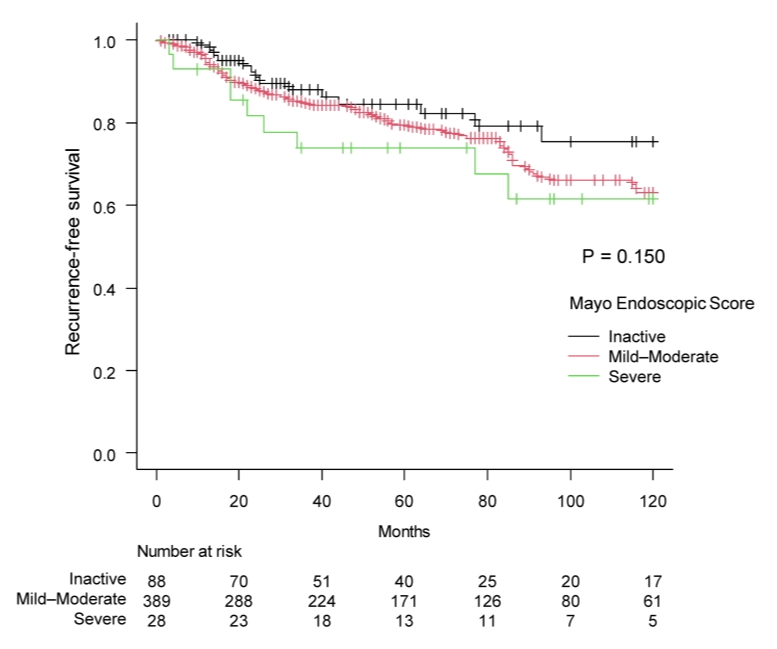
图4. 区域内病例按MES分层的RFS Kaplan-Meier曲线
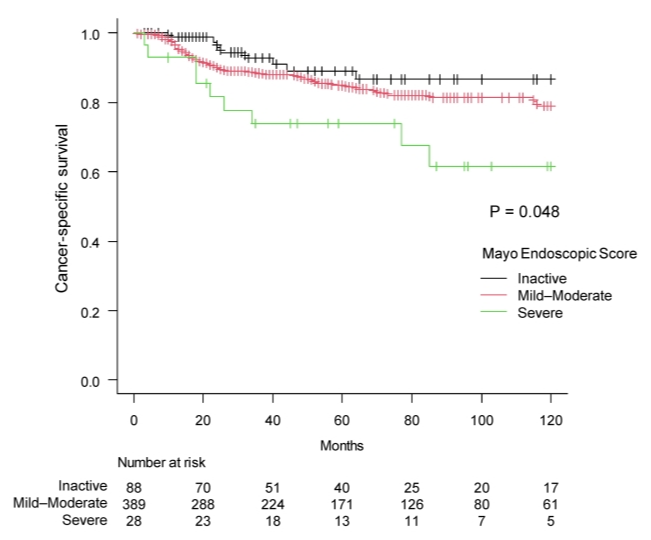
图5. 区域内病例按MES分层的CSS Kaplan-Meier曲线
此外,补充分析比较了非活动性炎症(MES:0)与活动性炎症(MES≥1)组,结果显示MES:0组的5年RFS率和CSS率在数值上均更高,但差异同样无统计学显著性(RFS:P=0.165;CSS:P=0.214)(图6)。
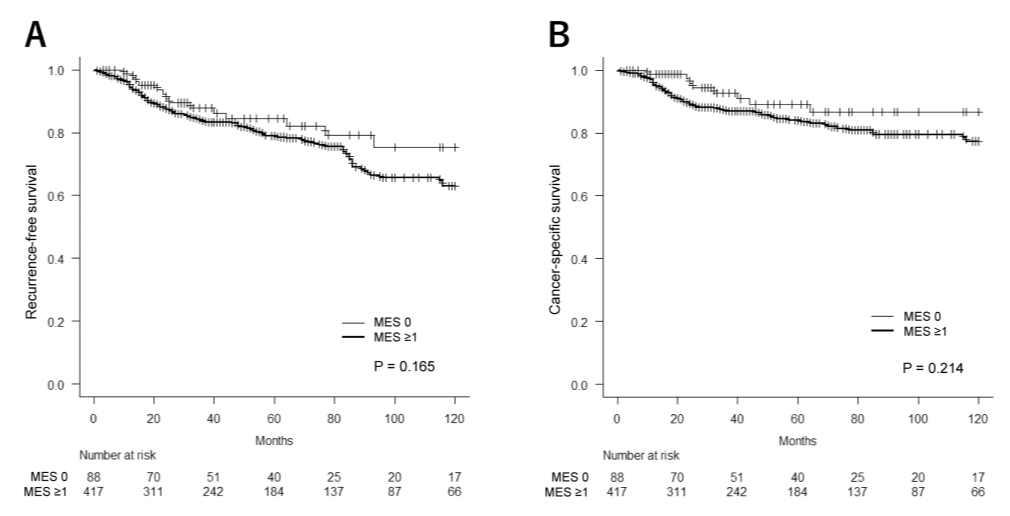
图6. 区域内病例中,非活动性与活动性炎症组的RFS和CSS比较
研究结论
癌症确诊时存在的基础黏膜炎症与UC患者CRC的不良预后显著相关。在确诊癌症时进行系统的内镜评估,可能有助于预后分层,并为治疗决策提供依据。
小结
本研究基于肿瘤与确诊时UC炎症范围的位置关系,探讨了基础黏膜炎症对UC患者CRC预后的影响。结果显示,位于UC累及“区域内”的CRC患者,其RFS和CSS均显著差于“区域外”患者,且此分类是独立的预后因素。进一步分析发现,在区域内患者中,内镜下炎症严重程度(MES)越高,尤其是重度炎症,与更差的预后(特别是CSS)呈阶梯式相关。这提示,诊断时的局部黏膜炎症不仅是癌变风险因素,更是重要的预后决定因素。
本研究也存在一定局限性。包括其回顾性设计可能引入偏倚、未基于病理学严格区分UC相关癌与散发性癌、评估炎症仅依赖内镜且缺乏对全身性炎症的系统评估,以及区域外组样本量相对较少等。这些因素均需在未来通过前瞻性、更大规模的研究加以验证与拓展。
尽管如此,本研究明确提示,在UC患者确诊CRC时,应系统性评估其背景黏膜的炎症状态。这一评估为预后分层提供了有价值的新维度,并可能指导更为个体化的术后辅助治疗决策与随访监测强度,从而将炎症控制从单纯的预防策略延伸至影响预后的临床管理环节。
参考文献
Akiyoshi Ikebata, et al. Background Mucosal Inflammation Affects Colorectal Cancer Prognosis in Ulcerative Colitis: A Nationwide, Multicenter Study. Journal of Crohn's and Colitis. 2025 Dec: jjaf207. https://doi.org/10.1093/ecco-jcc/jjaf207.
- 推荐文章
