- 首页 > 正文
STTT丨文天夫教授团队合作取得新进展:仑伐替尼+经肝动脉化疗栓塞+PD-1单抗三联转化治疗可显著提高不可切除HCC转化手术率
发表时间:2026-03-07 11:38:46

HCC是全球健康的重大威胁,其发病率和死亡率依然居高不下。近半数患者初诊时已处于中晚期,常因多灶性双叶受累、大血管侵犯或未来剩余肝体积不足等因素,肿瘤被判定不可切除,根治机会受限、预后不良。
不过,对符合条件的患者而言,R0切除是获得长期生存乃至潜在治愈的最佳机会。为填补“不可切除”与“可切除”之间的治疗缺口,“转化治疗”应运而生,即通过全身性和/或局部区域性治疗,降低肿瘤分期、控制疾病进展,将初始uHCC转化为可切除病灶,进而施行挽救性肝切除术(SLR)。但由于缺乏前瞻性研究的有力证据,转化治疗在常规临床实践中的应用仍受到制约。
多年来,TACE是中期HCC局部治疗的基石,也被探索作为单一转化治疗策略。然而,其单一手段的转化疗效有限,历史转化率仅为9.8%~12%。这部分归因于TACE术后缺氧微环境诱导促血管生成因子上调,促进肿瘤血管再生、进展和转移。分子靶向治疗的整合可有效对抗这种促血管生成逃逸机制。LAUNCH等研究表明,仑伐替尼联合TACE可显著提高晚期HCC的客观缓解率(ORR)和总生存期(OS),展现出巨大的转化治疗潜力。
与此同时,免疫检查点抑制剂(ICIs)的引入改变了肿瘤治疗格局。近期研究表明,TACE可通过多种机制增强免疫治疗疗效。多项回顾性分析显示,TACE、酪氨酸激酶抑制剂(如仑伐替尼)和抗PD-1药物三联方案对uHCC患者有良好效果,但受回顾性分析方法学局限性的制约。除评估临床结局外,确定治疗反应的预测性生物标志物对实现治疗个性化和优化患者选择至关重要。在HCC患者中,针对复杂三联疗法反应的特定且易于测量的免疫细胞亚群仍有待确定。
在此背景下,文天夫教授团队开展了一项Ⅱ期研究,旨在探究仑伐替尼+TACE+PD-1抑制剂序贯三联疗法在uHCC患者中的疗效和安全性,并通过探索性生物标志物分析识别外周血中具有增殖特征的TCD8+ T细胞亚群,探讨其动态变化作为无创性生物标志物用于预测治疗反应的潜在价值。
疗效突破:LEN-TAP组手术转化率提高3倍以上
研究在中国8家三级医院开展,纳入年龄18~70岁、BCLC分期为B/C期、Child-Pugh分级为A/B级且ECOG PS≤1分的uHCC患者。研究主要终点为转化治疗后成功行SLR的比例。关键次要终点包括:ORR、OS、无事件生存期(EFS)、无复发生存期(RFS),以及转化治疗期间不良事件发生率和SLR后围手术期并发症发生率。2020年10月1日至2021年11月30日期间,共142例符合条件的患者被分配至LEN-TAP组(N=71)或TACE单药组(N=71),两组基线特征匹配良好。
LEN-TAP转化治疗的疗效
在LEN-TAP组中,共有62例(87.3%)患者达到SLR标准,TACE组中则有23例(35.2%)符合标准。在SLR实施方面,LEN-TAP组最终共有42例患者(59.2%)成功接受SLR,显著高于TACE组的13例(18.3%)(P<0.001)。肿瘤缓解情况同样显示LEN-TAP方案优势显著:根据mRECIST标准,其ORR达78.9%,明显高于TACE组的16.9%(P<0.001);按RECIST 1.1标准评估,两组ORR分别为38.0%和7.0%(P<0.001)。疾病控制率(DCR)方面,依据mRECIST标准,LEN-TAP组为94.4%,TACE组为43.7%(P<0.001);根据RECIST 1.1标准,相应结果分别为92.9%和45.1%(P<0.001)。上述结果表明,与TACE单药治疗相比,LEN-TAP转化治疗可获得更优的肿瘤缓解,并能提高uHCC患者接受SLR治疗的比例(图1、表1)。
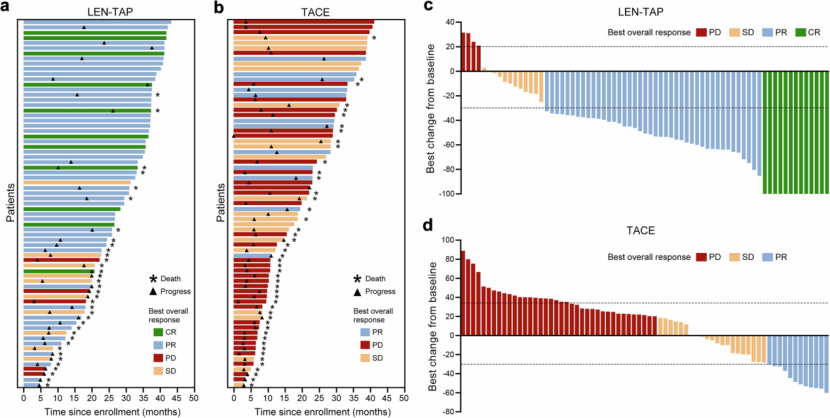
图1. 治疗疗效
表1. 转化治疗后确认的抗肿瘤活性

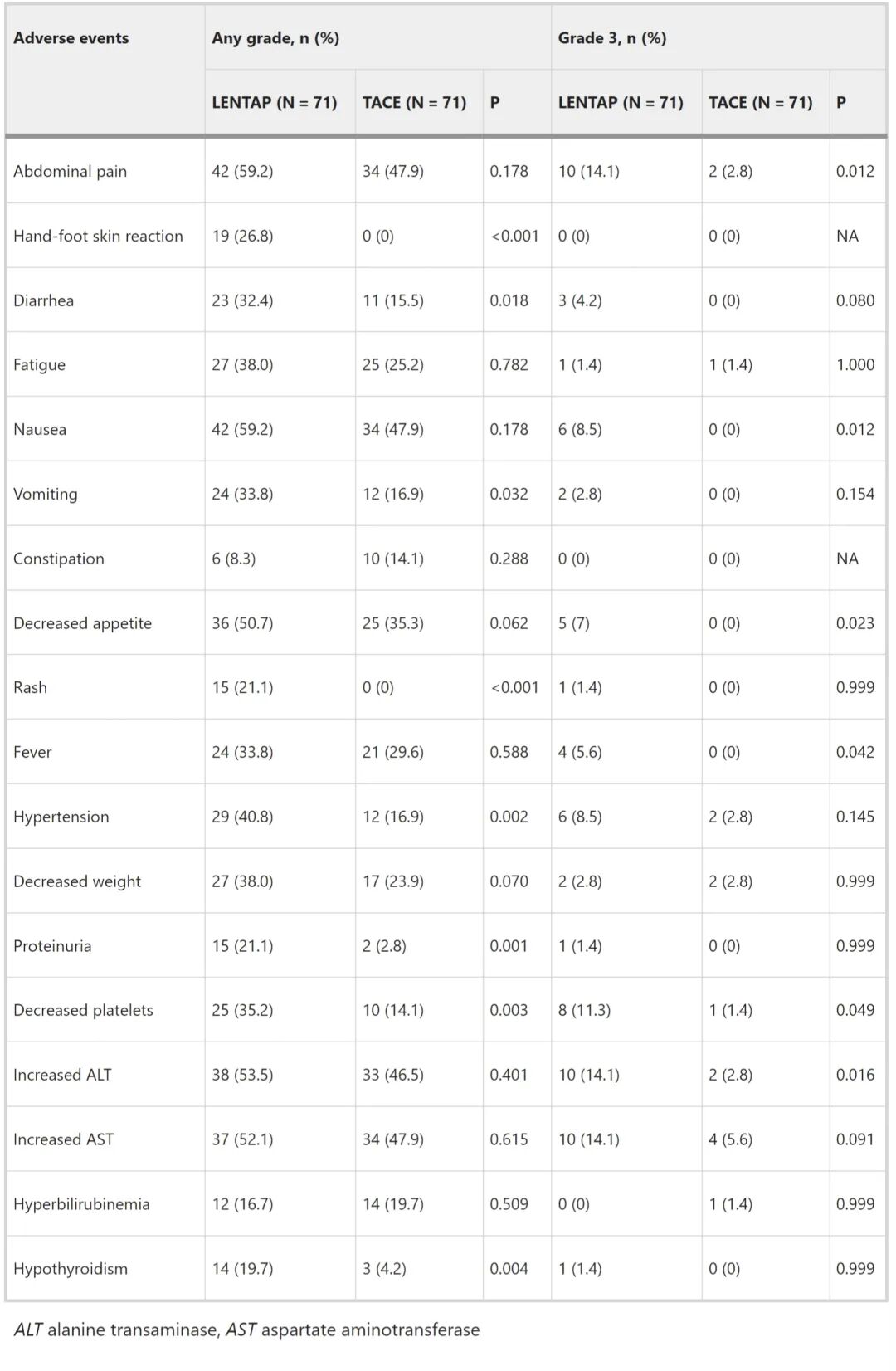
无论因果关系如何,LEN-TAP组所有级别治疗相关不良事件(TRAEs)发生率均高于TACE单药组(表2),包括手足皮肤反应、腹泻、呕吐、皮疹、高血压、蛋白尿、血小板减少和甲状腺功能减退等。其中,3级TRAEs在LEN-TAP组中同样更常见(60.6% vs. 21.1%,P<0.001),但未记录到4级及以上的不良事件。未出现新的或非预期的毒性反应,表明LEN-TAP作为转化治疗方案的安全性整体可控。
表2. 转化治疗后的不良事件
LEN-TAP转化治疗后的挽救性肝切除
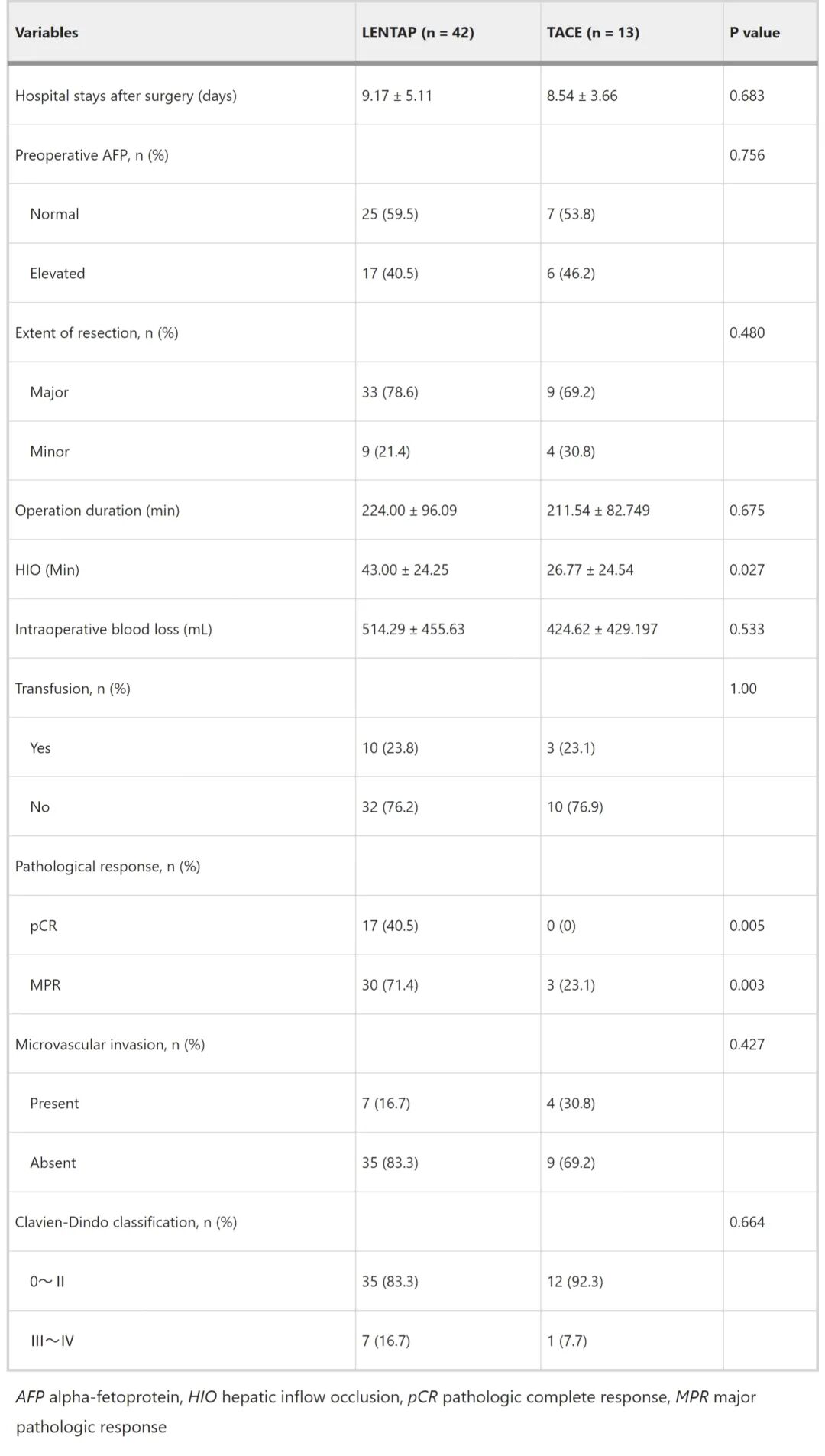
从开始治疗至施行SLR的中位时间方面,LEN-TAP组为4.3个月,TACE组为2.8个月(P=0.001)。在手术方式上,4例患者(LEN-TAP组3例,TACE组1例)接受了腹腔镜手术,其余51例接受开腹手术。两组在并发症发生率、住院时间、手术时长、术中失血量或输血需求方面均未无显著差异。病理评估显示,与TACE组相比,LEN-TAP组达到主要病理缓解(MPR)的患者显著更多(30例 vs. 3例,P=0.003),达到病理学完全缓解(pCR)的患者亦更多(17例 vs. 0例,P=0.005)。在BCLC C期患者中,LEN-TAP组有21例成功接受了SLR;术后病理显示,其中10例(47.6%)患者的门静脉癌栓完全坏死,而其余11例(52.4%)患者的癌栓中仍存在存活的肿瘤细胞。在TACE组,仅有5例BCLC C期患者接受了SLR,且所有患者(100%)的癌栓中均存在残留肿瘤(表3)。
表3. 接受SLR患者的围手术期结局
LEN-TAP转化治疗的长期结局
根据数据截止日期(2024年1月31日),中位随访时间为18.5个月(LEN-TAP组29.33个月,TACE组19.83个月)。LEN-TAP组共有31例(43.7%)患者死亡,TACE组有48例(67.6%)患者死亡。LEN-TAP组的中位OS显著长于TACE组(未达到 vs. 23.0个月,HR=0.48,95%CI:0.31~0.75,P<0.001)(图2a)。LEN-TAP组有42例(59.2%)患者,TACE有63例(88.7%)患者出现疾病进展、死亡或SLR后复发(P<0.001)。LEN-TAP组的中位EFS显著长于TACE组(20.03个月 vs. 6.52个月,HR=0.36,95%CI:0.24~0.54,P<0.001(图2b)。LEN-TAP组17例患者与TACE组9例患者出现复发;两组中位RFS存在显著差异(36.6 vs. 19.0个月,HR=0.45,95%CI:0.17~1.20,P=0.048)(图2c)。
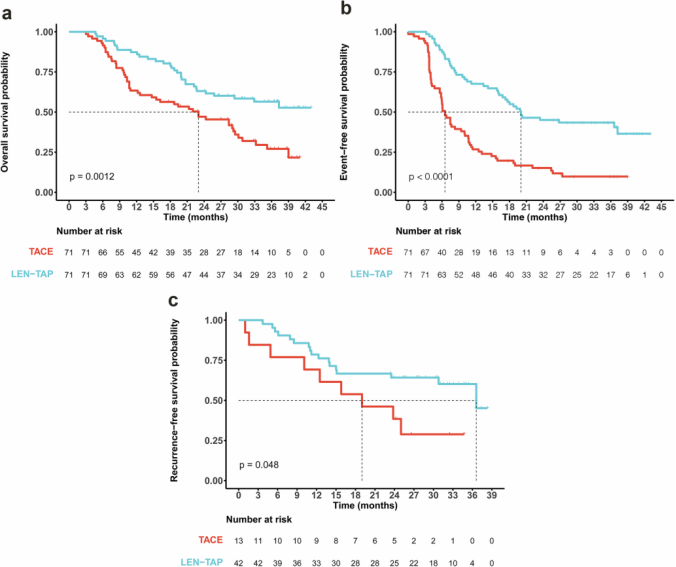
图2. Kaplan–Meier生存分析
生物标志物突破:免疫细胞水平预测疗效
本研究的另一大亮点是深入探寻了潜在的疗效标志物,旨在回答“哪些患者更能从该联合方案中获益”的这一关键问题。
单细胞测序评估LEN-TAP转化治疗导致的免疫改变
研究通过单细胞测序技术评估了LEN-TAP对uHCC患者外周免疫系统的影响。从6例患者(疗效达PR/CR与PD/SD的患者各3例)的外周血中新鲜分离外周血单核细胞,并采用10x Genomics单细胞测序技术进行分析。共计获得并分析了100 367个细胞的转录组数据,这些细胞被聚类为T细胞、B细胞、NK细胞、单核细胞及增殖细胞五大主要类型。
鉴于T细胞是PD-1抑制剂应答的关键效应细胞,研究对其进行了深入分析。T细胞被进一步细分为13种类型。比较疗效良好(PR/CR)患者治疗前后这13类T细胞比例发现HLA-DR+CD38+ T细胞的比例在治疗后显著升高(P=0.039)。进一步将HLA-DR+CD38+ T细胞解析为CD4+、CD8+及双阴性亚群。结果显示,仅在PR/CR患者中,HLA-DR+CD38+CD8+ T细胞亚群在治疗后显著扩增(P=0.03)。
单细胞测序在肿瘤组织中的验证
通过对接受LEN-TAP治疗前后患者的34 042个肝细胞进行单细胞RNA测序,研究识别出八种主要细胞类型,即T细胞、B细胞、肿瘤相关巨噬细胞、胸腺上皮细胞、内皮细胞、浆细胞、癌症相关成纤维细胞和恶性肿瘤细胞。进一步对T细胞亚群分析显示,治疗后HLA-DR+CD38+CD8+ T细胞比例显著升高(P=0.0018)。
CellChat分析揭示,HLA-DR+CD38+CD8+ T细胞与恶性细胞之间存在89个配体-受体网络,其中恶性肿瘤细胞主要提供配体,而HLA-DR+CD38+CD8+ T细胞主要作为受体。值得注意的是,来自肿瘤细胞的CXCL16(配体)和HLA-DR+CD38+CD8+ T细胞上的CXCR6(受体)可能介导关键的肿瘤-免疫相互作用。
免疫荧光和H&E染色显示,治疗后肿瘤组织结构趋于规整,肿瘤细胞密度下降,并伴随表达颗粒酶B的HLA-DR+CD38+CD8+ T细胞浸润增加,提示其细胞毒性功能增强。功能实验进一步发现,LEN-TAP治疗可诱导肿瘤细胞中BAD表达上升,而敲低CXCR6则减弱此效应。
KEGG通路富集分析提示,治疗后HLA-DR+CD38+CD8+ T细胞中差异表达基因显著富集于PI3K-AKT信号通路。Western blotting显示,治疗后p-PI3K与p-AKT水平升高,该效应在CXCR6敲低后呈下降趋势,而总PI3K/AKT比例不变。
外周血HLA-DR+CD38+CD8+ T细胞增加预示更佳治疗反应
为验证单细胞测序结果,研究采用流式细胞术动态监测患者外周血免疫细胞亚群变化。分析发现,在健康对照者、患者治疗前、首次PD-1抑制剂用药后(第1周期)及第二次PD-1抑制剂用药后(第2周期)的外周血中,HLA-DR+CD38+CD8+ T细胞的比例存在显著差异(F=5.942,P=0.0016)(图3a、b)。健康对照者中该细胞的比例远低于接受治疗患者(健康对照 vs. 第1周期:1.45%±0.51% vs. 12.39%±8.15%,P=0.0024;健康对照 vs. 第2周期:1.45%±0.51% vs. 9.86%±8.95%,P=0.03)。与未治疗患者相比,接受首剂PD-1抑制剂治疗的患者该细胞比例更高(12.39%±8.15% vs. 9.86%±8.95%,P=0.03)。
进一步分析发现,在达到PR/CR的患者中,治疗期间HLA-DR+CD38+CD8+ T细胞数量显著增加(F=7.003,P=0.0059),且这种变化在接受首剂PD-1抑制剂后尤为明显(首剂后 vs. 未治疗:16.68%±7.02% vs. 5.50%±1.57%,P=0.0037)(图3c、d)。此外,首剂PD-1抑制剂给药后,PR/CR患者血液中该细胞比例高于PD/SD患者(16.68%±7.02% vs. 4.66%±1.24%,P=0.0029)(图3e)。而在PD患者中,治疗前后该细胞比例未出现显著变化(基线 vs. 首剂后 vs. 第二剂后:5.24%±2.33% vs. 4.66%±1.24% vs. 3.98%±2.09%,F=0.55,P=0.51)(图3f)。
以上结果表明,外周血HLA-DR+CD38+CD8+ T细胞的动态升高可能与LEN-TAP转化治疗的疗效相关,有望成为预测该方案应答的有效生物标志物。
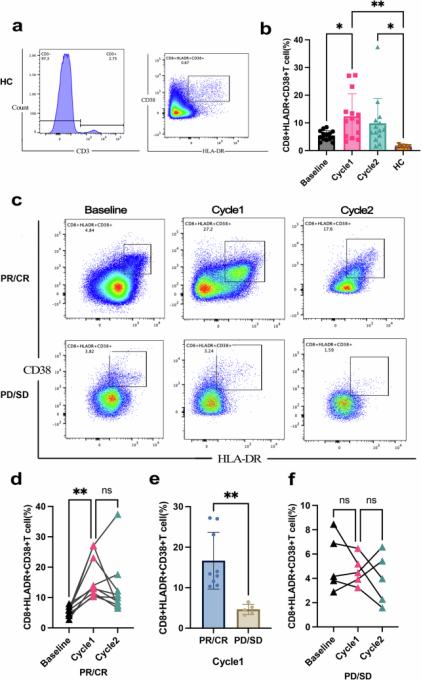
图3. 流式细胞术检测T细胞活化状态分析
研究小结与讨论
本研究作为首项前瞻性临床试验证实对于uHCC患者,LEN-TAP转化治疗安全有效。在本研究中,LEN-TAP疗法使87.3%的uHCC转化为可切除疾病,最终59.2%的患者接受了根治性SLR。与单独使用TACE作为转化治疗相比,LEN-TAP转化治疗显著提高了SLR率、ORR、OS、EFS和RFS。同时,未出现新的或非预期毒性,且未发生4级及以上不良事件,表明该三联方案的毒性特征总体可控。研究同时发现,外周血HLA-DR+CD38+CD8+ T细胞比例动态升高可作为预测LEN-TAP疗效的潜在生物标志物,该细胞群似乎通过CXCR6–PI3K–AKT信号轴发挥抗肿瘤作用。总之,该研究结果表明LEN-TAP是极具前景的转化治疗策略,并为个体化治疗提供了新的生物标志物方向。
参考文献
Zhang X, et al. Signal Transduct Target Ther. 2026 Jan 22;11(1):37.- 推荐文章
