- 首页 > 正文
《NEJM》及其子刊发布2025最佳论文榜单:结直肠癌2项研究入选!
发表时间:2026-03-04 08:46:15
编者按
近日,《新英格兰医学杂志》(NEJM)及其子刊发布了2025年度的一些重磅研究,结直肠癌领域的两项入选研究分别从“主动干预”与“精准去手术”两个维度,为患者提供了新的治疗选择。一方面,研究发现规律运动干预能显著延长结肠癌患者的无病生存期,提示在药物和手术之外,积极的生活方式干预已成为癌症综合管理中不可或缺的一环。另一方面,对于存在错配修复缺陷(dMMR)的局部晚期直肠癌患者,使用程序性死亡受体1(PD-1)免疫检查点抑制剂进行新辅助治疗,可实现较高的病理完全缓解率,使许多患者在根治肿瘤的同时最大程度保留器官功能与生活质量。
这两项进展共同指向一个核心方向:现代结直肠癌治疗正从“最大可耐受治疗”转向“最小有效干预”,在追求长期生存的同时,更加关注治疗过程中的生活品质与功能保全。以下是相关研究的详细解读与临床启示。

结肠癌辅助化疗后的结构化运动试验
结直肠癌是全球第三大常见癌症,也是癌症相关死亡的第二大原因。对于高危Ⅱ期或Ⅲ期结肠癌,标准治疗方案包括术后辅助化疗。尽管如此,仍有20%~40%的患者出现疾病复发,这意味着此类人群亟需既能改善生存又能提升生活质量的干预措施。多项研究表明,运动可抑制包括结肠癌在内的肿瘤生长,并降低癌症复发和死亡风险,其潜在机制可能与运动对代谢生长因子、炎症及免疫功能的影响有关。然而,运动干预是否能确实改善恶性肿瘤预后仍需Ⅲ期临床试验证实。
为填补这一研究空白,加拿大癌症试验组(CCTG)开展了CO.21“结肠健康与终身运动改变”(CHALLENGE)试验,这是一项Ⅲ期随机研究,旨在比较单纯健康教育与健康教育联合3年结构化运动计划对已完成辅助化疗的结肠癌患者的影响。既往已报告了该试验中运动行为改变的可行性,本文报告了最终结果。
研究设计
在这项于55个中心开展的Ⅲ期随机试验中,将已完成辅助化疗并接受结肠癌切除术的患者随机分配到结构化运动计划组(运动组)或仅接受健康教育材料组(健康教育组),随访时间为3年。主要终点是无病生存期(DFS),关键次要终点包括总生存期(OS)、患者报告的身体功能、客观身体功能与体能水平、休闲中高强度体育活动。2009年至2024年,共有889例患者被随机分配至运动组(445例)或健康教育组(444例)。
研究结果
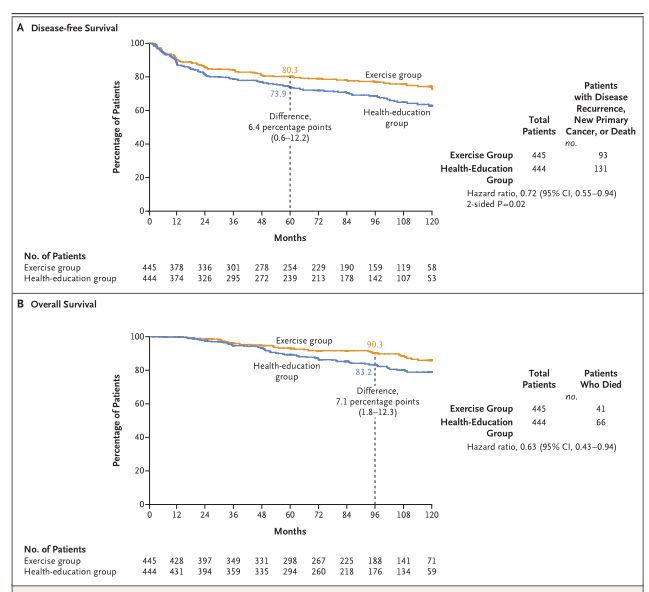
中位随访7.9年,共有224例DFS终点事件(包括疾病复发、新原发癌或死亡),运动组93例,健康教育组131例。Kaplan–Meier生存曲线显示,运动组DFS显著优于健康教育组(HR=0.72;95%CI:0.55~0.94;P=0.02)。运动组年DFS事件发生率(复发、新发原发癌或死亡)为3.7%,健康教育组为5.4%。两组的5年DFS率分别为80.3%和73.9%,绝对差6.4个百分点(图1A)。预设亚组分析显示大部分预设亚组均可获益,提示运动获益在各亚组中具有一致趋势。
运动组的OS长于健康教育组(HR=0.63;95%CI:0.43~0.94)。运动组每年死亡发生率为1.4%(95%CI:1.0~1.8),健康教育组为2.3%(95%CI:1.7~2.8)。运动组8年OS率为90.3%,健康教育组为83.2%(差异为7.1个百分点;95%CI:1.8~12.3)(图1B)。
安全性数据显示,干预期间,运动组351例患者(82.0%)和健康教育组352例患者(76.4%)发生了至少一起任意级别不良事件。运动组79例患者(18.5%)和健康教育组53例患者(11.5%)发生了肌肉骨骼不良事件。运动组的79例肌肉骨骼不良事件中,8例(10%)被认为与运动干预相关。运动组66例患者(15.4%)和健康教育组42例患者(9.1%)报告了≥3级不良事件。
研究意义与未来展望
CHALLENGE研究证实,结肠癌辅助化疗后开展为期3年的结构化运动可显著改善患者生存,且安全性可控。结果显示,运动组患者疾病复发、新发原发癌或死亡的风险较健康教育组降低28%。OS方面,运动组死亡风险降低37%。进一步分析发现,运动主要通过减少肝转移、降低继发原发癌发生率来驱动DFS获益。该结果支持将运动干预纳入结肠癌标准治疗体系,具有重要的临床实践意义。未来需进一步探索运动介入的最佳时机及个体化实施方案,并推动医疗系统建立相应的行为支持体系[1]。
错配修复缺陷型肿瘤的非手术治疗
在dMMR型局部晚期直肠癌患者中,新辅助免疫检查点抑制剂已使很大一部分患者无需手术。但这种方法是否适用于所有早期dMMR实体瘤(无论肿瘤部位如何),目前尚不清楚。为验证这一理念,该研究入组了适合根治性治疗的早期dMMR肿瘤患者(不限原发部位),给予为期6个月的PD-1抑制剂dostarlimab治疗,并密切监测疗效、进展及复发情况。
研究设计
本研究为一项Ⅱ期临床试验,旨在评估新辅助dostarlimab在可根治性切除的Ⅰ~Ⅲ期dMMR实体瘤患者中的疗效与安全性。患者接受为期6个月的dostarlimab治疗后,其治疗反应在两个预设队列中分别进行评估:队列1为dMMR局部晚期直肠癌患者,队列2为dMMR非直肠实体瘤患者(包括食管胃癌、结肠癌、肝胆癌、泌尿生殖系统癌和妇科肿瘤)。达到临床完全缓解(cCR)的患者可选择非手术治疗及密切随访;仍有残留病灶者则接受根治性手术切除。主要研究终点为队列1中患者在12个月时的持续cCR率。次要终点包括无复发生存期与安全性。
研究结果
共有117例患者纳入分析。在队列1中,49例完成治疗的患者均达到cCR,并选择非手术治疗。其中37例患者在12个月时仍保持cCR,符合疗效标准。在队列2中,54例完成治疗的患者中有35例(65%)达到cCR,其中33例(61%)选择非手术治疗。两个队列共103例完成治疗的患者中,84例(82%,95%CI:72%~88%)达到cCR,82例(80%,70%~87%)未接受手术治疗(图2)。117例患者的2年无复发生存率为92%(95%CI:86%~99%);中位复发随访时间为21.5个月(范围:0~60.8个月)。绝大多数患者(95%)出现可逆的1级或2级不良事件(60%)或未出现不良事件(35%)。所有患者在治疗期间或治疗后,均未影响根治性切除的选择。
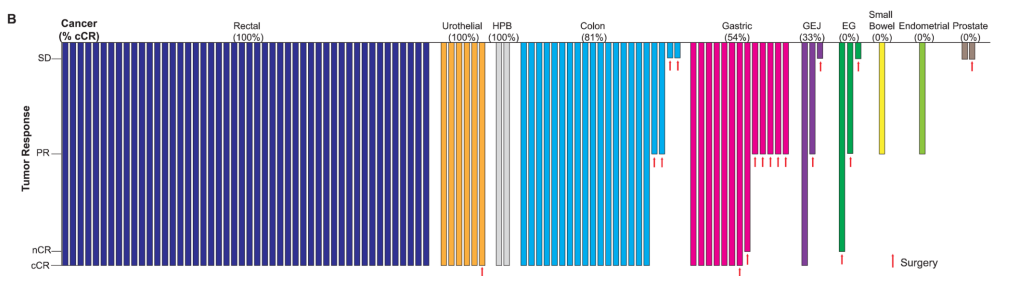
图2. 按肿瘤类型划分的临床反应
研究意义与未来展望
初步研究数据表明,在早期患者中,为期6个月的新辅助免疫治疗安全性良好,且未影响后续手术的可及性。值得注意的是,所有达到cCR的患者均成功保留了器官功能,其中部分直肠癌患者甚至在治疗后正常生育。疗效差异可能与肿瘤类型有关,如胃食管癌、前列腺癌的缓解率相对较低,其机制或与肿瘤微环境相关。疾病复发较少见,且复发后通过局部治疗或再次免疫治疗仍可控制。该疗法仍需更大规模、更长随访的研究验证,尤其在非直肠癌人群中。未来研究方向包括探索联合治疗、优化疗程,并依据不同肿瘤手术对生活质量的影响程度,设计差异化的临床验证路径。本研究为早期肿瘤的“去手术化”精准治疗奠定了重要基础[2]。
总结
现代结直肠癌治疗已从“最大可耐受治疗”逐步迈向“最小有效干预”的新阶段。NEJM及其子刊近期评选的2025年度重要研究成果中,两项来自结直肠癌领域的研究深刻体现了这一理念转变的实践成果。一方面,CHALLENGE试验证实,在完成辅助化疗的结肠癌患者中,为期三年的结构化运动干预可使疾病复发、新发原发癌或死亡风险降低,这标志着生活方式干预已成为重要的综合管理支柱之一。另一方面,针对dMMR型局部晚期直肠癌患者,新辅助PD-1抑制剂治疗显示出强大的肿瘤清除能力,使绝大多数患者达到cCR,从而实现器官功能保全并避免根治性手术,且不影响根治机会。两项研究共同启示我们:肿瘤治疗的成功,不仅在于消灭疾病,更在于帮助患者有质量地长期生存。未来,以运动为代表的行为干预和以免疫治疗为代表的精准去手术化策略,将进一步推动结直肠癌诊疗模式向更人性化、更个体化的方向演进,最终实现生存时间与生活质量的双重提升。
参考文献:
[1]Courneya KS, et al. N Engl J Med. 2025 Jul 3;393(1):13-25.[2]Cercek A, et al. N Engl J Med. 2025 Jun 19;392(23):2297-2308.
- 推荐文章
