- 首页 > 正文
《Nature Medicine》发布2026年关键医学研究榜单:胰腺癌RASolute 302 Ⅲ期研究入选!
发表时间:2026-03-04 09:46:53
随着2025年的帷幕缓缓落下,医学界已将目光投向更具希望的2026年。值此辞旧迎新之际,Nature Medicine杂志集结全球顶尖专家,评选出“将影响2026年医学发展的11项关键临床试验”,这份名单如同一份寄往新年的“科学贺信”,涵盖传染病疫苗、基因编辑、癌症治疗等多个突破领域,勾勒出来年医学发展的关键脉络。在这11项研究中,一项针对胰腺癌的Ⅲ期临床试验尤为引人注目。胰腺癌是最具挑战性的恶性肿瘤之一,其治疗方案有限、肿瘤侵袭性强,且患者生存期极短。近90%的胰腺癌由KRAS基因突变驱动——这是科学家四十年来致力攻克的关键靶点[1]。如今,随着新型广谱RAS抑制剂RMC-6236(daraxonrasib)的出现,胰腺癌治疗困局或迎来转机。
本文将系统阐述RMC-6236的作用机制及关键Ⅰ期临床证据,概述其获FDA突破性疗法认定的依据,并深入解读其Ⅲ期验证性研究RASolute 302的设计与意义。该研究结果预计于2026年公布,其数据有望为晚期胰腺癌治疗带来新的标准。科学探索永不止步,我们期待2026年见证该领域的重要进展。

RMC-6236简介:一种广谱靶向RAS的新型口服抑制剂
胰腺导管腺癌(PDAC)是癌症相关死亡的第三大主要原因,目前临床治疗选择有限。即使采用多药联合化疗方案,二线治疗PDAC患者的中位无进展生存期(PFS)仅约2~3.5个月,中位总生存期(OS)约6~7个月。从分子机制看,约90%的PDAC病例存在KRAS基因突变,主要集中于12号密码子,常见亚型包括G12D(35%)、G12V(20~30%)、G12R(10~20%)及G12C(1~2%)。KRAS突变在胰腺癌发生发展中起关键驱动作用,可在癌前病变早期出现,且KRAS突变型肿瘤患者的预后显著差于野生型(中位OS:22个月 vs. 38个月)。RMC-6236是一种口服的RAS(ON)多选择性三复合物抑制剂,能够同时抑制突变型与野生型RAS的活性鸟苷三磷酸(GTP)结合状态,为PDAC的靶向治疗提供了新策略[2,3]。
Ⅰ期临床研究数据:显示良好安全性与初步疗效
RMC-6236-001 Ⅰ期研究评估了RMC-6236在RAS突变型PDAC患者中的安全性、疗效及早期ctDNA动态变化。该研究采用剂量递增设计,后续开展剂量优化与扩展队列。入组标准为在2024年7月23日数据截止前接受≥14周临床有效剂量(160~300 mg,每日一次)治疗的患者。研究通过采集配对血浆样本,分析基线及治疗期间RAS突变等位基因频率的变化。
截至2024年7月23日,共127例RAS突变型PDAC患者接受RMC-6236治疗。在300 mg剂量组中,患者中位PFS达到7.6~8.5个月,显著优于历史对照。最常见的(≥10%的患者)任何级别的治疗相关不良事件包括皮疹(91%)、腹泻(48%)、恶心(43%)、呕吐(31%)、口腔炎(31%)、疲乏(20%)、甲沟炎(13%)、黏膜炎症(13%)、食欲下降(11%)和外周水肿(10%)。127例患者中有106例进行了配对血浆样本检测。其中,68例基线时存在RAS突变等位基因的患者可评估ctDNA结果。
该研究表明,RMC-6236在经治RAS突变型PDAC患者中安全性良好,并显示出良好的抗肿瘤活性及早期ctDNA清除效应(表1)[2]。基于这些结果,全球Ⅲ期临床试验RASolute 302已启动,旨在评估RMC-6236对比标准化疗用于转移性PDAC二线治疗的疗效。
表1. RMC-6236-001研究疗效数据
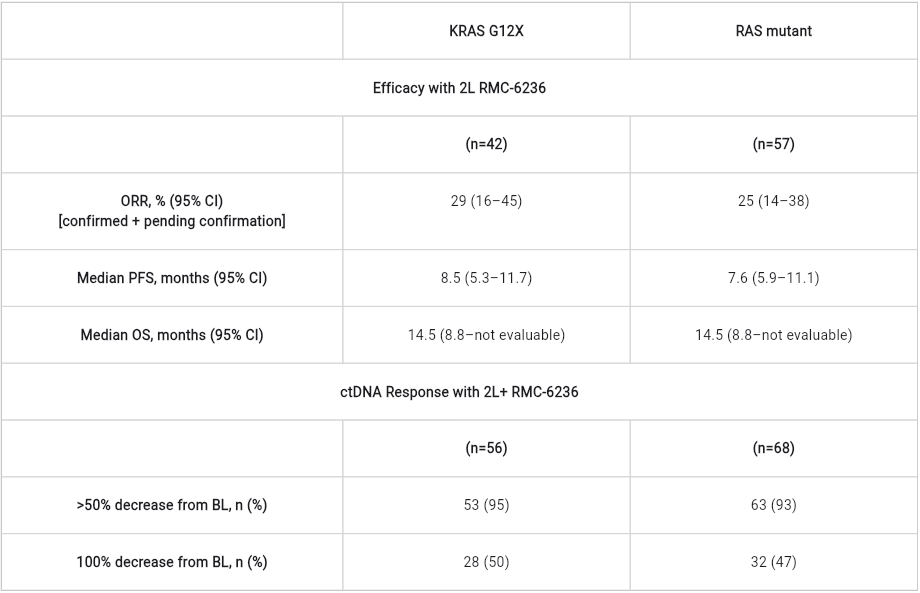
基于RMC-6236-001 Ⅰ期研究中观察到的积极数据,美国食品药品监督管理局已授予RMC-6236(daraxonrasib)突破性疗法认定,用于既往接受过治疗、携带KRAS G12突变的转移性PDAC患者。突破性疗法认定旨在加速针对严重疾病且存在重大未满足临床需求药物的研发与审评,要求药物在临床终点上显示出较现有疗法更具潜力的改善。该认定进一步支持了RMC-6236的临床开发价值[4]。
Ⅲ期临床试验设计:RASolute 302研究方案详解
为满足晚期PDAC患者迫切的治疗需求,一项名为RASolute 302的全球、多中心、开放、随机对照Ⅲ期研究(NCT06625320)正在进行。该研究计划纳入约460例年龄≥18岁、美国东部肿瘤协作组体能状态评分(ECOG PS)0~1、既往接受一线含5-氟尿嘧啶或吉西他滨方案治疗后进展的转移性PDAC患者。患者需明确RAS突变状态,符合条件者按1:1随机分组,分别接受RMC-6236 300 mg每日一次口服,或研究者选择的标准化疗。允许既往接受过靶向治疗的RAS野生型患者入组。
研究主要终点为RAS G12X突变人群经独立盲态评估的PFS和OS;关键次要终点包括全RAS突变人群及RAS野生型人群的PFS、OS、客观缓解率与生活质量。肿瘤评估每8周进行一次,直至疾病进展或研究终止。该试验于2024年10月启动患者入组,其结果有望为RMC-6236在PDAC二线治疗中的定位提供关键证据[5]。
总结
胰腺癌的靶向治疗或将迎来关键转折,以RMC-6236为代表的新型广谱RAS抑制剂,通过独特机制突破传统靶向策略,为占胰腺癌绝大多数的KRAS突变患者带来了一定治疗获益。Ⅰ期研究数据显示,该药物在经治患者中展现出显著优于现有二线化疗的疗效(中位PFS 7.6~8.5个月,中位OS 14.5个月),且可快速降低ctDNA水平,其潜力已获FDA突破性疗法认定。
目前正在开展的RASolute 302 Ⅲ期全球研究,将直接对比RMC-6236与标准化疗在晚期胰腺癌二线治疗中的疗效,预计2026年公布结果。若研究成功,将可能为胰腺癌治疗格局带来关键变化——从传统化疗转向精准靶向。这项突破也预示着胰腺癌治疗正从“针对器官”向“针对驱动基因”的精准治疗新时代加速迈进。
参考文献:
[1] May M. Nat Med. 2025 Dec;31(12):3943-3947.[2] Ignacio Garrido-Laguna,et al. 2025
ASCO GI. Abstract 722.
[3] Fivaz M, et al. BMJ Open Gastroenterol. 2025 Nov 27;12(1):e001925.
[4] https://ir.revmed.com/news-releases/news-release-details/revolution-medicines-announces-fda-breakthrough-therapy/
[5] Brian M. Wolpin,et al. 2025
ASCO GI. TPS4230.
- 推荐文章
