- 首页 > 正文
JAMA Oncol重磅:ctDNA精准识别塞来昔布辅助治疗获益人群,结肠癌术后治疗迎来新突破!
发表时间:2026-03-04 09:55:03
结直肠癌(CRC)是全球范围内发病率与死亡率均位居前列的恶性肿瘤。其中,Ⅲ期结肠癌患者虽经根治性手术切除,但仍面临较高的复发风险,术后辅助治疗方案的优化与疗效预测是当前临床研究的核心议题之一。塞来昔布作为非甾体抗炎药(NSAIDs),其抗肿瘤潜力及在CRC辅助治疗中的价值逐渐受到关注,CALGB/SWOG 80702 Ⅲ期随机临床试验为此提供了重要的循证医学依据。与此同时,循环肿瘤DNA(ctDNA)凭借其无创性、实时检测的优势,已成为肿瘤早筛、疗效评估及预后判断的新型生物标志物,在CRC诊疗中的应用前景广阔。本研究是基于CALGB/SWOG 80702试验的事后分析,旨在探索ctDNA在塞来昔布治疗的Ⅲ期结肠癌中的预测价值,以期为精准筛选获益人群、制定个体化辅助治疗策略提供科学依据,进一步推动Ⅲ期结肠癌诊疗模式的革新与发展。该研究成果已正式发表于JAMA Oncology。本文将对该研究进行深入解读,以飨读者。

研究介绍
CALGB/SWOG 80702 Ⅲ期试验将接受根治性切除术后的Ⅲ期结肠癌患者随机分配至两组,分别接受为期3个月或6个月的辅助氟尿嘧啶、亚叶酸钙和奥沙利铂(FOLFOX)方案化疗,并同时接受每日400 mg塞来昔布或安慰剂治疗,疗程为3年。虽然塞来昔布组和安慰剂组之间的无病生存期(DFS)无统计学差异,但呈现出改善趋势(HR=0.89),提示部分患者可能获益。ctDNA作为分子残留病灶标志物已确立预后价值,但其在治疗指导中的作用尚未明确。基于此,开展了这项事后分析,旨在评估:1)ctDNA状态对Ⅲ期结肠癌的预后价值;2)ctDNA能否预测塞来昔布联合治疗的疗效差异。研究终点包括DFS和总生存期(OS)。
研究结果
940例ctDNA状态有效的患者被纳入本研究,中位随访时间为6.0年(95%CI:6.0~6.0),767例(81.6%)为ctDNA阴性,173例(18.4%)为ctDNA阳性。
根据ctDNA状态和塞来昔布使用情况评估的结果
在所有患者中,ctDNA状态是生存期的重要预后因素。与ctDNA阴性患者相比,ctDNA阳性患者的DFS(校正HR=6.12,95%CI:4.66~8.03)和OS(校正HR=5.86,95%CI:4.19~8.19)均较短。ctDNA阴性患者的3年DFS率估计值为86.5%,而阳性患者为33.7%;5年OS率估计值分别为91.5%和52.6%(图1)。
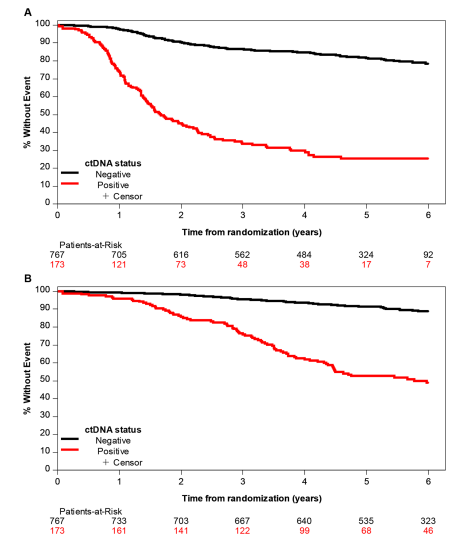
图1. 根据术后ctDNA状态评估的DFS和OS。(A)DFS;(B)OS
在ctDNA阳性患者中,与安慰剂相比,应用塞来昔布可改善DFS,估计3年DFS率分别为41.0%和22.6%(校正后HR=0.61,95%CI:0.42~0.89;图2A,表1)。相反,在ctDNA阴性患者中,DFS无统计学显著差异(估计3年DFS率分别为87.4%和85.6%;校正后HR=0.76,95%CI:0.53~1.09;图2A,表1)。然而,按ctDNA状态比较塞来昔布与安慰剂效应的交互作用检验无统计学显著性(P=0.41)。
同样,在ctDNA阳性患者中,与安慰剂相比,应用塞来昔布可改善OS,估计5年OS率分别为61.6%和39.9%(校正后HR=0.62,95%CI:0.40~0.96;图2B,表1);但在ctDNA阴性患者中未见此关联(估计5年OS率分别为91.8%和91.3%;校正后HR=0.85,95%CI:0.54~1.36;图2B,表1)。该交互作用同样无统计学显著性(P=0.33)。
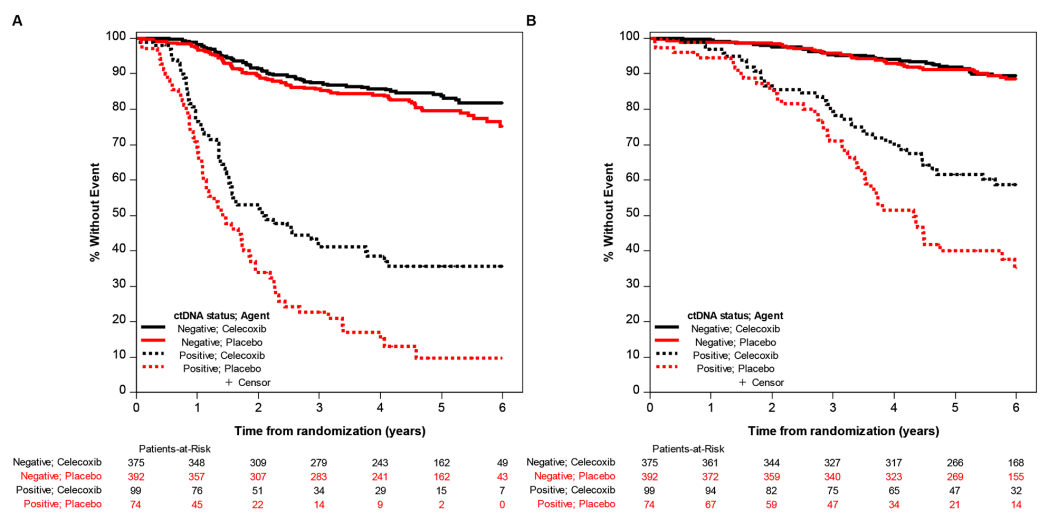
图2. 根据分配的口服药物(塞来昔布 vs. 安慰剂)与术后ctDNA状态评估的DFS和OS。(A)DFS;(B)OS
表1. 根据分配的口服药物(塞来昔布 vs. 安慰剂)与术后ctDNA状态评估的生存结果
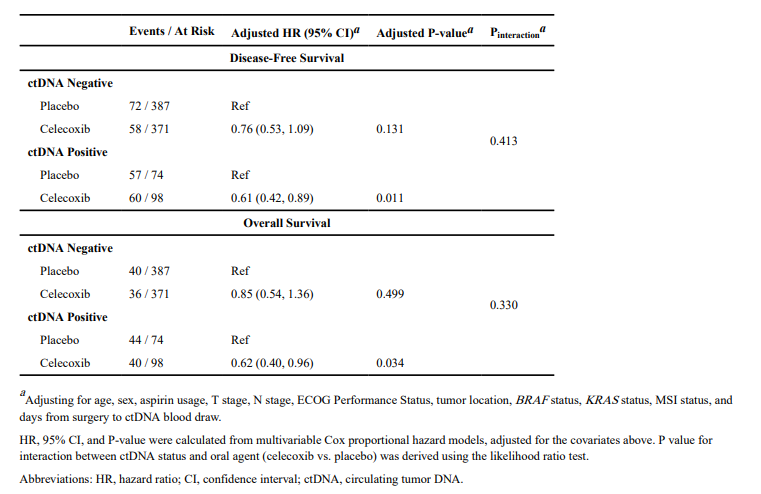
亚组分析结果
本研究通过特定亚组分析,评估ctDNA状态对塞来昔布治疗生存获益的潜在影响效应。按微卫星不稳定性(MSI)状态分层显示:在非MSI高表达(MSI-H)肿瘤患者中,ctDNA阳性患者使用塞来昔布的3年DFS率估计值为39.7%,安慰剂组为22.3%(校正HR=0.63,95%CI:0.42~0.93)(图3A,B);而在ctDNA阴性且非MSI-H肿瘤患者中,塞来昔布相比安慰剂未显示显著生存获益(校正HR=0.76,95%CI:0.52~1.11)。在MSI-H肿瘤患者中,ctDNA阳性者使用塞来昔布与DFS改善显著相关(校正HR=0.05,95% CI:0.00~0.59),而ctDNA阴性者则无此关联(校正HR=1.25,95%CI:0.37~4.23)。
研究者进一步根据原发肿瘤PIK3CA突变状态分析了ctDNA与塞来昔布的关联,已知激活型或功能获得性PIK3CA突变可预测塞来昔布辅助治疗的生存获益。在202例(21.5%)携带该突变的患者中,对于PIK3CA野生型肿瘤患者,ctDNA阳性者使用塞来昔布与DFS改善相关(校正HR=0.64,95%CI:0.42~0.98)(图3C,D),而ctDNA阴性者无此获益(校正HR=0.80,95%CI:0.55~1.18)。在PIK3CA激活型肿瘤患者中,塞来昔布使用同样与DFS改善相关(估计3年DFS率分别为44.4% vs. 15.4%;校正HR=0.19,95%CI:0.06~0.58);反之,ctDNA阴性且携带PIK3CA激活突变的患者未显示DFS获益(校正HR=0.85,95%CI:0.33~2.24)。
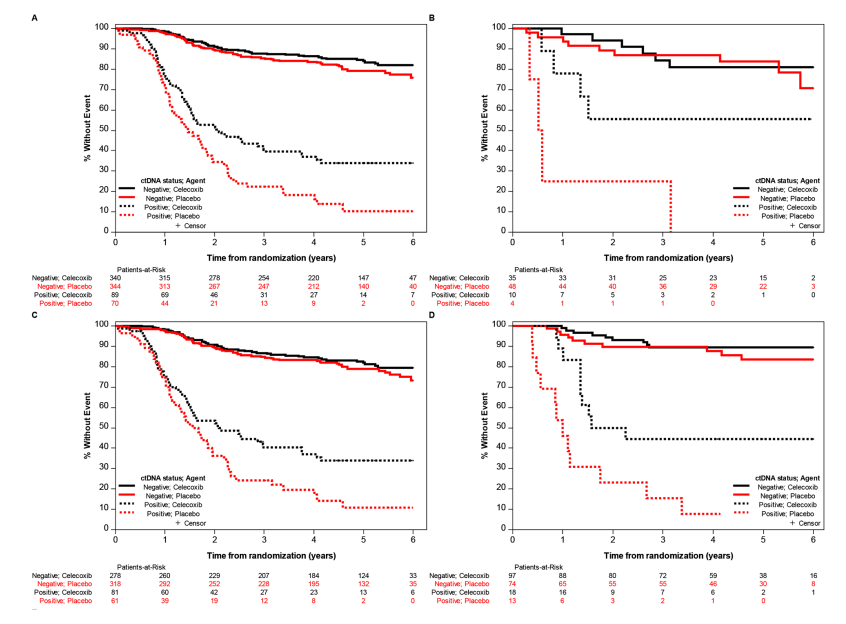
研究讨论与结论
在这项针对Ⅲ期结肠癌随机研究的事后分析中,研究者发现术后ctDNA阳性患者在接受常规化疗联合辅助性塞来昔布治疗后,其DFS和OS均获得改善,而ctDNA阴性患者则未显现获益。在调整了包括MSI和PIK3CA突变状态在内的基线人口统计学、病理学及分子学因素后这些发现仍然成立。虽然在整个队列中,ctDNA状态与治疗组间的交互作用未达到统计学显著性,但在仅限于高质量ctDNA结果的亚组分析中呈现出显著性。此外,ctDNA阳性患者使用塞来昔布后,其预估3年DFS率提高了18.4%(从22.6%升至41.0%),而ctDNA阴性患者仅提高1.8%(从85.6%升至87.4%),这表明可能存在具有临床意义的治疗效果差异。
本研究首次提出,通过ctDNA评估的分子残留疾病可能作为CRC患者对辅助性COX抑制治疗反应的潜在预测因子。鉴于其强相关性,目前已有研究致力于利用ctDNA指导临床决策,其中大多数研究聚焦于辅助化疗的强化或降级。针对ctDNA状态与CALGB/SWOG 80702试验中第二个随机化因素(3个月 vs. 6个月辅助FOLFOX化疗)的分析正在进行,结果将另行报告。根据已知信息,本研究首次提供证据支持分子残留疾病可作为CRC辅助治疗中附加治疗策略(特别是COX抑制)的决定因素,从而将其应用范围拓展至传统化疗指导之外。
本研究表明,术后ctDNA阳性与Ⅲ期结肠癌生存率降低密切相关,而辅助性塞来昔布能为ctDNA阳性患者带来生存获益。ctDNA有助于通过识别最有可能从常规化疗联合辅助性COX抑制治疗中获益的患者亚群来指导临床决策,并为CRC的个体化治疗提供新机遇。
参考文献:
[1]Zhang GQ, et al. JAMA Oncol. 2025 Dec 4:e255144.- 推荐文章
