- 首页 > 正文
“瘤瘤”新知丨警惕!新发糖尿病成胰腺癌高风险“信号灯”,精准锁定早期检测“黄金窗口期”至关重要
发表时间:2026-03-04 15:27:42
导 语
胰腺导管腺癌(PDAC)作为消化道常见的高度恶性肿瘤,因其恶性程度高、早期诊断困难、手术切除率低、预后极差,且对传统治疗方法普遍抵抗,导致患者长期生存率低下,素有“癌中之王”之称。手术切除是唯一可能实现根治的手段,但其成功依赖于在肿瘤仍可切除时发现病灶,这凸显了早期检测的迫切需求。
对具有PDAC家族史、特定基因突变或遗传综合征等高危人群进行监测,相比未监测人群,可更早发现肿瘤、提高切除率并延长生存期。然而,大多数PDAC病例为散发性,因此识别散发性PDAC的高风险人群成为临床工作的重点。其中,一个值得关注的高风险群体是50岁以上新发糖尿病(NOD)患者,其罹患PDAC的风险比一般人群高6~8倍。NOD与PDAC的关联早在多年前已被认识,近期研究进一步揭示了PDAC确诊前出现的代谢功能障碍,其机制涉及复杂的癌症-宿主代谢相互作用,导致葡萄糖和脂质代谢发生改变。尽管NOD已被公认为PDAC的高风险人群,但目前仍缺乏基于人群的PDAC风险精确发病率数据。现有研究多受限于回顾性设计、未基于血糖标准定义NOD,或仅来自单一机构数据,可能引入偏倚风险。此外,关于从NOD到PDAC确诊之间的时间信息仍十分有限,而了解这一时间信息对于评估NOD在早期PDAC检测中的作用至关重要。
在此背景下,研究人员开展了一项多中心前瞻性队列研究。该研究评估了18 838例年龄≥50岁、依据血糖标准定义为新发糖尿病(GNOD)的成年患者中PDAC的发病风险及从GNOD到确诊PDAC的时间特征,为将NOD定义为具有临床相关性的早期散发性PDAC检测人群提供了关键指导。
研究一览
研究方法
本研究为一项基于多中心电子健康记录的前瞻性队列研究,旨在评估GNOD人群中PDAC的发病风险与确诊前的时间特征。
研究对象需同时满足“GNOD”三项标准:①14天内首次达到美国糖尿病协会(ADA)糖尿病阈值(单次HbA1c≥6.5%即视为达标,空腹血糖仍需二次检测);②过去18个月内至少有一次血糖记录但未超标;③既往无糖尿病诊断或降糖药物/胰岛素史。排除既往恶性肿瘤、妊娠、严重肝硬化或长期糖皮质激素使用者。
研究纳入经特定标准定义的GNOD患者,通过电子病历收集患者糖尿病及PDAC相关信息、人口统计学特征等数据。主要研究终点为GNOD中PDAC的标准发病率比、绝对发病率及从GNOD至PDAC临床确诊的时间分布特征;次要终点为经种族调整的绝对发病率以及GNOD识别延迟对PDAC风险的影响。统计分析计算了发病率相关数据、Kaplan-Meier估计值、不同情景下的绝对发病率及各间隔的SIR等。
研究结果
研究纳入2018年9月至2022年5月在4个参与机构中确定的18 838例GNOD患者。中位年龄为63岁,51%的参与者为男性。患者种族和民族分类如下:35%为非西班牙裔白人,32%为西班牙裔,12%为非裔美国人,18%为亚裔/太平洋岛民。与非西班牙裔白人患者(65岁)相比,西班牙裔患者(61岁)、非裔美国人患者(61岁)和亚裔/太平洋岛民患者(63岁)在确诊GNOD时的中位年龄显著更低(P<0.001),且西班牙裔(47%)、非裔美国人(44%)和亚洲/太平洋岛民患者(38%)中处于50~59岁年龄段的比例高于非西班牙裔白人患者(28%,P<0.001)(表1)。
表1. 研究人群的人口学特征
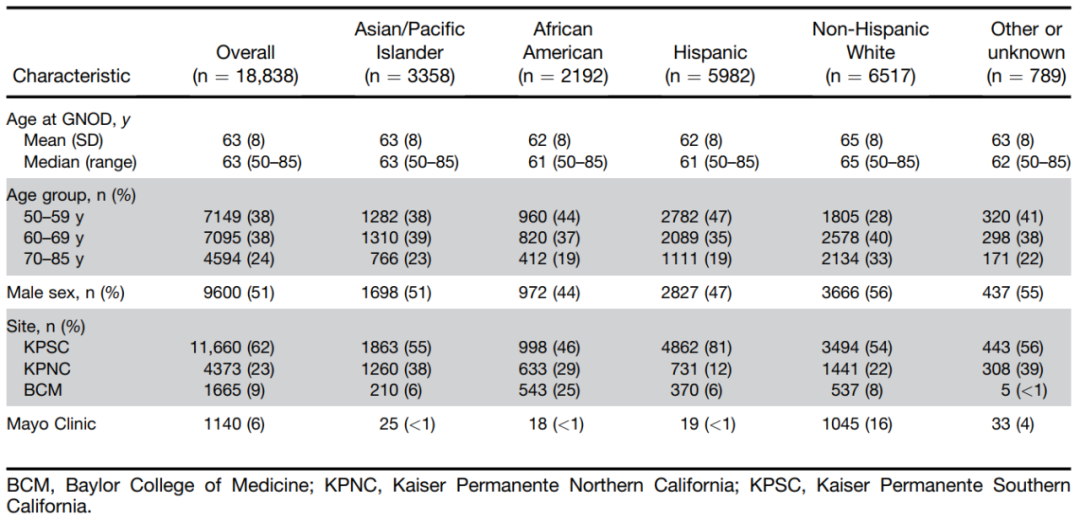
主要结局
中期分析时的中位随访时间为2.3年,期间共诊断出82例PDAC。根据研究标准,其中74例(90%)被归类为确诊PDAC,8例(10%)为疑似PDAC。PDAC患者的平均年龄为71岁,60%为男性。在PDAC患者中,60%为非西班牙裔白人,23%为西班牙裔,7%为非裔美国人,9%为亚洲/太平洋岛民。由于本研究为观察性研究,未进行早期检测干预。确诊时,大多数PDAC为Ⅳ期(65%),27%为Ⅰ/Ⅱ期,9%为Ⅲ期。
PDAC的标准化发病率:PDAC总体标准化发病率比(SIR)达4.6倍,且存在显著的种族和民族差异。其中,非西班牙裔白人患者的SIR最高(6.4,P<0.001)。西班牙裔(SIR=4.2,P<0.001)、非裔美国人(SIR=2.4,P=0.04)和亚洲/太平洋岛民患者(SIR=3.0,P=0.009)的风险也显著升高,但效应值较小。在年龄≥60岁的亚组中,非西班牙裔白人、西班牙裔、非裔美国人和亚洲/太平洋岛民患者的SIR分别为6.3、5.0、2.6和2.6(表2)。
表2. 针对不同种族和族裔群体中50岁及以上及60岁及以上、近期血糖升高与新发糖尿病患者PDAC发病率的分析结果
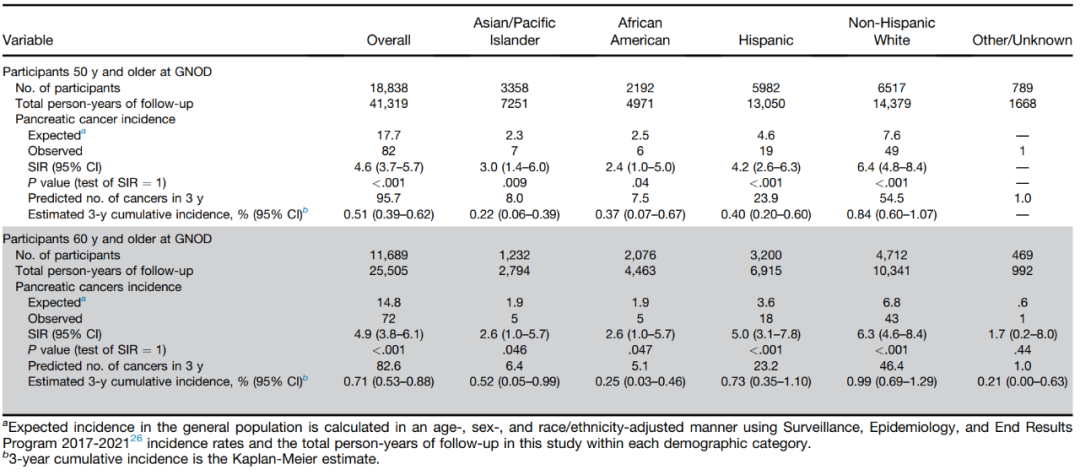
PDAC的绝对发病率:GNOD患者中PDAC的估计发病率为每1000人年2.0例(图1A)。总体估计3年发病率为0.51%(图1B)。非西班牙裔白人患者3年内被确诊为PDAC的预估风险为0.84%,西班牙裔(0.40%)、非裔美国人(0.37%)和亚洲/太平洋岛民患者(0.22%)的风险较低(表2)。在年龄≥60岁的亚组中,非西班牙裔白人、西班牙裔、非裔美国人和亚洲/太平洋岛民参与者的3年绝对发病率估计值分别为0.99%、0.73%、0.52%和0.25%(表2)。使用非PDAC死亡作为竞争风险计算的绝对发病率(总体及各种族和民族亚组)与上述结果相似。
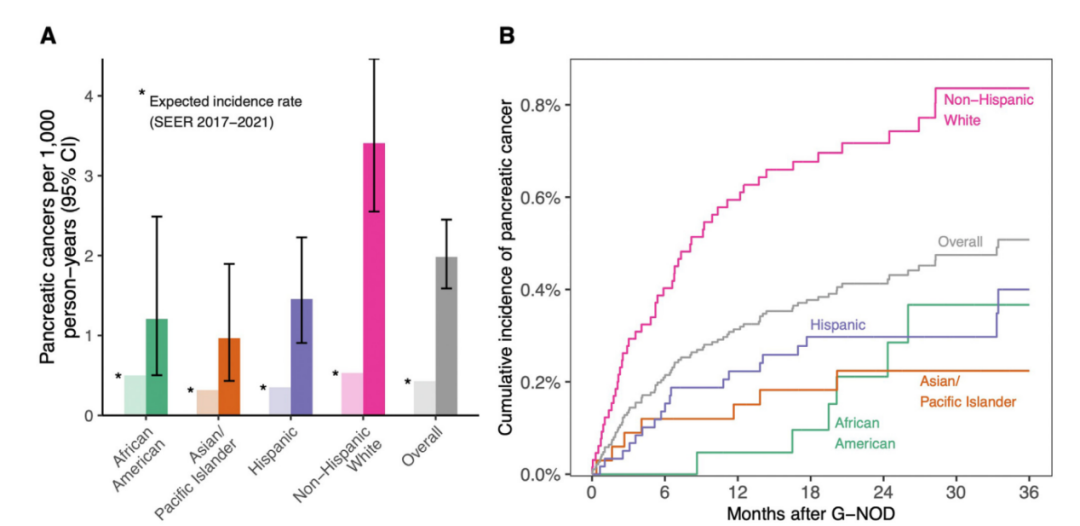
图1. PDAC发病率按种族和族裔群体划分,以(A)每1000人年观察发病率和(B)累积发病率呈现
PDAC发病的时间分布特征:从GNOD到PDAC确诊的中位时间的Kaplan-Meier估计值为8.1个月,其中估计有69.5%的患者时间窗在4个月或以上。在本研究确诊的所有PDAC患者中,61.8%在GNOD后12个月内确诊,19.5%在GNOD后12~24个月内确诊,18.7%在GNOD后24~36个月内确诊(图2)。
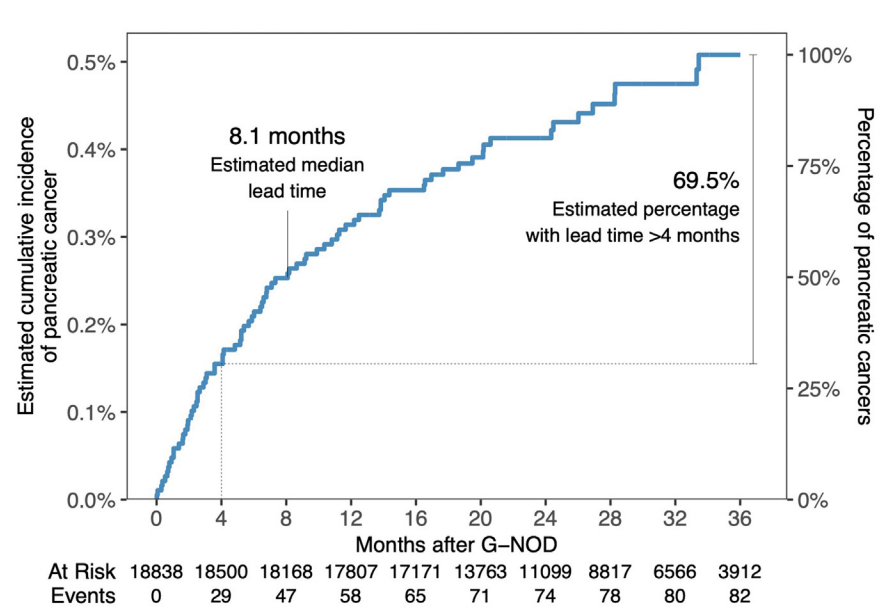
图2. 基于自GNOD日期起至确诊PDAC的时间差分布Kaplan-Meier估计图
次要结局
经种族调整的PDAC总体绝对发病率:根据种族和民族分布进行调整后,PDAC的总体3年绝对发病率为0.62%。与SIR类似,绝对发病率也存在种族和民族差异。
GNOD识别延迟对PDAC风险的影响:研究观察到SIR在第一年内呈渐进且显著下降(图3A)。这一现象在模拟情景中得以印证,若GNOD识别延迟6个月,将因排除那些在延迟确诊GNOD之前已确诊的PDAC病例,导致PDAC的SIR及绝对发病率被显著低估(图3B和C)。
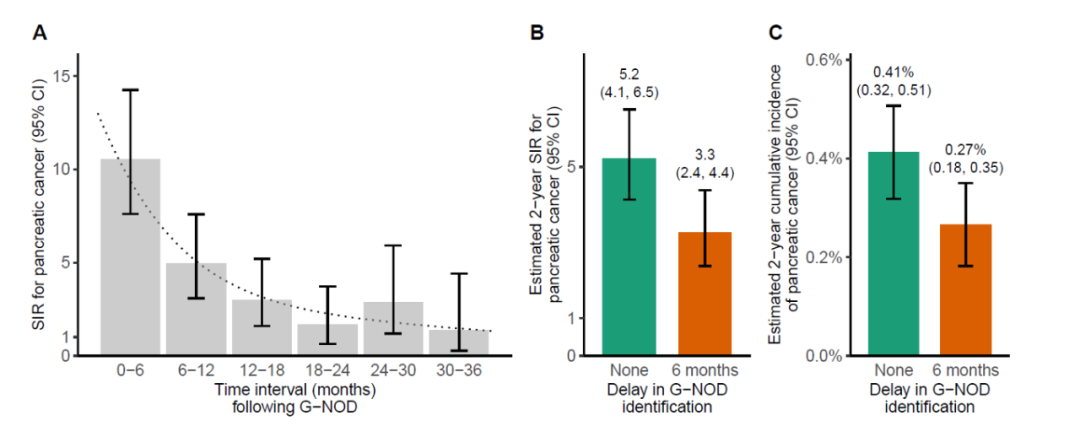
图3. GNOD识别延迟6个月带来的PDAC风险低估程度
研究结论
GNOD可通过电子健康记录的主动实时监测在全系统范围内实现自动化识别,并与PDAC的3年高发病率密切相关:非西班牙裔白人、西班牙裔、非洲裔美国人和亚裔/太平洋岛民的3年发病率依次为0.84%、0.40%、0.37%和0.22%,种族差异显著;GNOD出现的时间较PDAC临床诊断中位领先8.1个月,约70%的PDAC在GNOD后4个月以上才被诊断;对GNOD识别的延迟会显著低估PDAC风险。
小结
本研究首次通过多中心前瞻性队列设计与自动化电子健康记录监测,系统性评估了GNOD患者中PDAC的发病风险与时间特征。研究证实,GNOD人群在三年内发生PDAC的风险增高,SIR达4.6倍,且风险存在明显的种族差异,非西班牙裔白人群体风险尤为突出。同时,研究揭示从GNOD到PDAC临床确诊之间存在中位约8个月的时间窗口,约70%的病例在GNOD出现4个月后才被确诊,这为PDAC的早期监测提供了关键的时间依据。
研究结果凸显了基于血糖异常进行主动监测在识别散发性PDAC高危人群中具有一定的临床价值,也为开展分层筛查和早期干预提供了证据。未来可进一步整合临床生物标志物与影像学手段,构建更精准的风险预测模型,并通过前瞻性干预研究验证针对GNOD人群的早筛策略能否改善进一步PDAC患者的生存结局。
参考文献
1. Olesen SS, et al. Gastroenterology. 2026 Jan;170(1):12-14.
2. Chari ST, et al. Gastroenterology. 2026 Jan;170(1):106-117.
- 推荐文章
